微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
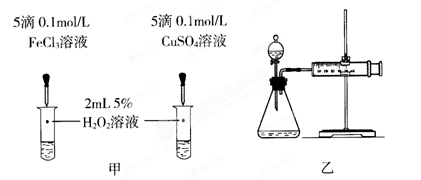
①定性分析:如图甲可通过观察_________________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_________________________。
②定量分析:用图乙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是________________________。
2、填空题 某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HC1挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题。

(1)若用含有0.2 mol HC1的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12L的原因是?。
(2)①装置B中盛放的试剂名称为?,作用是?。
装置C中盛放的试剂名称为?,作用是? ?。
?。
②装置D和E中出现的不同现象说明的问题是?。
③装置F的作用是____?。
④写出装置G中发生反应的离子方程式?。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在?与?之间(填装置字母序号),装置中应放入?(填写试剂或用品名称)
3、实验题 (16分)某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其发扬进行吸收处理。
(1)请完成SO2与过量NaOH溶液反应的化学方程式:SO2+2NaoH=_____________。
(2)反应Cl2+Na2SO3+2NaOH="2NaCl" + Na2SO4 +H2O中的还原剂为______________________-。
(3)吸收尾气一段时间后,吸收液(强碱性)吵肯定存在Cl-、OH-和SO42- 。请设计实验,探究该吸收液中可能存在的其它离子(不考虑空气的CO2的影响)
①提出合理假设
假设1:只存在SO32-
 假设2:既不存在SO32-也不存在ClO-
假设2:既不存在SO32-也不存在ClO-
假设3:_______ ______
______
②设计实验方案,进行实验。请在答题卡上写出实验步骤以及预期现象和结论。限选实验试剂:3moL L-1H2SO4、1moL
L-1H2SO4、1moL L-1NaOH、0.01mol
L-1NaOH、0.01mol L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
实验步骤
| 预期现象和结论
|
步骤1:取少量吸收液于试管中,滴加3 moL L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中 L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中
| 
|
步骤2:
| ?
|
步骤3:
| ?
4、计算题 将固体MnC2O4・2H2O放在一个可以称出质量的容器里加热,固体质量随温度变化
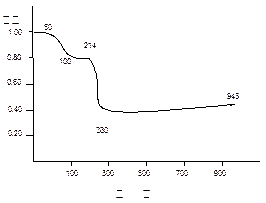
的关系如图所示(相对原子质量:H 1.0,? C 12.0,? O 16.0,? Mn 55.0 ):
纵坐标是固体的相对质量。
说出在下列五个温度区间各发生什么变化,并简述理由:
0~50℃;50~100℃;100~214℃;214~280℃;280~943℃
5、实验题 (12分) 甲、乙、丙、丁四位同学在探究碱溶液与酚酞作用的实验时,发现了一个意外现象:氢氧化钠溶液滴入酚酞试液,溶液变成了红色,可是过了一会儿红色就消失了。
[猜想]
甲:可能是酚酞变质造成的;
乙:可能是氢氧化钠溶液与空气中的二氧化碳反应的缘故;
丙:可能是酚酞与空气中的氧气反应,使红色消失;
丁:可能与氢氧化钠溶液浓度大小有关。
[理论分析]
(1)甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是:?
?;
(2)丙同学认为乙同学的猜想也不正确,他的理由是?
?。
[实验设计]
(3)为证实丙同学的猜想,还需做如下实验,请完成下表:
实验步骤
| 设计这一步骤的目的
| 1.将配制的氢氧化钠溶液加热??
| ?
| 2.在加热后的溶液中滴入酚酞,并在上方滴一些植物油?
| ?
|
(4)通过以上实验,四位同学观察到的现象是:溶液先变成红色,过了一会儿红色仍然消失。因此酚酞红色褪去与氧气无关。若丁同学的猜想正确,大家能设计实验证明吗?
实验方法
| 可能观察到的现象和结论
| 方案一:分别配制不同物质的量浓度的氢氧化钠溶液,然后各滴加数滴酚酞溶液。
| 物质的量浓度大的溶液中酚酞红色消失
证明?
| 方案二:向原红色消失的溶液中加?
(填试剂名称)
| 红色重新出现,则说明红色消失与氢氧化钠物质的量浓度大小有关
|
|