��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��������̼��̼�Ļ���������������ʵ����Ӧ�ù㷺��
(1)��2�����ܱ������У�����2mol CO��4mol ˮ�������ڴ��������½������»�ѧ��Ӧ��CO(g)+H2O(g) CO2(g)+H2(g)��CO��ת���ʺ��¶�t�Ĺ�ϵ���±���
CO2(g)+H2(g)��CO��ת���ʺ��¶�t�Ĺ�ϵ���±���
t(��)
| 750
| 850
| 1000
|
CO%
| 0.7
| 2/3
| 0.5
|
?
1000��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ___________________��850��ʱ���������������ͨ��1mol CO��1.5mol H2O��0.5mol CO2��2molH2����ʱ��Ӧ___________(����ҽ��С�����������С�����ƽ��״̬��)��
(2)��֪��C(s)��O2 (g) ===CO2(g) ��H1=��393.5kJ��mol��1
2H2(g)��O2(g)===?2H2O(g) ��H2=��483.6kJ��mol��1
C(s)��H2O(g)===?CO(g)��H2(g) ��H3=+131.3kJ��mol��1
��CO��H2O����CO2��H2���Ȼ�ѧ����ʽΪ_______________________________��
(3) Ŀǰ��ҵ�Ͽ���CO2������ȼ�ϼ״����йط�ӦΪ��
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ��H��-49.0 kJ��mol��1���������Ϊ1 L���ܱ������У�����
CH3OH(g)+H2O(g) ��H��-49.0 kJ��mol��1���������Ϊ1 L���ܱ������У�����
1mol CO2��3mol H2����Ӧ�����в��CO2��CH3OH(g)��Ũ����ʱ��ı仯��ͼ��ʾ��
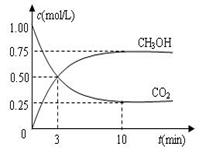
�ٴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v(H2)��_____________��
�����ı�����ʹƽ��������Ӧ�����ƶ�����ƽ�ⳣ��______________(�����)
a�����ܲ���?b�����ܼ�С ?c���������� ?d�����䡢��С��������п���
(4)NaHCO3��ˮ��Һ�ʼ��ԣ���ԭ����(����������)_______________________�������£���100mL
0.2mol/LNaHCO3��Һ�еμ�amol/L�Ĵ�����Һ�����μӵ���Һ������ʱ������ȥ�Ĵ�������պ�Ҳ
Ϊ100mL����ʱ����ĵ��볣��Ϊb�� �ú�b�Ĵ���ʽ��ʾ�����Ũ��a=_____________________��
2��ѡ���� ��ҵ�����������������Ⱦ���������·�Ӧ��
CH4(g)��2NO2(g) N2(g)��CO2(g)��2H2O(g) ?��H��a kJ/mol
N2(g)��CO2(g)��2H2O(g) ?��H��a kJ/mol
���¶�T1��T2ʱ���ֱ�0.50 molCH4��1.2 molNO2�������Ϊ1 L���ܱ������У����n(CH4)��ʱ��仯�������±���
�¶�
| ?ʱ��/min
n/mol
| 0
| 10
| 20
| 40
| 50
|
T1
| n(CH4)
| 0.50
| 0.35
| 0.25
| 0.10
| 0.10
|
T2
| n(CH4)
| 0.50
| 0.30
| 0.18
| ����
| 0.15
|
����˵������ȷ���ǣ�?��
A��10 min�ڣ�T1ʱ��(CH4)��T2ʱС? B���¶ȣ�T1��T2
C����H��a��0? D��ƽ�ⳣ����K(T1)��K(T2)
3��ѡ���� �ں��¡����ݵ������£��з�Ӧ2A��g��+2B��g�� C��g��+3D��g�����ִ�����;���ֱ���ƽ�⡣;��I��A��B����ʼŨ��Ϊ2mol��L��1��;��II��C��D����ʼŨ�ȷֱ�Ϊ2mol��L����6mol��L����������������ȷ����?��?��
C��g��+3D��g�����ִ�����;���ֱ���ƽ�⡣;��I��A��B����ʼŨ��Ϊ2mol��L��1��;��II��C��D����ʼŨ�ȷֱ�Ϊ2mol��L����6mol��L����������������ȷ����?��?��
A����;�����յ�ƽ��ʱ����ϵ�ڻ�����İٷ������ͬ
B����;�����մﵽƽ��ʱ����ϵ�ڻ�����İٷ���ɲ�ͬ
C����ƽ��ʱ��;��I�ķ�Ӧ����v��A������;��II�ķ�Ӧ����v��A��
D����ƽ��ʱ��;��I���û�������ܶ�Ϊ;��II���û�����ܶȵ�1/2
4��ѡ���� ��Ӧ4A��g��+5B��g��?4C��g��+6D��g����H=-Q?kJ/mol����һ���¶��´ﵽ��ѧƽ��״̬ʱ������˵����ȷ���ǣ�������
A��������ѹǿ��A��B��ת���ʶ�����
B���������¶����������ɸ����C��D
C����λʱ������4n?mol?A���ģ�ͬʱ��5n?mol?B����
D��������A��B��C��D��Ũ�ȱ���4��5��4��6
5��ѡ���� ��֪298Kʱ��Ӧ2SO2( g ) + O2( g )  2SO3( g )����H =" -197" kJ �� mol-1������ͬ�¶�����һ�ܱ������м���2 mol SO2��1 molO2���ﻯѧƽ��ʱ�ų�����Ϊa1 kJ ������һ�ݻ���ͬ���ܱ�������ͨ�� 1 mol SO2��0.5 molO2���ﻯѧƽ��ʱ�ų�����Ϊa2 kJ ,�����й�ϵʽ����ȷ���ǣ�?��
2SO3( g )����H =" -197" kJ �� mol-1������ͬ�¶�����һ�ܱ������м���2 mol SO2��1 molO2���ﻯѧƽ��ʱ�ų�����Ϊa1 kJ ������һ�ݻ���ͬ���ܱ�������ͨ�� 1 mol SO2��0.5 molO2���ﻯѧƽ��ʱ�ų�����Ϊa2 kJ ,�����й�ϵʽ����ȷ���ǣ�?��
A��2a2��a1�� 197
B��2a2��a1����197
C��2a2 = a1����197
D��2a2 = a1��= 197