微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关用惰性电极电解AgNO3溶液的说法不正确的是:
A.电解过程中阴极质量不断增大
B.电解过程中阳极附近的pH不断降低
C.电解一段时间后,向溶液中加入适量的Ag2O固体可使溶液恢复到电解前的状况
D.电解过程中,溶液中电子由阴极迁向阳极
参考答案:D
本题解析:A、电极过程中银镜反应为:Ag++e?=Ag,阴极质量不断增大,正确;B、电解过程中阳极水电离出的OH?失电子:4OH?-4e?=2H2O+O2↑,使水的电离平衡向右移动,H+浓度不断增大,所以pH不断降低,正确;C、电解一段时间后,向溶液中加入适量的Ag2O固体,Ag2O与HNO3反应生成AgNO3和H2O,可使溶液恢复到电解前的状况,正确;D、电解过程中,溶液中阴阳离子移动进行导电,电子不移动,错误。
本题难度:一般
2、选择题 储氢合金表面镀铜过程发生反应Cu2++2HCHO+4OH-=Cu +H2
+H2 +2H2O+2HCOO-,下列说法错误的是
+2H2O+2HCOO-,下列说法错误的是
A.电镀过程中氢气在镀件表面析出
B.电镀时溶液中Cu2+移向阴极,并在阴极上发生还原反应
C.阳极反应式为HCHO+3OH--2e-=2H2O+HCOO-
D.电镀时每生成6.4g铜镀层放出2.24L H2
参考答案:D
本题解析:A、根据化学方程式可知,电镀时阴极除了生成Cu外,还生成了H2,正确;B、根据电流方向,电镀时,阳离子向阴极移动,所以Cu2+移向阴极,并在阴极上发生还原反应,正确;C、HCHO在阳极上失去电子,C元素升高2价,所以失去2个电子,电解方程式为:HCHO+3OH--2e-=2H2O+HCOO-,正确;D、没有指明标准状况,无法求算H2的体积,错误。
本题难度:一般
3、填空题 铝和氢氧化钾都是重要的工业产品。请回答
(1)工业冶炼铝的化学方程式是__________________________________。
(2)铝与氢氧化钾溶液反应的离子方程式是__________________________________。
(3)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
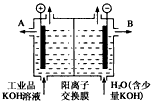
①该电解槽的阳极反应式是__________________________________。
②通电开始后,阴极附近溶液pH会增大,请简述原因________________________________。
③除去杂质后得氢氧化钾溶液从液体出口____________(填写A或B)导出。
参考答案:(1)2Al2O3 4Al+3O2↑
4Al+3O2↑
(2)2Al+2H2O+2OH-==2AlO2-+3H2↑
(3)①4OH--4e-==O2↑+2H2O;②H+放电,促进水的电离,OH-浓度增大;③B
本题解析:
本题难度:一般
4、选择题 用铂作电极,电解一定浓度的下列物质的水溶液,电解结束后,向剩余电解液中加适量水,能使溶液和电解前相同的是( )?
A.AgNO3
B.H2SO4?
C.NaOH
D.NaCl?
参考答案:A.电解AgNO3,阳极析出Ag,阴极生成O2,要使溶液恢复到原来的浓度,应加入Ag2O,故A错误;
B.电解硫酸,阳极生成氧气,阴极生成氢气,实际为电解水,电解后加入水可恢复到原来的浓度,故B正确;
C.电解NaOH,阳极生成氧气,阴极生成氢气,实际为电解水,电解后加入水可恢复到原来的浓度,故C正确;
D.电解食盐水,生成NaOH、H2、Cl2,加盐酸显然不能恢复电解前的状态,应通入适量的HCl气体,故D错误.
故选BC.
本题解析:
本题难度:简单
5、选择题 如图所示,在一U型管中装入含有紫色石蕊的Na2SO4试液,通直流电,一段时间后U型管内会形成一个倒立的三色 “彩虹”,从左到右颜色的次序是
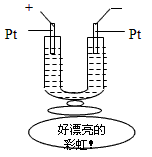
[? ]
A.蓝、紫、红
B.红、蓝、紫
C.红、紫、蓝
D.紫、红、蓝
参考答案:C
本题解析:
本题难度:一般