��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��ͼ��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��100?g?5.00����NaOH��Һ��������CuSO4��Һ��100?g?10.00����K2SO4��Һ���缫��Ϊʯī�缫��?
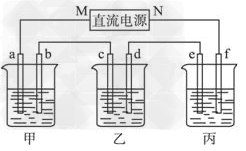
��1����ͨ��Դ������һ��ʱ���ñ���K2SO4Ũ��Ϊ10.47��������c�缫�������ӡ��ݴ˻ش����⣺
�ٵ�Դ��N��Ϊ___________����
�ڵ缫b�Ϸ����ĵ缫��ӦΪ________________��
�۵缫b�����ɵ������ڱ�״���µ������_____________________��
�ܵ缫c�������仯��__________g�� �ݵ��ǰ�����Һ��pHֵ�ı仯������䡱�������С��������Һ________������Һ________������Һ________��
��2�������������ͭȫ����������ʱ����ܷ�������У�Ϊʲô�� ____________________________________________________________��
�ο��𰸣���1����������4OH-��4e-��O2��+2H2O����2.8 L����16���ݼױ���Ҽ�С��������
��2����Cuȫ����������ҺΪϡ���ᣬ�����Ȼ��������
���������
�����Ѷȣ�һ��
2��ѡ���� ������Ʒ���������缫����NaHCO3��Һ�����Һ���е�⣬ͨ���������Ʒ����Һ�ĽӴ��������γ�һ��Al��OH��3��Ĥ����Ĥ��ijЩ��λ������С�ף����Һ��С��ͨ��������������ʹ���������ֽ⣬�Ӷ�������Ʒ�����γ�һ��Ϻ������Ĥ��������һ����������������ȷ���ǣ�������
A��������������������
B��ʹ��NaHCO3��Һ��Ϊ���Һ���ܼ�����������pH����
C�����Һ���뱣��pH���൱�ȶ�
D���õ�������������Ӧʽ�ǣ�Al-3e-=Al3+
�ο��𰸣�A�������ϻ��ý���ʧȥ���ӣ�������������������������A��ȷ��
B���������������������ӣ���HCO3-+OH-�TCO32-+H2O��֪����NaHCO3��Һ��Ϊ���Һ���ܼ�����������pH����B��ȷ��
C������в�����Al��OH��3��Al2O3�����������ʣ������Һ�����Ի�ǿ����ʱ�����γɵ�Al2O3��Ĥ�ᱻ���Һ�ܽ⣬�Ӷ�ʹ���Һ��pH�൱�ȶ�����C��ȷ��
D��������ӦΪAl-3e-+3HCO3-�TAl��OH��3��+3CO2������D����
��ѡD��
���������
�����Ѷȣ���
3������� ij������ʹ���վö���������־ģ��������������ҵ��������������ĺ��Լ����ش������жϸ�������ģ�������ص��������ķ�����
��1���Ȼ�ͭ��Һ����������ͭ���ߵ�̼����?��
��2������ͭ��Һ������ͭ���ߣ�?��
�ο��𰸣���1��������̼��Ϊ�缫��ɵ��أ����һ��ʱ�����������ɫ��̼�������ӵĵ缫Ϊ��������һ�缫Ϊ����
��2��ֱ��������ͭ����Ϊ�缫��ɵ��أ����һ��ʱ������������ܽ��ͭ���������ĵ缫Ϊ��������һ�缫Ϊ����
�����������1�������ء��Ȼ�ͭ��Һ����������ͭ���ߵ�̼�������һ�����أ���̼�����缫����������Ϊ���Ե缫���缫��ӦʽΪ2Cl--2e- Cl2���������ĵ缫��ӦʽΪCu2++2e-
Cl2���������ĵ缫��ӦʽΪCu2++2e- Cu����ԭ���ɵ�Cu������������̼���϶�ʹ̼���Ժ�ɫ�������Ϻ�ɫ��̼��Ϊ����������������������ĵ缫Ϊ��������2�������ء�����ͭ��Һ������ͭ���߿����һ�����أ�����ͭ����ֱ�����缫�����������ĵ缫��ӦʽΪCu-2e-
Cu����ԭ���ɵ�Cu������������̼���϶�ʹ̼���Ժ�ɫ�������Ϻ�ɫ��̼��Ϊ����������������������ĵ缫Ϊ��������2�������ء�����ͭ��Һ������ͭ���߿����һ�����أ�����ͭ����ֱ�����缫�����������ĵ缫��ӦʽΪCu-2e- Cu2+�������ĵ缫��ӦʽΪCu2++2e-
Cu2+�������ĵ缫��ӦʽΪCu2++2e- Cu�������ĵ缫��Ӧʹͭ�������ܽ���ܱ��ֳ���������ͬ���������ܽ��ͭ�����ǵ��ص�����������������������ĵ缫Ϊ������
Cu�������ĵ缫��Ӧʹͭ�������ܽ���ܱ��ֳ���������ͬ���������ܽ��ͭ�����ǵ��ص�����������������������ĵ缫Ϊ������
�����Ѷȣ���
4��ѡ���� һЩ��ѧ�Ҳ��ø����ӵ����Ե�SCY�մ�(�ܴ���H+)��ʵ���˰��ĵ绯ѧ�ϳɣ��ù���N2��H2��ת����Զ�������ڹ�ҵ��ʹ�õİ��ϳɷ������ڵ绯ѧ�ϳɰ����й�������ȷ����
[? ]
A��N2�������ϱ�����
B����ѡ������Ϊ��������
C�������ĵ缫��Ӧʽ��N2+6e-+6H+===2NH3
D���ù��̵��ܷ�Ӧʽ��N2+3H2 2NH3
2NH3
�ο��𰸣�D
���������
�����Ѷȣ�һ��
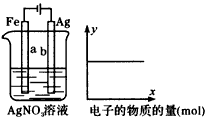
5��ѡ����& nbsp; ����ͼװ�ý���ʵ�飬����ͼ��x���ʾ���������ĵ��ӵ�������y��ɱ�ʾ������Щ�仯�������������ˮ�ֲ�������
[? ]
��c(Ag+)����c(NO3-)����a������������b��������������Һ��pH��
A���٢�
B���ۢ�
C���٢ڢ�
D���٢ڢ�
�ο��𰸣�D
���������
�����Ѷȣ�һ��