微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于粗盐提纯的下列说法中正确的是
A.溶解粗盐时,应尽量让溶液稀些,防止食盐不完全溶解
B.滤去不溶性杂质后,将滤液移至坩埚内加热浓缩
C.当蒸发到剩余少量液体时,停止加热,利用余热将液体蒸干
D.将制得晶体转移到新制过滤器中用大量水进行洗涤
2、实验题 (13分)实验室用下列方法测定某水样中O2的含量。
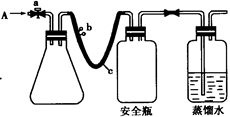
(1)实验原理
用如图所示装置,使溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为?。
再用I-将生成的MnO(OH)2再还原为Mn2+,反应的离子方程式为: MnO(OH)2+2I―+4H+=Mn2++I2+3H2O。
然后用Na2S2O3标准溶液滴定生成的I2,反应方程式为: I2+2Na2S2O3=2NaI+Na2S4O6。
(2)实验步骤
①打开止水夹a 和b,从A 处向装置内鼓入过量N2,此操作的目的是?;
②用注射器抽取某水样20.00 mL从A 处注入锥形瓶;
③再分别从A 处注入含m mol NaOH溶液及过量的MnSO4 溶液;
④完成上述操作后,关闭a、b,将锥形瓶中溶液充分振荡;
⑤打开止水夹a、b,分别从A 处注人足量NaI溶液及含n mol H2SO4的硫酸溶液;
⑥重复④的操作。
⑦取下锥形瓶,向其中加入2~3滴?作指示剂;
⑧用0.005 mol ・ L―1Na2S2O3滴定至终点。
(3)数据分析
①若滴定过程中消耗的Na2S2O3标准溶液体积为3.90 mL,则此水样中氧(O2)的含量为?(单位:mg・L―1)。
②若未用Na2S2O3标准溶液润洗滴定管,则测得水样中O2的含量将?(填“偏大”、“偏小”或“不变”)。
③实验要求加入适量的H2SO4使溶液接近中性,其原因是?。
3、选择题 下列制备设计错误的是
A.以苯为原料制水杨酸(邻羟基苯甲酸),应向苯环上先引入酚羟基
B.制备表面活性剂对十二烷基苯磺酸钠,可向苯环上先引入磺酸基(-SO3H)
C.制备十二烷基苯可以采用1-十二烯在一定条件下与苯加成
D.采用对MgCl2・6H2O在氯化氢气流中加热脱水制无水MgCl2
4、选择题 光卤石是化工生产中一种重要的中间产物,其化学成分是KCl・MgCl2・6H2O。当用光卤石为原料制取金属镁时,一共有下列几步:①过滤②溶解?③加入适量Ca(OH)2④蒸发⑤用盐酸溶解⑥电解熔融MgCl2⑦在HCl气流中强热MgCl2・6H2O晶体,正确的顺序是(? )?
A.⑤③①②④⑥⑦
B.②③①⑤④⑦⑥
C.②④①③⑦⑤⑥
D.⑤③①④②⑦⑥
5、选择题 下列叙述正确的是
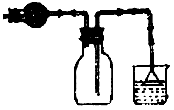
[? ]
A.①分液②过滤③分馏④重结晶都是混合物分离常用方法,其中根据粒子大小分离的只有②
B.欲配制质量分数为10%的硫酸铜溶液,可准确称取10 g硫酸铜晶体溶于90 g水中
C.中和滴定时,滴定前滴定管必须洗净并烘干
D.可用上图装置干燥、储存并吸收多余的HCl气体