Ԥ������ͽ���
��
______
______
��
______
______
��
______
______
______
______
��
��
��
�ο��𰸣���1���Ȼ�����ǿ����������ˮ�������������������ᣬ������ˮ�ⷽ��ʽΪFe3++3H2O?Fe��OH��3+3H+��
�ʴ�Ϊ��Fe3++3H2O?Fe��OH��3+3H+��
��2��Ӱ������ˮ��������У���Һ��Ũ�ȡ���Һ���¶ȡ�����Һ������ԣ�
�ʴ�Ϊ���Ȼ�����Һ��Ũ�ȣ���Һ���¶ȣ�?
��3���ٸ���Һ���ȣ��۲���Һ��ɫ�ı仯�������Һ��ɫ���˵�������¶��ܴٽ��Ȼ�����ˮ�⣬���ɸ���������������壮
������Һ��ͨ���Ȼ������壬�Ȼ�������ˮ���Ȼ������������ƶ��������ӣ������Ũ�����������Һ��ɫ��dz��˵����������������Ȼ���ˮ�⣮
������Ͳ��ȡ10ml?lmol/L�Ȼ������ձ��У���pH�Ʋ��pHֵ����ȡ90ml����ˮ�����ձ�����ֽ��裬����pH�Ʋ��pHֵ�����ǰ����pHֵ֮��С��1��˵����ˮϡ�ͺ�ƽ�����ƣ����ɸ����H+���������Ȼ���Ũ�ȣ�������ˮ�⣮
�ʴ�Ϊ��
������ʵ�����Ԥ������ͽ��ۢ����Թ��м���2ml?lmol/L�Ȼ������۲���Һ��ɫ������һ��ʱ�䣮���Ⱥ���Һ��ɫ���
˵�����´ٽ��Ȼ���ˮ�⣬���ɸ���������������壮����������Һ��ͨ��HCl����������Һ��ɫ��dz��˵��������ʹƽ�����ƣ��������Ȼ���ˮ�⣮������Ͳȡ10ml?lmol/L�Ȼ������ձ��У���pH�Ʋ��pHֵ����ȡ90ml����ˮ�����ձ�����ֽ��裬����pH�Ʋ��pHֵ��ǰ����pHֵ֮��С��1��˵����ˮϡ�ͺ�ƽ�����ƣ����ɸ����H+���������Ȼ���Ũ�ȣ�������ˮ�⣮
���������
�����Ѷȣ�һ��
2��ѡ���� �����£���NH4NO3����ˮ�õ���ɫ��Һ��Ϊʹ��Һ�е�c��NH4+����c��NO3-��=l��l���ɲ�ȡ�����д�ʩ��
A������������HNO3������NH4+ˮ��
B�����������İ�ˮ��ʹ��Һ��pH=7
C������������ˮϡ����Һ
D������������NaOH��ʹ��Һ��pH=7
�ο��𰸣�B
���������
�𰸣�B
A������������HNO3��NO3�D��Խ��Խ�࣬��NH4��Ũ�ȴ�B��ȷ��C��ˮ�ٽ�NH4����ˮ�⣻DNH4����OH�D=NH3��H2O
�����Ѷȣ�һ��
3������� ��10�֣���������Ũ�Ⱦ�Ϊ0.05mol/L��������Һ����Na2CO3��NaHCO3��HCl ��NH3��H2O���ش�������⣺
��1��������Һ�У��ɷ���ˮ�����?������ţ�
��2��������Һ�У�������NaOH��Һ��Ӧ��������H2SO4��Һ��Ӧ����
Һ�У�����Ũ�ȴ�С�Ĺ�ϵ?
��3������м�������NH4Cl���壬��ʱc(NH4+/OH-)��ֵ?������������С�����䡱 ��
��4�������ۺܵ͢���Һ��Ϻ���Һǡ�ó����ԣ�����ǰ�۵����?�ܵ�����������ڡ�����С�ڡ����ڡ� ��
��5��ȡ10mL�Ģ���Һ����ˮϡ�͵�500mL�������Һ����ˮ�������c(H+) =?mol/L
�ο��𰸣���10�֣�
��1��?�٢�?
��2��? c(Na+)�� c(HCO3��) �� c(OH��) �� c(H+)�� c(CO32��)?
��3��?����??��4��?��?
��5��? 10-11?
�����������1��������Һ�У�ֻ�к��������Ӳ���ˮ�⣬���ԣ�������Һ�пɷ���ˮ����ǣ�Na2CO3��NaHCO3��������٢�
��2��������NaOH��Һ��Ӧ��������H2SO4��Һ��Ӧ����Һָ����NaHCO3��NaHCO3��Һ�Լ��ԣ�HCO3����ˮ��̶ȴ��ڵ���̶� ������Ũ�ȵĴ�С��ϵ�ǣ�c(Na+)�� c(HCO3��) �� c(OH��) �� c(H+)�� c(CO32��)
��3������м�������NH4Cl���壬�ܴ���һˮ�ϰ��ĵ���ƽ�⣬��������Ũ������ƽ�����ƣ���ʱc(NH4+/OH-)��ֵ����
��4�������ۺܵ͢���Һ��Ϻ�õ��Ȼ�泥���Һǡ�ó����ԣ���ˮӦ�ù��������ԣ����ǰ�۵����С�ڢܵ����
��5��0.05mol/L10mL��HCl��Һ����ˮϡ�͵�500mL����ʱ�����Ũ��Ϊ0.001mol/L, c(H+) = 10-3mol/L,��ôˮ�������c(H+)=10-11mol/L
�����Ѷȣ�һ��
4��ѡ���� �������ӷ�Ӧ����ʽ�У�����ˮ�ⷴӦ����
A��CN����H2O HCN��OH�� HCN��OH��
B��NH3��H2O NH4+��OH�� NH4+��OH��
C��HCO3-��H2O H3O����CO32- H3O����CO32-
D��H2CO3 HCO3-��H�� HCO3-��H��
�ο��𰸣�A
���������
��ȷ��:A
B�����룻C�����룻D�����롣
�����Ѷȣ�һ��
5��ѡ���� ����Ũ�Ⱦ�Ϊ0.1mol/L��MgCl2��Һ����ˮ��Һ���������1:2��ϡ���֪Mg(OH)2��Ksp=4.0��10��12������˵����ȷ����
A�����ǰ����ˮ��Һ��c(NH4+)��c(OH��)=1��1
B����Ϻ�c(NH4+)��c(Cl��)=1��1
C����Ϻ�c(Mg2+)��c(OH��)= 4.0��10��12
D�����Ϻ�ķ�ɢϵ�м���FeCl3��Һ����ɫ��������ɫ
�ο��𰸣�D
���������A����ˮ�д�����������ƽ�⣺NH3?H2O 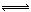 NH4++OH?��H2O NH4++OH?��H2O 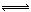 H++OH?������OH?��Ũ�ȴ���NH4+��Ũ�ȣ�����B����Ϊ0.1mol/L��MgCl2��Һ����ˮ��Һ���������1:2��ϣ�����Mg(OH)2��NH4Cl����ΪNH4+ˮ�⣬����c(NH4+) < c(Cl��)������C������Ksp�ĺ��壬Ksp= c(Mg2+)��c(OH��)2= 4.0��10��12������D�����Ϻ�ķ�ɢϵ�м���FeCl3��Һ��Mg(OH)2ת��Ϊ�����ܵ�Fe(OH)3����������ɫ��������ɫ����ȷ��sp�ĺ�����Ӧ�á�����ƽ�⡢�����ˮ�⡣ H++OH?������OH?��Ũ�ȴ���NH4+��Ũ�ȣ�����B����Ϊ0.1mol/L��MgCl2��Һ����ˮ��Һ���������1:2��ϣ�����Mg(OH)2��NH4Cl����ΪNH4+ˮ�⣬����c(NH4+) < c(Cl��)������C������Ksp�ĺ��壬Ksp= c(Mg2+)��c(OH��)2= 4.0��10��12������D�����Ϻ�ķ�ɢϵ�м���FeCl3��Һ��Mg(OH)2ת��Ϊ�����ܵ�Fe(OH)3����������ɫ��������ɫ����ȷ��sp�ĺ�����Ӧ�á�����ƽ�⡢�����ˮ�⡣
�����Ѷȣ�һ��
|