��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �������������������й㷺Ӧ�á�
��ҵ�����ؾ�ʯ����Ҫ�ɷ�BaSO4��Ϊԭ���Ʊ�BaCl2���乤������ʾ��ͼ���£�
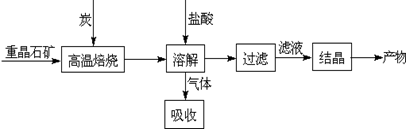
ij�о�С��������ϵã�
BaSO4��s��+4C��s�� 4CO��g��+BaS��s����H1=+571.2kJ?mol-1 ��
4CO��g��+BaS��s����H1=+571.2kJ?mol-1 ��
BaSO4��s��+2C��s�� 2CO2��g��+BaS��s����H2=+226.2kJ?mol-1 ��
2CO2��g��+BaS��s����H2=+226.2kJ?mol-1 ��
��1���ù���NaOH��Һ�������壬�õ����ơ��÷�Ӧ�����ӷ���ʽ�� ��
��2����ӦC��s��+CO2��g�� 2CO��g���ġ�H= ��
2CO��g���ġ�H= ��
��3��ʵ�������б�����������̿��ͬʱ��Ҫͨ���������Ŀ��������
�ٴ�ԭ�ϽǶȿ��� ��
�ڴ������Ƕȿ����٢�Ϊ���ȷ�Ӧ��̿��������Ӧ����ά�ַ�Ӧ������¡�
��4����С��ͬѧ���BaSO4��ˮ�еij����ܽ�ƽ������һ���о��������Ϸ�����ij�¶�ʱBaSO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ��
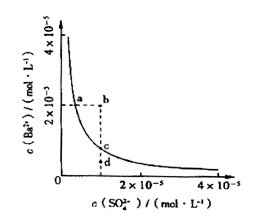
��С��ͬѧ����������ֹ۵㣺
�ٵ�����SO42-����Һ�м���Ba2+ ʹSO42-������ȫ�����ʱSO42-����Һ�е�Ũ��Ϊ0
�ڼ���Na2SO4����ʹ��Һ��a��䵽b��
��ͨ����������ʹ��Һ��d��䵽c��
��d����BaSO4��������
������ȷ���� ������ţ���
��ijȼ�ϵ����CaHSO4����Ϊ����ʴ���H+��������ṹ��ͼ��ʾ������ܷ�Ӧ�ɱ�ʾΪ2H2+O2
�ο��𰸣�
���������
�����Ѷȣ�����
2������� п���̸ɵ�����ձ�ʹ�õĻ�ѧ��أ����к���MnO2��NH4Cl��ZnCl2�Ⱥ�״���пͲΪ�������ϣ�ʯīΪ�������ϡ�
����ʱ��Ӧ����ʽ�ǣ� Zn+2MnO2+2NH4+��Zn2++Mn2O3+2NH3+H2O
��1����д���ɵ�طŵ�ʱ���������缫��Ӧʽ��������_____________������_____________���ɵ���þ��˾ͻ��������ԭ����_______________��
��2��������Ӧ�У�ǰ�������з�Ӧ��2NH4++2e-��2NH3+H2��2MnO2+H2��Mn2O3+H2O�����û��MnO2���룬�ɵ�ؽ����ڳ����ȶ���������˵�����ɣ�_____________________________��
�ο��𰸣���1��������2NH4++2MnO2+2e-=2NH3+Mn2O3+H2O��������Zn-2e-=Zn2+����طŵ��������ˮ������пͲ�䱡��ɸɵ�ر�����
��2��������Ӧ���м����H2������ʯī�����ӵ�����衣
���������
�����Ѷȣ�һ��
3������� ������ͼ�ش��������⣺
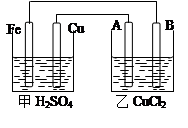
��A��B��Ϊ̼������������Һ��������
��1����װ����?�أ���װ����?����Fe��Ϊ?����A��Ϊ?��
��2��A���ĵ缫��Ӧ??
��3�����׳���Fe�ܽ�0��3 mol�����ҳ��в���������������״����Ϊ?L��
�ο��𰸣���1��ԭ��أ����أ�����������?��2��2Cl��---2e-? == Cl2��?��3��6��72
�����������1��ԭ�����һ�����2�����Բ�ͬ�����������Ը�װ���м׳���ԭ��أ����ǵ��أ�����������ͭ����������A��������
��2��A����������������Ӧ�������ӷŵ磬���������ӵõ��������������缫��ӦʽΪ2Cl��---2e-? == Cl2����
��3�����׳���Fe�ܽ�0��3 mol����װ����ת��0��6mol���ӣ��ҳ���ֻ��A������0��3mol��������״���µ������0��3mol��22��4L/mol=6��72L��
�����Ѷȣ�һ��
4������� ����������ɴ���ʹ�õ�������ȼ�ϵ�أ������ܷ�ӦΪ��2H2+O2�T2H2O���Իش��������⣺
��1�����������ҺΪKOH��Һ������ȼ�ϵ�أ���
�ٸ�����ӦʽΪ______
��������ӦʽΪ______
�۹���һ��ʱ�����ҺpH______�������С�����䡱��
��2�����KOH��ΪϡH2SO4������ʣ���
�ٸ�����ӦʽΪ______
��������ӦʽΪ______
�۹���һ��ʱ�����ҺpH______�������С�����䡱����
��3�����H2��Ϊ���飬KOH������ʣ���������ӦʽΪ______��
�ο��𰸣���1���ٸ÷�Ӧ������ʧ���ӱ�����������ʧ�������������ӣ������Ӻ���Һ�е���������������ˮ�����Ե缫��ӦʽΪ2H2+4OH--4e-=4H2O��
�������õ��ӱ���ԭ�������õ��Ӻ�ˮ��Ӧ�������������ӣ����Ե缫��ӦʽΪO2+2H2O+4e-=4OH-��
�����ŷ�Ӧ�Ľ��У����ɵ�ˮԽ��Խ�࣬�����������ص������䣬���Ե�����Һ��Ũ�Ƚ��ͣ�������Һ��PHֵ��С��
�ʴ�Ϊ����2H2+4OH--4e-=4H2O����O2+2H2O+4e-=4OH-�� �ۼ�С��
��2���÷�Ӧ������ʧ���ӱ�����������ʧ�������������ӣ����Ե缫��ӦʽΪ2H2-4e-�T4H+
�������õ��ӱ���ԭ�������õ��Ӻ���Һ�е�����������ˮ�����Ե缫��ӦʽΪO2+4H++4e-�T2H2O��
�����ŷ�Ӧ�Ľ��У����ɵ�ˮԽ��Խ�࣬��������������䣬���Ե�����Һ��Ũ�Ƚ��ͣ�������Һ��PHֵ����
�ʴ�Ϊ����2H2-4e-�T4H+����O2+4H++4e-�T2H2O��������
��3�������ϼ���ȼ�����ɶ�����̼��ˮ������ʧ���ӷ���������Ӧ���ɶ�����̼��������̼����Һ�е��������ط�Ӧ����̼��غ�ˮ��
�����������õ��Ӻ�ˮ��Ӧ�������������ӣ����Ե缫��ӦʽΪ��O2+2H2O+4e-�T4OH-��
�ʴ�Ϊ��O2+2H2O+4e-�T4OH-��
���������
�����Ѷȣ�һ��
5������� ��8�֣���ͼ��̽����ͬ�����»�ѧ��ת��Ϊ���ܵ�װ�á���ش��������⣺
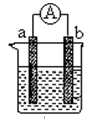
��1�����缫aΪAl���缫bΪCu���������ҺΪϡ����ʱ�������ĵ缫��ӦʽΪ�� �����һ�缫��������5.4 g������һ���ų���������Ϊ L����״������
��2��ȼ�ϵ�صĹ���ԭ���ǽ�ȼ�Ϻ�������(��O2)��Ӧ���ų��Ļ�ѧ��ֱ��ת��Ϊ���ܡ������һȼ�ϵ�أ��Ե缫aΪ�������缫bΪ����������Ϊȼ�ϣ�����KOH��ҺΪ���Һ��������Ӧͨ�� ������a ��b����ͬ�������Ӵ� ��������
a �������缫��ӦʽΪ��_____________________________��
�ο��𰸣���1��Al-3e-= Al3+��2�֣� 6.72 L��2�֣�
(2) ��2��b b ����2�֣���1�֣� O2+2H2O+4e-=4OH- ��2�֣�
���������Al---H2SO4-----Cu��ԭ�������������Al-3e-= Al3+��ͭ������2H++2 e-=H2��
ȼ�ϵ���л�ԭ��Ϊ������������Ϊ����������Ϊ���������ӴӸ���������������+��O2+2H2O+4e-=4OH-
�����Ѷȣ�һ��