微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 实验室中,用如下图所示装置及所给药品(图中部分夹持仪器已略去)探究工业制硫酸接触室中的反应,并测定此条件下二氧化硫的转化率。已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略装置内空气中的CO2。
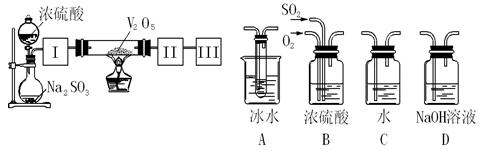
(1)已知0.5molSO2被O2氧化成气态SO3,放出49.15 kJ热量,反应的热化学方程式为?。
(2)根据实验目的,请从上面右图中选择Ⅰ、Ⅱ、Ⅲ处合适的装置,将其序号填入空格中:装置Ⅰ?,装置Ⅱ?,装置Ⅲ?。
(3)开始进行实验时,首先应进行的操作是?。
(4)加热硬质玻璃管时,若不断升高温度,SO2的转化率会?(填“增大”、“不变”或“减小”)。
(5)停止通入SO2,熄灭酒精灯后,为使残留在装置中的SO2、SO3被充分吸收,操作方法是?。
(6)实验结束后,若装置Ⅱ增加的质量为b g ,装置Ⅲ增加的质量为a g,则此条件下二氧化硫的转化率是?(用含字母的代数表示)。
2、选择题 下列反应中,SO2不是作为还原剂而发生反应的是
?
A.2SO2+O22SO3
B.SO2+H2O H2SO3
H2SO3
C.SO2+2H2S====3S↓+2H2O
D.SO2+Cl2+2H2O====H2SO4+2HCl
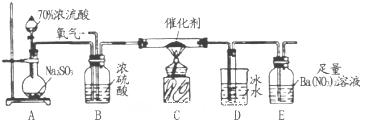
3、实验题 二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。 (1)T业上用黄铁矿(FeS2)在高温下和氧气反应制备SO2:4FeS2+11O2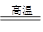 8SO2+2Fe2O3该反应中被氧化的元素是_______(填元素符号)。当该反应转移2. 75mol电子时,生成的二氧化硫在标准状况下的体积为_______L。
8SO2+2Fe2O3该反应中被氧化的元素是_______(填元素符号)。当该反应转移2. 75mol电子时,生成的二氧化硫在标准状况下的体积为_______L。
(2)实验室中用下列装置测定SO2催化氧化为SO3的转化率(已知SO3。熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略空气中CO2的影响)。
①简述使用分液漏斗向圆底烧瓶中滴加浓硫酸的操作是______。
②当停止通入SO2,熄灭酒精灯后,需要继续通一段时间的氧气,其目的是______。
③实验结束后,若装置D增加的质量为mg,装置E中产生白色沉淀的质量为ng,则此条件下二氧化硫的转化率是______(用含字母的代数式表示,不用化简)。
(3)某兴趣小组欲在绿色环保的条件下探究SO2的性质,设计如下图实验装置。
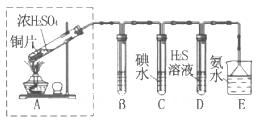
B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为_______;
C中反应的离子方程式为______ ;D中的实验现象为______ ;E装置的作用是______。
4、实验题 用下图装置进行实验。
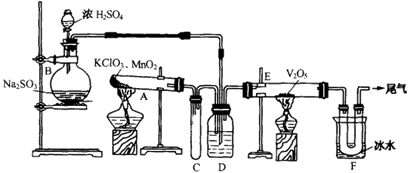
回答有关问题:
(1)玻璃管E内发生反应的化学方程式是?。
(2)小试管C的作用是?。
(3)广口瓶D内盛的试剂是?,装置D的3个作用是①?, ②?, ③?。
(4)从管E导出的气体成分是?。
(5)装置F中U形管观察到所收集物质的颜色状态是?。
(6)若U形管内收集到的物质很少,分析其原因不可能是?(填标号)。
a.装置气密性不好; b.制得的SO2中混有少量H2S杂质使催化剂中毒;c.气流速度过快。
(7)从U形管导出的尾气的处理方法是?。
5、选择题 下列反应中,浓硫酸表现出强氧化性的是
①用铁槽车盛装浓硫酸?②铜片与浓硫酸共热制备SO2
③将含水蒸气的氯气通过盛浓硫酸的洗气瓶
④浓硫酸吸收NH3?⑤浓硫酸使蔗糖炭化时有刺激性气体产生
A.①②④
B.③④⑤
C.①②⑤
D.②⑤