��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ͬ�ݻ����ĸ��ܱ������н���ͬ���Ŀ��淴Ӧ��2X��g����Y��g�� 3W��g����2Z��g����ʼʱ�ĸ�������װX��Y�����ֱ�Ϊ���ף�X��2mol��Y��1mol��?�ң�X��1mol��Y��1mol������X��2mol��Y��2mol��?����X��1mol��Y��2mol������ͬ�¶��£�����ƽ��ʱ��X��Y��ת���ʴ�С��ϵΪ
3W��g����2Z��g����ʼʱ�ĸ�������װX��Y�����ֱ�Ϊ���ף�X��2mol��Y��1mol��?�ң�X��1mol��Y��1mol������X��2mol��Y��2mol��?����X��1mol��Y��2mol������ͬ�¶��£�����ƽ��ʱ��X��Y��ת���ʴ�С��ϵΪ
A��X��ת����Ϊ���ף������ң���
B��X��ת����Ϊ���ף��ң�������
C��Y��ת����Ϊ���ף������ң���
D��Y��ת����Ϊ�������ң�������
�ο��𰸣�A
������������൱�����ҵĻ�����������X�����ʵ��������Լ���Y��ת���ʴ�������Y��ת���ʣ���X��ת����ҪС������X��ת���ʣ����൱�����ҵĻ�����������Y�����ʵ��������Զ���X��ת���ʴ�������X��ת���ʣ���Y��ת����ҪС������Y��ת���ʣ���������ȣ��൱��������ѹǿ����������Ӧ���������Ŀ��淴Ӧ������ƽ�����淴Ӧ�����ƶ������X��Yת���ʾ����ͣ����ͼ���ȣ��൱���ڼĻ�����������Y�����ʵ��������Ա���X��ת���ʴ��ڼ���X��ת���ʣ���Y��ת����ҪС�ڼ���Y��ת���ʣ����Ͷ���ȣ��൱���ڶ��Ļ�����������X�����ʵ��������Ա���Y��ת���ʴ��ڶ���Y��ת���ʣ���X��ת����ҪС�ڶ���X��ת���ʡ�����ʼʱ������������У�
2X��g����Y��g�� 3W��g����2Z��g��
3W��g����2Z��g��
�� 2 mol 1 mol
�� 1 mol 1 mol
�� 2 mol 2 mol
�� 1 mol 2 mol
XԽ��YԽ�࣬X��ת����Խ�ߣ���Xת������ߵ�Ϊ������͵�Ϊ�ף��������Ƚϣ����൱�����ҵĻ������ٷֱ�����1 mol X��1 mol Y�����Ǻ���Ϊ��ѹ��ƽ�������ƶ�ʹX��ת���ʼ�С����X��ת���ʼף������ң�����ͬ����Y��ת���ʣ����������ң��ף���˴�ѡA��
�����Ѷȣ�һ��
2��ѡ���� ���жԻ�ѧƽ���ƶ��ķ����У�����ȷ����
���Ѵ�ƽ��ķ�ӦC(s)+H2O(g) CO(g)+H2(g)�������ӷ�Ӧ�����ʵ���ʱ��ƽ��һ��������Ӧ�����ƶ�
CO(g)+H2(g)�������ӷ�Ӧ�����ʵ���ʱ��ƽ��һ��������Ӧ�����ƶ�
���Ѵ�ƽ��ķ�ӦN2(g)+3H2(g) 2NH3(g)��������N2��Ũ��ʱ��ƽ��������Ӧ�����ƶ���N2��ת����һ������
2NH3(g)��������N2��Ũ��ʱ��ƽ��������Ӧ�����ƶ���N2��ת����һ������
��2��0molPCl3��1��0molCl2������ݵ��ܱ������У�������Ӧ��PCl3(g)+ Cl2(g) PCl5��g����ƽ��ʱ��PCl5Ϊ0��4mol�������ʱ����1��0 molPCl3 ��0��50 molCl2������ͬ�¶����ٴ�ƽ��ʱPCl5�����ʵ���Ӧ����0��20mol��С��0��40mol
PCl5��g����ƽ��ʱ��PCl5Ϊ0��4mol�������ʱ����1��0 molPCl3 ��0��50 molCl2������ͬ�¶����ٴ�ƽ��ʱPCl5�����ʵ���Ӧ����0��20mol��С��0��40mol
��������μӵķ�Ӧ��ƽ��ʱ���ں�ѹ��Ӧ���г���ϡ�����壬ƽ�ⲻ�ᷢ���ƶ�
A���٢�
B���٢ڢ�
C���ڢۢ�
D���٢ڢۢ�
�ο��𰸣�D
������������Ѵ�ƽ��ķ�ӦC(s)+H2O(g) CO(g)+H2(g)��̼�ǹ��壬����̼������ƽ�ⲻ�ƶ��������Ѵ�ƽ��ķ�ӦN2(g)+3H2(g)
CO(g)+H2(g)��̼�ǹ��壬����̼������ƽ�ⲻ�ƶ��������Ѵ�ƽ��ķ�ӦN2(g)+3H2(g) 2NH3(g)��������N2��Ũ��ʱ��ƽ��������Ӧ�����ƶ���N2��ת���ʽ��ͣ���ߵ���������ת���ʣ���2��0molPCl3��1��0molCl2������ݵ��ܱ������У�������Ӧ��PCl3(g)+ Cl2(g)
2NH3(g)��������N2��Ũ��ʱ��ƽ��������Ӧ�����ƶ���N2��ת���ʽ��ͣ���ߵ���������ת���ʣ���2��0molPCl3��1��0molCl2������ݵ��ܱ������У�������Ӧ��PCl3(g)+ Cl2(g) PCl5��g����ƽ��ʱ��PCl5Ϊ0��4mol�������ʱ����1��0 molPCl3 ��0��50 molCl2���൱�ڼ�ѹ��ƽ�������ƶ�������ͬ�¶����ٴ�ƽ��ʱPCl5�����ʵ���ӦС��0��20mol������������μӵķ�Ӧ��ƽ��ʱ���ں�ѹ��Ӧ���г���ϡ�����壬ѹǿ���䣬������ӣ�Ũ�ȱ仯�����ڷ���ʽ����������ϵ�����ȵķ��̣�ƽ�⽫�ᷢ���ƶ���������˴�ѡD��
PCl5��g����ƽ��ʱ��PCl5Ϊ0��4mol�������ʱ����1��0 molPCl3 ��0��50 molCl2���൱�ڼ�ѹ��ƽ�������ƶ�������ͬ�¶����ٴ�ƽ��ʱPCl5�����ʵ���ӦС��0��20mol������������μӵķ�Ӧ��ƽ��ʱ���ں�ѹ��Ӧ���г���ϡ�����壬ѹǿ���䣬������ӣ�Ũ�ȱ仯�����ڷ���ʽ����������ϵ�����ȵķ��̣�ƽ�⽫�ᷢ���ƶ���������˴�ѡD��
�����Ѷȣ�һ��
3������� �����ǹ�ҵ����Ҫ��ԭ�ϡ�
��1���������ڹ�ҵ�ϳɰ�? N2(g) + 3H2(g) 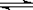 ?2NH3(g)����H =" -92.2" kJ��mol-1��
?2NH3(g)����H =" -92.2" kJ��mol-1��
��?һ���¶��£����ݻ��㶨���ܱ������У�һ������N2��H2��Ӧ�ﵽƽ��ı�ijһ�����������Ӧ������ʱ��Ĺ�ϵ����ͼ��ʾ������t4?�pt5�pt7ʱ������Ӧ��ʵ�������ı�ֱ���
t4??t5??t7?��

���¶�ΪT��ʱ����2amolH2��amolN2����0.5L�ܱ������У���ַ�Ӧ����N2��ת����Ϊ50������ʱ�ų�����46.1 kJ������¶��·�Ӧ��ƽ�ⳣ��Ϊ?��?
��2����ҵ�ϴ�����������Դ�ڽ�̿��ˮ���������µķ�Ӧ��
C(s) + H2O(g) 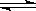 ?H2(g) + CO(g)? ��H =" +131.3" kJ/mol
?H2(g) + CO(g)? ��H =" +131.3" kJ/mol
�ٸ÷�Ӧ�ڵ����²����Է����е�ԭ����?��
�ں��£����ݻ��ɱ���ܱ������У��������Ͽ��淴Ӧ��һ��ʱ��������������������仯ʱ���ܱ����÷�Ӧ�Ѵﵽƽ��״̬���У�����������ܶȣ��������������ѹǿ����������������ʵ����� ��CO���ʵ���Ũ��?��?��
A��ֻ�Т�?B��ֻ�Т�͢�?C��ֻ�Т�͢�?
D����͢�?E��������
��3�����ݻ���ͬ�����ܱ�����A��B�У������¶�Ϊ423K��ͬʱ��A��B�зֱ����amol��bmol�⻯�⣨a��b������Ӧ��2HI(g)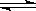 H2(g)+I2(g)?�ﵽƽ���ƽ��ʱI2��Ũ��c(I2)A?c(I2)B?��ƽ��ʱHI�ķֽ��ʦ�A?��B?��ƽ��ʱH2�ڻ�������е��������A?B ����д��������������������
H2(g)+I2(g)?�ﵽƽ���ƽ��ʱI2��Ũ��c(I2)A?c(I2)B?��ƽ��ʱHI�ķֽ��ʦ�A?��B?��ƽ��ʱH2�ڻ�������е��������A?B ����д��������������������
�ο��𰸣���1����t4 ?����������??t5?��СNH3Ũ��??t7?����?
��? 4.0??
��2�����÷�Ӧ�SH��0 �SS��0 ���ݨSG = �SH�CT�SS?���¡��SG��0�����Է�??
�� ?D?
��3��?��??��??��?��??��?
�����������
�����Ѷȣ�һ��
4��ѡ���� ��һ�������£���2L�ܱ������м���2 mol N2��10 mol H2������ӦN2��3H2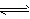 2NH3,2 minʱ�����ʣ��N2Ϊ1 mol�����ڴ˻�ѧ��Ӧ���ʱ�ʾ����ȷ����
2NH3,2 minʱ�����ʣ��N2Ϊ1 mol�����ڴ˻�ѧ��Ӧ���ʱ�ʾ����ȷ����
[? ]
A��v(N2)��0.25 mol��L��1��min��1
B��v(H2)��0.75 mol��L��1��min��1
C��v(NH3)��1 mol��L��1��min��1
D��v(N2)��0.5 mol��L��1��min��1
�ο��𰸣�CD
���������
�����Ѷȣ���
5��ѡ���� ������������ԭ�����͵��ǣ�?��?
A������ɫ��NO2����ѹ����ɫ�ȱ�����dz
B����ҵ�Ϻϳ�NH3��Ӧʹ�ô���
C��ʵ���ҿ��Բ����ű���ʳ��ˮ�ռ�Cl2
D����H2��I2(g)��HI(g)������ɵ�ƽ����ϵ��ѹ����ɫ����
�ο��𰸣�AC
�����������������������ʱ���ı�Ӱ��ƽ���һ��������ƽ������ܼ������ָı�ķ�����У��������������ԭ������NO2�д���ƽ��2NO2 N2O4������ѹǿƽ��������Ӧ�����ƶ�������A��ȷ���������ܸı�ƽ��״̬����������������ԭ�����͡�����ʳ��ˮ�������ӵ�Ũ�ȴ��������������ܽ⣬��ȷ��D�еĿ��淴Ӧ�Ƿ�Ӧǰ���������ģ����Ըı�ѹǿ��ƽ�ⲻ�ƶ�����������������ԭ�����͡�����AC��
N2O4������ѹǿƽ��������Ӧ�����ƶ�������A��ȷ���������ܸı�ƽ��״̬����������������ԭ�����͡�����ʳ��ˮ�������ӵ�Ũ�ȴ��������������ܽ⣬��ȷ��D�еĿ��淴Ӧ�Ƿ�Ӧǰ���������ģ����Ըı�ѹǿ��ƽ�ⲻ�ƶ�����������������ԭ�����͡�����AC��
�����Ѷȣ���