��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪��550��ʱ��һ���ݻ��������з�����Ӧ��2SO2+O2 ?2SO3(����Ӧ����)���жϸ÷�Ӧ�ﵽƽ��״̬�ı�־��
?2SO3(����Ӧ����)���жϸ÷�Ӧ�ﵽƽ��״̬�ı�־��
A��SO2��SO3Ũ�����
B��SO3������������SO2�������������
C�������������ѹǿ����
D�������л��������ܶȱ��ֲ���
2��ѡ���� ��ijһ�ݻ�Ϊ2 L���ܱ������ڣ�����2 mol��CO��2 mol��H2O�����¼��ȣ��������·�Ӧ��CO(g) +H2O(g)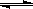 ?CO2(g) + H2(g)��1molCO��ȫ��Ӧ����a kJ����Ӧ�ﵽƽ����n(CO2)= 0.8mol����˵����ȷ����(? )
?CO2(g) + H2(g)��1molCO��ȫ��Ӧ����a kJ����Ӧ�ﵽƽ����n(CO2)= 0.8mol����˵����ȷ����(? )
A���жϸ÷�Ӧ�ﵽƽ���������CO��H2O��CO2��H2��Ũ�ȶ����
B����Ӧ�ų�������Ϊ0.4a kJ
C��ƽ��ʱH2O ��ת����Ϊ40%
D������������Է�Ӧ�ӿ죬���ȸ���
3������� ��1��80��ʱ����0.40 mol��N2O4�������2L�Ѿ���յĹ̶��ݻ����ܱ������У��������·�Ӧ��N2O4 (g) ? ?2NO2 (g)?��H��0����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
?2NO2 (g)?��H��0����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
?ʱ�䣨s��
n(mol)
| 0
| 20
| 40
| 60
| 80
| 110
|
n(N2O4)
| 0.40
| a
| 0.20
| c
| d
| e
|
n(NO2)
| 0.00
| 0.24
| b
| 0.52
| 0.60
| 0.60
|
���ϱ���c =___________��e =_____________
�ڼ���20s��40s����NO2��ʾ��ƽ����Ӧ����Ϊ??mol/(L��s)
�ۼ�����80��ʱ�÷�Ӧ��ƽ�ⳣ��K=?��
��2����(1)�з�Ӧ������110s�����¶Ⱥ�������䣬���������ټ���0.2mol N2O4����ʱ��ƽ�⳯_______�����ƶ���������ƽ���N2O4��ת����_______75%���>��<��=������
��3����(1)�з�Ӧ������110s�����¶Ⱥ�������䣬���������ټ���0.2mol N2O4��0.1mol NO2ʱ��v��________ v��(�>��<��=��)
4������� ���ݻ�Ϊ2.0 L���ܱ������г���0.60 mol X��1.60 mol Y��������Ӧ��aX(g)+3Y(g) 2Z(g) ����10 min��Ӧ�ﵽƽ��״̬��Y��Ũ��Ϊ0.2 mol/L��Z�����ʵ�������Ϊ�����㲢�ش�
2Z(g) ����10 min��Ӧ�ﵽƽ��״̬��Y��Ũ��Ϊ0.2 mol/L��Z�����ʵ�������Ϊ�����㲢�ش�
�� 10�����ڣ�Z��ƽ����Ӧ����Ϊ _______________
�� ����a ��ֵ��Ҫ���о�����̣�_____________
�� ��������X��ƽ��ת����_____________________���ٷ�����ʾ������һλС����
�� �������·�Ӧ2Z(g)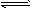 aX(g)+3Y(g)��ƽ�ⳣ��Ϊ___________
aX(g)+3Y(g)��ƽ�ⳣ��Ϊ___________
�� �������Ϊ 1�U3��X��Y�Ļ�����壬ͨ�������ܱ������У���һ���������·�����Ӧ���ﵽ��ѧƽ��ʱ�����������A ���������Ϊw %��w < 25���� ����������Z�����������________�������ڵ�ѹǿΪ��Ӧǰ��_________ ����
5��ѡ���� ��2L�����ܱ������з�����Ӧ��2A(g)+B(g)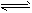 2C(g)������������A��B����4mol��10 s��Ӧ�ﵽƽ�⣬��ʱ���A��ƽ����Ӧ������0��12mol��L-1��s-1����ƽ���������B�����ʵ���Ũ��Ϊ
2C(g)������������A��B����4mol��10 s��Ӧ�ﵽƽ�⣬��ʱ���A��ƽ����Ӧ������0��12mol��L-1��s-1����ƽ���������B�����ʵ���Ũ��Ϊ
[? ]
A��2��8 mol��L-1
B��1��4 mol��L-1
C��3��2 mol��L-1
D��3��6 mol��L-1