微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某种一元强碱MOH溶液加入一种一元酸HA反应后,溶液呈中性,下列判断一定正确的是
A.加入的酸过量
B.生成的盐不水解
C.酸和碱等物质的量混合
D.反应后溶液中c(A-)=c(M+)
参考答案:D
本题解析:一元强碱MOH溶液加入一种一元酸HA反应后,溶液呈中性,则有c(OH-)=c(H+),如HA为强酸,则物质的量相等,如HA为弱酸,则碱应过量,以此进行分析。A、如HA为强酸,则物质的量相等,故A错误;B、如HA为强酸,,则生成强酸强碱盐,不会水解,故C错误;C、如HA为弱酸,则酸物质的量应过量,混合前酸与碱中溶质的物质的量不等,故B错误;D、溶液呈中性,则有c(OH-)=c(H+),根据溶液电中性原则可知c(A-)=c(M+),故D正确,故选D。
点评:本题考查酸碱混合的计算或判断,题目难度不大,明确碱的强弱是解答本题的关键,并注意电荷守恒的应用来解答。
本题难度:一般
2、填空题 某温度(t ℃)时,水的离子积为KW=1.0×10-13mol2・L-2,则该温度(填“大于”、“小于”或“等于”)________25 ℃,其理由是_______________________________________。
若将此温度下pH=11的苛性钠溶液a L与pH=1的稀硫酸b L混合(设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两种溶液的体积比:
(1)若所得混合液为中性,则a∶b=________;此溶液中各种离子的浓度由大到小排列顺序是___________________________________。
(2)若所得混合液的pH=2,则a∶b=________。此溶液中各种离子的浓度由大到小排列顺序是__________________________________________。
参考答案:大于 水的电离是吸热过程,KW随温度升高而增大 (1)10∶1 c(Na+)>c(SO)>c(H+)=c(OH-)或c(Na+)=2c(SO42―)>c(H+)=c(OH-) (2)9∶2
c(H+)>c(SO42―)>c(Na+)> 91ExAM.orgc(OH-)
本题解析:水的电离是吸热过程,KW随温度升高而增大,故温度高于25 ℃。
(1)稀H2SO4中,c(H+)=0.1 mol・L-1,NaOH溶液中c(OH-)=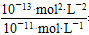 =0.01 mol・L-1
=0.01 mol・L-1
0.01 mol・L-1×a L=0.1 mol・L-1×b L
a∶b=10∶1
离子浓度关系c(Na+)>c(SO42―)>c(H+)=c(OH-)或c(Na+)=2c(SO42―)>c(H+)=c(OH-)
(2)若pH=2,则
c(H+)混=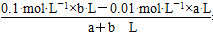 =0.01 mol・L-1
=0.01 mol・L-1
a∶b=9∶2
离子浓度关系:此时,假如原来NaOH溶液为9 L,H2SO4溶液则为2 L
n(Na+)=0.01 mol・L-1×9 L=0.09 mol
剩余n(H+)=0.01 mol・L-1×(9 L+2 L)=0.11 mol
n(SO42―)=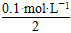 ×2 L=0.1 mol
×2 L=0.1 mol
所以:c(H+)>c(SO42―)>c(Na+)>c(OH-)。
本题难度:一般
3、选择题 实验室需配制一种仅含四种离子(不包括水电离出的离子)的无色混合溶液,且在混合溶液中四种离子的物质的量浓度均为1 mol/L。下面四个选项中能达到此目的的是(?)
A.Na+、K+、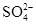 、Cl-
、Cl-
B.Cu2+、K+、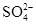 、
、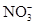
C.H+、K+、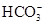 、Cl-
、Cl-
D.Mg2+、Na+、Cl-、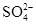
参考答案:D
本题解析:A项,若四种离子的浓度均为1 mol/L,溶液中正、负电荷的总数不相等;B项,含有Cu2+,溶液为蓝色;C项,H+和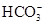 不能大量共存。
不能大量共存。
解答该题易出现的错误是容易忽视题中的部分信息,判断错误。如忽视“混合溶液中四种离子的物质的量浓度均为1 mol/L”,仅考虑离子之间相互不发生反应而错选A项,或忽视“无色溶液”的信息而错选B项。
本题难度:一般
4、选择题 下列各组离子能大量共存的是( )
A.Fe2+、K+、H+、NO3-
B.Na+、K+、AlO2-、CO32-
C.Na+、AlO2-、Cl-、HCO3-
D.Fe3+、Na+、AlO2-、NO3-