微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各物质的主要成分,皆为同一酸所对应的盐的是
A.大理石、重晶石、光卤石
B.小苏打、苏打、大苏打
C.绿矾、蓝矾、明矾
D.铝土矿、硫铁矿、磁铁矿
参考答案:C
本题解析:A项,大理石的主要成分是碳酸钙,重晶石的主要成分是硫酸钡,光卤石是镁和钾的氯化物,错误;B项,小苏打和苏打都是碳酸盐,大苏打的主要成分是硫代硫酸钠;C项,三者都是硫酸盐;铝土矿和磁铁矿都是金属氧化物,硫铁矿是铁的硫化物.
本题难度:简单
2、填空题 短周期元素X、Y、Z,它们的原子最外层电子数依次为1、6、6,Z位于Y的上一周期,则X、Y、Z三种元素形成的某种化合物的化学式可能为
A.XY2Z3
B.X2YZ4
C.X3YZ4
D.X3YZ3
参考答案:B
本题解析:略
本题难度:一般
3、选择题 短周期元素R、T、Q、W、K在元素周期表中的相对位置如下图所示,其中T所处的周期序数与族序数相等。下列判断正确的是
?
A.原子半径及其最高价氧化物对应水化物的酸性:Q<W<K
B.含元素T的盐溶液一定显酸性
C.最简单气态氢化物沸点和还原性:Q>R
D.最简单气态氢化物的热稳定性和水溶液酸性:K>W
参考答案:D
本题解析:根据元素在周期表中的相对位置可知,T是第三周期元素。又因为T所处的周期序数与族序数相等,所以T是铝元素,则Q是Si,R是N,W是S,K是Cl。A、同周期自左向右原子半径逐渐减小,最高价氧化物的水化物的酸性逐渐增强,A不正确;B、偏铝酸钠溶液显碱性,B不正确;C、氮元素的非金属性强于Si的,因此硅氢化物的还原性强于氮氢化物的还原性。由于氨气分子间存在氢键,所以氨气的沸点高于SiH4的沸点,C不正确;D、同周期自左向右非金属性逐渐增强,最高价氧化物的水化物的酸性逐渐增强,D正确,答案选D。
本题难度:一般
4、选择题 某元素原子核外电子排布为:第二层上的电子数比第一层与第三层电子数之和的两倍还多2,该元素是
A.Na
B.Mg
C.Al
D.Cl
参考答案:A
本题解析:根据核外电子排布规律可知,第二层只能容纳8个电子,而第一层只能容纳2个电子。如果第二层上的电子数比第一层与第三层电子数之和的两倍还多2,这说明最外层电子数 91ExAm.org一定是1个,所以是钠元素,答案选A。
点评:该题是高考中的常见题型,属于基础性试题的考查,侧重对学生基础知识的巩固和训练。该题的关键是明确核外电子的排布规律,并能结合题意灵活运用即可,有利于培养学生的逻辑推理能力。
本题难度:一般
5、填空题 (16分)下表是元素周期表的一部分, 针对表中的①~⑩种元素,
按要求填写下列空白:
?主族
周期
| ⅠA
| ⅡA
| ⅢA
| ⅣA
| ⅤA
| ⅥA
| ⅦA
| 0族
|
2
| ?
| ?
| ?
| ①
| ②
| ③
| ?
| ?
|
3
| ④
| ?
| ⑤
| ⑥
| ?
| ⑦
| ⑧
| ⑨
|
4
| ⑩
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?(1) 在这些元素中,化学性质最不活泼的元素是:?(填元素符号),其原子结构示意图为?。
(2) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是?,碱性最强的化合物的电子式是?。
(3) 最高价氧化物属两性氧化物的元素是?(填元素符号);写出它的最高价氧化物与氢氧化钠溶液反应的化学方程式:?。
(4) 用电子式表示元素④与⑦形成的化合物的形成过程:?,
该化合物属于?(填 “共价”或“离子”)化合物。
(5) 比较:氢化物稳定性②?③,最高价氧化物对应水化物的酸性②?⑥
(填“>”、“<”或“=”)。
(6) ⑥的最高价氧化物与烧碱溶液反应的离子方程式为?;
(7) 工业上制取元素⑥的单质的化学方程式为?
参考答案:(16分)(方程式和电子式形成每空2分,其余每空一分)
(1)Ar;?略? (2)HClO4;?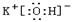 ;
;
(3)Al;? Al2O3+2NaOH= 2NaAlO2 + H2O;
(4)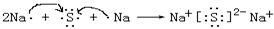 ;?离子
;?离子
(5)<?>
(6)SiO2+2OH-=SiO32-+H2O?(7)SiO2+2C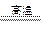 Si+2CO↑
Si+2CO↑
本题解析:略
本题难度:简单