微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有些商贩为了使银耳增白,就用硫磺(燃烧硫磺)对银耳进行熏制,用这种方法制取的洁白的银耳对人体是有害的。这些不法商贩制取银耳利用的是(?)
A.S的漂白性
B.S的氧化性
C.SO2的漂白性
D.SO2的还原性
参考答案:C
本题解析:略
本题难度:简单
2、选择题 下列反应生成的新化合物中,不稳定的是?(?)
A.SO3与水
B.SO2与水
C.SO2与氯水
D.SO3与NaOH溶液
参考答案:B
本题解析:A稳定,生成物为硫酸;B不稳定,生成物为亚硫酸,具有不稳定性易分解;C稳定,生成物为硫酸;D稳定,生成物为硫酸钠;
本题难度:简单
3、实验题 (16分)某研究小组想研究碳与浓硝酸的反应。其实验过程如下。
操作
| 现象
|
a.用干燥洁净的烧杯取约10 mL浓硝酸,加热。
| ?
|
b.把小块烧红的木炭迅速伸入热的浓硝酸中。
| 红热的木炭与热的浓硝酸接触发生剧烈反应,同时有大量红棕色气体产生,液面上木炭迅速燃烧,发出光亮。
|
(1)热的浓硝酸与红热的木炭接触会发生多个化学反应。
①碳与浓硝酸的反应,说明浓硝酸具有?性。
②反应产生的热量会使少量浓硝酸受热分解,写出反应的化学方程式?。
(2)实验现象中液面上木炭迅速燃烧,发出光亮。小组同学为了研究助燃气体是O2还是NO2,设计了以下实验。
Ⅰ.制取NO2气体。
①在虚线框内画出用铜与浓硝酸制取和收集NO2的装置简图(夹持仪器略)。

②NaOH溶液的作用是吸收多余的NO2,反应生成两种物质的量相等的正盐,写出这两种盐的化学式?。
Ⅱ.探究实验。
实验操作:在空气中引燃木炭,使其燃烧并带有火焰,将带火焰的木炭伸入盛有NO2气体的集气瓶中。
实验现象:木炭在NO2气体中持续燃烧,火焰迅速变亮,集气瓶中气体颜色变浅直至无色,产生的气体能使澄清石灰水变浑浊,且遇空气不变色。
①根据实验现象写出碳与NO2气体反应的化学方程式?。
②试分析:是否需要增加带火焰的木炭与纯净O2反应的实验?。
③通过实验探究,你认为助燃气体是什么,简述理由?。
参考答案:(1)① 强氧化性(1分)
②4HNO3(浓) 4NO2↑+O2↑+2H2O(3分)
4NO2↑+O2↑+2H2O(3分)
(2)Ⅰ①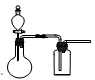 (3分)(两处导气管进出长短对各1分,漏斗对1分)
(3分)(两处导气管进出长短对各1分,漏斗对1分)
②NaNO2、NaNO3(2分)
Ⅱ①2NO2+2C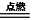 N2+2CO2(3分)②当木炭燃烧时,体系中氧气浓度低于空气中氧气浓度,所以不用补充木炭在纯氧中燃烧的实验。(2分)③助燃气体既有NO2又有O2,因为两种气体均存在且均能助燃。(2分)
N2+2CO2(3分)②当木炭燃烧时,体系中氧气浓度低于空气中氧气浓度,所以不用补充木炭在纯氧中燃烧的实验。(2分)③助燃气体既有NO2又有O2,因为两种气体均存在且均能助燃。(2分)
本题解析:(1)①碳与浓硝酸的反应,说明浓硝酸具有强氧化性。②反应产生的热量会使少量浓硝酸受热分解,反应的化学方程式4HNO3(浓) 4NO2↑+O2↑+2H2O。
4NO2↑+O2↑+2H2O。
(2)I.①铜与浓硝酸制取和收集NO2,可以在圆底烧瓶中进行,用分液漏斗滴加浓硝酸,同时用向上排气法收集NO2。
②NaOH溶液的作用是吸收多余的NO2,根据氧化还原反应的特征,生成正盐中N的化合价一种应该小于+4,一种大于+4,又N最高价位+5价,故应有NaNO3,因为,反应生成两种物质的量相等的正盐,所以另一种应为NaNO2。
II.①木炭在NO2气体中持续燃烧,火焰迅速变亮,集气瓶中气体颜色变浅直至无色,产生的气体能使澄清石灰水变浑浊,且遇空气不变色,说明生成了CO2,那么另一种应该为氮气,反应方程式为:2NO2+2C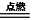 N2+2CO2。
N2+2CO2。
②当木炭燃烧时,体系中氧气浓度低于空气中氧气浓度,所以不用补充木炭在纯氧中燃烧的实验。
③通过实验探究可以知道:助燃气体既有NO2又有O2,因为两种气体均存在且均能助燃。
本题难度:一般
4、实验题 某课外活动小组的同学,在实验室研究用过量的锌与浓硫酸反应制取二氧化硫的有关问题。
(1)这样制取的二氧化硫气体中可能含有的杂质是?。
(2)某同学用下列装置连接成一整套实验装置以验证(1)的判断是否正确,若按气体从左到右流向时,气体流经的各装置导管的编号依次是?(用a、b……填写)。
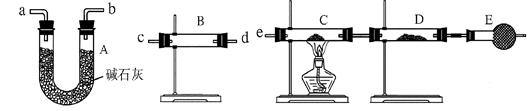
(3) 根据(2)确定的实验过程,请将实验时有关装置中所盛药品、实验现象、结论或解释填入下表:
装置
| 所盛药品
| 实验现象
| 结论或解释
|
B
| ?
| ?
| ?
|
C
| ?CuO固体
| ?
| ?
参考答案:(1) 氢气和水蒸气? (2)c d (或d c) a b (或b a) e
(3)
装置
所盛药品
实验现象
结论或解释
B
无水硫酸铜
固体由白色变成蓝色
SO2中含有水蒸气
C
?
固体由黑色变成红色
SO2中含有氢气
本题解析:(1)由于在反应过程中,浓硫酸的密度会逐渐减小,所以在反应后期会产生氢气。又因为气体从溶液中挥发出时一定会带有水蒸气,即SO2中含有的杂质是氢气和水蒸气。
(2)检验氢气可用其还原性,即利用氢气还原氧化铜;检验水蒸气一般用无水硫酸铜,且首先要检验水蒸气;又因为氢气在还原氧化铜时应该是干燥的,所以正确的答案是c d (或d c) a b (或b a) e
(3)见分析(2).
本题难度:一般
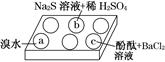
5、填空题 某化学小组进行Na2SO3的性质实验探究。
在白色点滴板的a、b、c三个凹槽中滴有Na2SO3溶液,再分别滴加下图所示的试剂:
实验现象如下表:
编号
| 实验现象
| a
| 溴水褪色
| b
| 产生淡黄色沉淀
| c
| 滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去
|
?
根据实验现象进行分析:
(1)a中实验现象证明Na2SO3具有________性。
(2)b中发生反应的离子方程式是_____________________________________________
(3)应用化学平衡原理解释c中现象(用化学用语及简单文字表述)__________________________________________________________。
参考答案:(1)还原性 (2)SO32-+2S2-+6H+=3S↓+3H2O
(3)在Na2SO3溶液中,SO32-水解显碱性:SO32-+H2O HSO3-+OH-,所以滴入酚酞后溶液变红;在该溶液中加入 BaCl2后,Ba2++SO32-=BaSO3↓(白色),由于c(SO32-)减小,SO32-水解平衡左移,c(OH-)减小,红色褪去。 HSO3-+OH-,所以滴入酚酞后溶液变红;在该溶液中加入 BaCl2后,Ba2++SO32-=BaSO3↓(白色),由于c(SO32-)减小,SO32-水解平衡左移,c(OH-)减小,红色褪去。
本题解析:(1)a中发生反应的化学方程式为:Na2SO3+Br2+H2O=Na2SO4+2HBr,证明Na2SO3具有还原性。
(2)b中产生淡黄色沉淀,发生反应的离子方程式是SO32-+2S2-+6H+=3S↓+3H2O。
(3)滴入酚酞溶液变红是因为SO32-发生了水解反应而使溶液显碱性:SO32-+H2O?HSO3-+OH-,再加入BaCl2溶液后,Ba2+与SO32-反应产生BaSO3沉淀,反应消耗了SO32-使其浓度减小,水解平衡向左移动,OH-浓度减小,红色褪去。
本题难度:一般
|