微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 两种大气污染物NO2和SO2在一定条件下可以发生如下反应:NO2+SO2=" NO" +SO3,在体积为V L的密闭容器中通入3molNO2和5molSO2, 反应后容器内氮原子和氧原子个数比为(? )
A.3/10
B.16/3
C.3/16
D.5/16
参考答案:C
本题解析:反应后容器内硫原子的物质的量n(N)=n(NO2)=3mol,氧原子的物质的量n(O)=2n(NO2)+2n(SO2)=2×3mol+2×5mol=16mol,原子个数之比等于物质的量之比,故反应后容器内硫原子和氧原子个数比为3:16,故选C。
本题难度:一般
2、选择题 木炭与浓硫酸反应可表示为:C +2H2SO4(浓)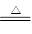 ?CO2↑+2SO2↑+2H2O。
?CO2↑+2SO2↑+2H2O。
(1)该反应的反应物和生成物中,属于氧化物的是?。
(2)木炭作?(填“氧化剂”或“还原剂”),硫酸?(填“被氧化”或“被还原”)。
(3)若消耗了2mol H2SO4,则生成?mol SO2。
参考答案:(1)CO2 、SO2、?H2O?(2)还原剂?被还原?(3)1
本题解析:氧化物是由氧和另一种元素组成的化合物,即氧化物的组成元素有两种,其中一种为氧元素。根据氧化物的定义可知该反应的反应物和生成物中,属于氧化物的是CO2 、SO2、H2O。(2)在反应中C的化合价由反应前单质中的0价变为反应后CO2中的+4价,化合价升高,失去电子,被氧化,作还原剂;H2SO4中的S的化合价一部分由反应前的+6价变为反应后SO2中的+4价,化合价降低,得到电子,被还原,作氧化剂,还有一部分未参加氧化还原反应,起酸的作用,提供酸根离子用来结合形成盐。每有2摩尔的浓H2SO4参加反应,产生1摩尔的SO2。
本题难度:一般
3、选择题 一定条件下硝酸铵受热分解的方程式为:5NH4NO3=2HNO3+4N2↑+9H2O,在反应中被氧化与被还原的氮原子数之比为
A.5∶3
B.5∶4
C.1∶1
D.3∶5
参考答案:A
本题解析:略
本题难度:一般
4、填空题 (10分)按要求完成下列各题。
(1)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为: 。
(2)ClO2常用子水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式: 。
(3)MnO2可与KOH和KClO3在高温条件下反应,生成K2MnO4,反应的化学方程式为: 。K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为 。
(4)(CN)2称为拟卤素,性质与卤素相似,其与氢氧化钠溶液反应的化学方程式为
。
参考答案:(每空2分)(1)PbO2+4HCl(浓) PbCl2+ Cl2↑+2 H2O
PbCl2+ Cl2↑+2 H2O
(2)2ClO2-+ Cl2= ClO2+2Cl-
(3)3MnO2+KClO3+6KOH 3K2MnO4+KCl+3 H2O 2:1
3K2MnO4+KCl+3 H2O 2:1
(4)2NaOH+(CN)2="NaCN+NaOCN+" H2O
本题解析:(1)黄绿色气体是氯气,说明氧化铅与浓盐酸反应生成氯气,化学方程式为PbO2+4HCl(浓) PbCl2+ Cl2↑+2 H2O
PbCl2+ Cl2↑+2 H2O
(2)Cl2氧化NaClO2溶液制取ClO2,则氯气被还原为氯离子,离子方程式为2ClO2-+ Cl2= ClO2+2Cl-
(3)根据氧化还原反应理论,MnO2可与KOH和KClO3在高温条件下反应,生成K2MnO4,同时氯酸钾被还原为氯化钾,反应的化学方程式3MnO2+KClO3+6KOH 3K2MnO4+KCl+3 H2O;K2MnO4中的Mn的化合价是+6价,KMnO4中Mn的化合价是+7价,而MnO2中Mn的化合价是+4价,根据得失电子守恒规律,KMnO4和MnO2的物质的量之比为2:1;
3K2MnO4+KCl+3 H2O;K2MnO4中的Mn的化合价是+6价,KMnO4中Mn的化合价是+7价,而MnO2中Mn的化合价是+4价,根据得失电子守恒规律,KMnO4和MnO2的物质的量之比为2:1;
(4)仿照氯气与氢氧化钠溶液反应的化学方程式,(CN)2与氢氧化钠溶液反应的化学方程式为2NaOH+(CN)2="NaCN+NaOCN+" H2O
考点:考查化学方程式的判断与书写
本题难度:一般
5、选择题 金属冶炼与处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是________。
a. Fe2O3? b.NaCl? c.Cu2S? d.Al2O3
(2)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2=4CuSO4+2H2O,该反应的还原剂是________。当1 mol O2发生反应时,还原剂所失电子的物质的量为________mol。向CuSO4溶液中加入镁条时有气体生成,该气体是________。
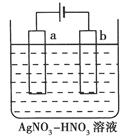
(3)右图为电解精炼银的示意图,________(填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体产生,则生成该气体的电极反应式为________。
(4)为处理银器表面的黑斑(Ag2S),将银器浸于铝质容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用是________。
参考答案:(1)b、d (2)Cu2S 4 H2 (3)a NO3―+2H++e-=NO2+H2O (4)做电解质溶液(或导电)
本题解析:结合氧化还原反应规律及原电池、电解池知识分析相关问题。
(1)电解法常用于冶炼非常活泼的金属,如K、Ca、Na、Mg、Al等,显然b、d项正确。工业上以Fe2O3、Cu2S为原料,采用热还原法冶炼金属Fe、Cu。
(2)该反应中,Cu元素由+1价变为+2价,S元素由-2价变为+6价,O元素由0价变为-2价,则O2为氧化剂,Cu2S为还原剂。1 mol O2发生反应时,得到4 mol电子,则还原剂Cu2S失去4 mol电子。CuSO4溶液中由于Cu2+发生水解而显酸性,加入镁条时,Mg与H+反应放出H2。
(3)电解精炼银时,用含杂质的粗银作阳极,用纯银作阴极,含Ag+的电解质溶液做电解液。图中b极与电源的负极相连,则b极为阴极,NO3―在阴极放电生成红棕色的NO2,电极反应式为NO3―+2H++e-=NO2+H2O。
(4)银器浸于铝质容器里的食盐水中并与铝接触,形成原电池,Al作负极被氧化成Al3+,银器表面的Ag2S作正极,被还原为金属Ag。食盐水为电解质溶液,起导电作用。
点拨:知识:金属的冶炼;氧化还原反应;电解精炼银;原电池原理的应用。能力:考查考生对教材基础知识的掌握及迁移应用能力、简单计算能力。试题难度:中等。
本题难度:一般