微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 密闭容器中的可逆反应3A(g)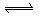 3 B+C? ΔH="+890" kJ/mol(A的式量为120)随着温度升高,容器中气体相对平均分子质量减小,则下列判断正确的是( ).
3 B+C? ΔH="+890" kJ/mol(A的式量为120)随着温度升高,容器中气体相对平均分子质量减小,则下列判断正确的是( ).
A.若C为固体,则B一定是气体
B.B和C一定都是气体
C.若起始时往容器中投入18 g A,则反应吸收的热量为44.5 kJ
D.若起始时往容器中投入18 g A,则反应放出的热量为44.5 kJ
参考答案:A
本题解析:略
本题难度:一般
2、选择题 将4 mol A 气体和2 mol B 气体在2 L的容器中混合并在一定条件下发生如下反应:
2A(g)+B(g)  ?2C(g)若经2 s 后测得C的浓度为0.6 mol/L,下列几种说法正确的是
?2C(g)若经2 s 后测得C的浓度为0.6 mol/L,下列几种说法正确的是
①用物质A表示的反应的平均速率为0.3 mol/(L・s)
②用物质B表示的反应的平均速率为0.6 mol/(L・s)
③反应达到平衡时,A、B、C的反应速率一定相等
④反应达到平衡时,A、B、C的物质的量均不再变化
A、①③? B、①④? C、②③? D、③④
参考答案:B
本题解析:考查可逆反应大有关计算,一般采用三段式,即
2A(g)+B(g)  ?2C(g)
?2C(g)
起始量(mol)? 4? 2? 0
转化量(mol)?1.2? 0.6? 1.2
平衡量(mol)? 2.8? 1.4? 1.2
所以用物质A表示的反应的平均速率为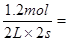 ? 0.3 mol/(L・s)
? 0.3 mol/(L・s)
用物质B表示的反应的平均速率为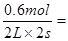 ? 0.6 mol/(L・s)
? 0.6 mol/(L・s)
平衡时正逆反应速率相等,各种物质大浓度不再发生变化。但各种物质的反应速率不一定相等,所以正确的答案是B。
本题难度:一般
3、计算题 在673K,1.01×105Pa时,有1mol气体A发生如下的反应:2A(气)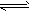 xB(气)+C(气)。在一定条件下已达到平衡。在平衡混合气体中,A占其体积百分比为58.84%。混合气体总质量为46g,密度为0.72g・L-1。求
xB(气)+C(气)。在一定条件下已达到平衡。在平衡混合气体中,A占其体积百分比为58.84%。混合气体总质量为46g,密度为0.72g・L-1。求
(1)平衡混合气体的平均分子量
(2)A的平衡转化率
(3)x值
(4)相同条件下,反应前A的密度是平衡混合气体密度的几倍。
参考答案:(1)39.73
(2)32%
(3)2
(4)1.16倍
本题解析:
本题难度:一般
4、选择题 在密闭容器中充入4mol SO2和 O2,在一定条件下建立平衡:2SO2(g) + O2(g) ? ?2SO3(g) △H,若SO2的转化率为90%,则在此条件下,反应放出的热量为(?)
A.3.6△H
B.1.8△H
C.2△H
D.0.9△H
参考答案:B
本题解析:由反应2SO2(g) + O2(g) ? ?2SO3(g) △H
起始物质的量? 4mol? 3mol? 0
变化物质的量? 3.6 mol? 1.8 mol? 3.6 mol
平衡物质的量? 0.43.6 mol? 1.2 mol? 3.6 mol
可逆反应方程式中的反应热为反应物完全转化为生成物时的反应热,在该反应中,每消耗2mol SO2放出的热量为△H,则反应3.6 mol SO2放出的热量为1.8△H;
本题难度:一般
5、填空题 已知 :N2(g)+3H2(g)  ?2NH3(g)?ΔH=-92 kJ・mol-1。
?2NH3(g)?ΔH=-92 kJ・mol-1。
(1) 在500℃、2.02×107Pa和铁催化条件下2L密闭容器中充入1molN2和3mol H2,10 min时达到平衡,有0.2 mol NH3生成,则10 min内用氢气表示的该反应的平均速率v(H2)为?,H2的转化率为__________。
(2)充分反应后,放出的热量______(填“<”“>”“=”)92.4kJ,理由是?
? ??。
??。
(3)为有效提高氢气的转化率,实际生产中宜采取的措施有____________
A.降低温度
B.不断补充氮气
C.恒容下充入He来增大压强
D.升高温度 E.原料气不断循环 F.及时移出氨
