��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ij���汻�����ĸ�����Ʒ���������ϡH2SO4�У����ˣ���ȥ���ʣ������еμ�KSCN��Һ��Ѫ��ɫ����������Һ�м�������������ټ�������İ�ˮ���г������ɣ������������м�������֮ǰ��Һ�е����ʺ��������ɵij�����ɫ�ֱ�Ϊ��������
A��Fe2��SO4��3����ɫ
B��Fe2��SO4��3�����ɫ
C��FeSO4�����ɫ
D��FeSO4��ɫ������ɫ�����ɫ
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2��ѡ���� 76.8mgͭ������Ũ���ᷴӦ��ͭȫ�����ú����NO3-���Ӽ���2��10-3mo l������Һ��H+����ͬʱ����?��?��
l������Һ��H+����ͬʱ����?��?��
A��4.8��10-3mol
B��4.4��10-3mol
C��3.2��10-3mol
D��2.2��10-3mol
�ο��𰸣�B
�����������
�����Ѷȣ���
3������� ��ҵ������������Ҫ�ɷ���Al2O3������������Fe2O3��SiO2����ȡұ������ԭ����������������������ͼ��
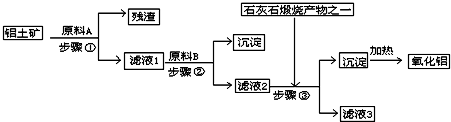
��1��ԭ��A��������______������ٷ�Ӧ�����ӷ���ʽ��______��
��2����Һ1��Ҫ�����Թ���ԭ��B��ԭ��B�Ļ�ѧʽ��______������ڷ�Ӧ�����ӷ���ʽ�ǣ�______��
��3������۵Ļ�ѧ����ʽ�ǣ�______��
��4�����ʡȥ����٣����ܽ��������ǴӼ���ԭ��B��ʼ�������������䣬��������������ȡ��ʲôӰ��______��
�ο��𰸣��ɹ������̿�֪�����ͨ���Ϊ������̼�����ɵij���Ϊ����������������Һ�ں���AlO2-�������Ӧ�����������ƣ�������Һ���к���Al3+�������ӦΪ�������ᣬ��ȥSiO2��
��1��������������֪������ټ������ᣬ��ȥSiO2������ԭ��AΪ���ᣬ
���������ᷴӦ���ӷ���ʽΪAl2O3+6H+=2Al3++3H2O�������������ᷴӦ���ӷ���ʽΪFe2O3+6H+=2Fe3++3H2O��
�ʴ�Ϊ��Al2O3+6H+=2Al3++3H2O��Fe2O3+6H+=2Fe3++3H2O��
��2������ټ���������ᣬ��Һ���к���Al3+��Fe3+��H+�ȣ�Ӧ�����������ƣ���ȥ�����ӣ���������ת��ΪAlO2-����ӦΪ?H++OH-=H2O��Fe3++3OH-=Fe��OH��3����Al3++4OH-=AlO2-+2H2O��
�ʴ�Ϊ��NaOH��?H++OH-=H2O��Fe3++3OH-=Fe��OH��3��Al3++4OH-=AlO2-+2H2O��
��3����Һ�ں���AlO2-�������ͨ�������̼����AlO2-��Ӧ���ɵij���Ϊ����������
��Ӧ��ѧ����ʽΪNaAlO2+CO2+2H2O=Al��OH��3��+NaHCO3��
�ʴ�Ϊ��NaAlO2+CO2+2H2O=Al��OH��3��+NaHCO3��
��4������NaOH��Һ�ܽ����������в���SiO2�ܽ���NaOH��Һ�����ɹ����ƣ�ͨ�������̼�����ɹ�����������ʹ�����Ƶõ�Al2O3����SiO2���ʣ�
�ʴ�Ϊ������NaOH��Һ�ܽ����������в���SiO2�ܽ���NaOH��Һ�����ɹ����ƣ����ʹ�����Ƶõ�Al2O3����SiO2���ʣ�
���������
�����Ѷȣ�һ��
4������� ij�о���ѧϰС���ò�����������������ΪFe2O3��Ϊԭ�ϣ������ұ���������¹������̣����ַ�Ӧ����û�б������
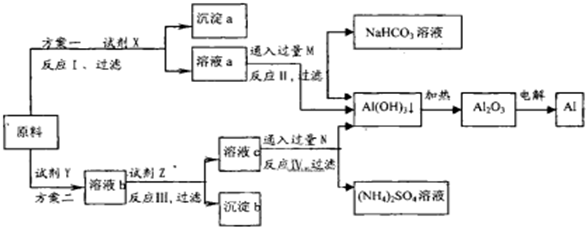
��1���Լ�X�Ļ�ѧʽΪ______����ӦI�����ӷ���ʽ��______��
ʵ��������480mL?1mol?L-1?X����Һ�����õ������������ձ������������Լ�ƿ����ͷ�ι��⣬����______�����������Ա궨����X����ҺŨ���Ƿ�ȷ��ʵ��������______��
��2�����շ�����ƣ��Լ�Z�������ǵ�����Һ��pH�������ɳ���b[Fe��OH��3]����ʵ�ʹ�ҵ�ĽǶȣ�����Ϊ����______��������������______
��3����֪NΪ������ʵ�����л���������ͼװ����ȡ���������а�����Ȫʵ�飮
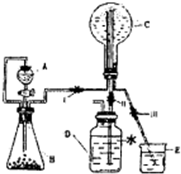
������A��������______��װ����A�ڲ���B�ڲ�֮����ͨ�����ܵ�������______
�����ô�װ���Ʊ�N������A��ʢ��Ũ��ˮ����Bװ���еĹ����Լ�������ѡ�����е�______������ĸ��ţ���
A����ʯ��?B���ռ�?C������?D����ʯ��
��4����D�����ȵ���������̪����C��Һ���______ɫ�������ӷ���ʽ����ԭ��______��
�ο��𰸣���1������һ������Һaͨ�������M������������������̼�����ƿ�֪����Һa�к���ƫ�����������MΪ������̼�����Լ�XΪNaOH��Һ����ӦIΪ������������������Һ��Ӧ����ƫ��������ˮ�����ӷ���ʽΪ��Al2O3+2OH-�T2AlO2-+H2O��
ʵ����û��480mL����ƿ��Ӧѡ��500mL����ƿ������500mL1mol?L-1?NaOH����Һ��Ҫ���������У��ձ������������Լ�ƿ����ͷ�ιܡ�500mL����ƿ����ȱ��500mL����ƿ��
���������к͵ζ������Ա궨����NaOH��ҺŨ���Ƿ�ȷ��
�ʴ�Ϊ��NaOH��Al2O3+2OH-�T2AlO2-+H2O��500mL����ƿ���к͵ζ���
��2��������������Һcͨ�������N����������������������刺�֪����Һc�к��������ӡ�NΪ���������Լ�YΪ���ᣬ��Һb�к�����������������������PHֵ����������ת��Ϊ�������������˺�������Һ�м�������İ�ˮ���������ӣ�
�뷽��һ��Ƚϣ�����һ�����٣��������ʷ���һ��������
�ʴ�Ϊ������һ�������٣�������
��3���١�����A�Ƿ�Һ©����װ����A�ڲ���B�ڲ�֮����ͨ�����ܵ������ǣ�ƽ���Һ©������ѹǿ����ֹ��Һ©��������
�ڡ�A��ʢ��Ũ��ˮ������ʯ�ҡ��ռ��ʯ�һ�ϣ��ų��������ȣ���Һ������������Ũ���������ð����ݳ������������İ�������ˮ�뵨����Ӧ����������ͭ���������ܲ�����������C���ܿ��ԣ�
�ʴ�Ϊ��C��
��4����������ˮ����Ӧ����һˮ�ϰ���һˮ�ϰ��������������NH3+H2O?NH3?H2O?NH4++OH-����Һ�ʼ��ԣ���̪�ڼ��������³ʺ�ɫ��
�ʴ�Ϊ���죻NH3+H2O?NH3?H2O?NH4++OH-��
���������
�����Ѷȣ�һ��
5������� Fe��OH��2�ܲ��ȶ���¶���ڿ��������ױ�������Fe��OH��2�������Ļ�ѧ����Ϊ��______��Ϊ�˻�ð�ɫ��Fe��OH��2�����������ò���Fe3+��FeSO4��Һ���ò���O2������ˮ���Ƶ�NaOH��Һ��Ӧ�Ʊ���
��1������������������������FeSO4��Һʱ����û������______����2����ȥ����ˮ���ܽ��O2������______�ķ�����
��3�����ɰ�ɫFe��OH��2�����IJ������ó��ι���ȡ����O2��NaOH��Һ������FeSO4��ҺҺ���£��ټ���NaOH��Һ������������������______��
��4������Fe3+���ڵ�����Լ���______��������______��
��5��д��Fe��H20��һ�������·�Ӧ�Ļ�ѧ����ʽ______��
�ο��𰸣�Fe��OH��2�������Ļ�ѧ����Ϊ4Fe��OH��2+O2+2H2O=4Fe��OH��3���ʴ�Ϊ��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
��1��FeSO4��Һ�����������ױ�����Ϊ���������ӣ��������ۿ��Է�ֹ���������ʴ�Ϊ�����ۣ�
��2�����������������Ʊ�Ҫ������������ȥ����ˮ���ܽ��O2�����ü��������ڵķ������ʴ�Ϊ�����ۣ����������ڣ�
��3�����ι���ȡ����O2��NaOH��Һ������FeSO4��ҺҺ���£��ټ���NaOH��Һ�����Է�ֹ��������NaOH��Һ�ļ��������Һ���ʴ�Ϊ�����Է�ֹ��������NaOH��Һ�ļ��������Һ��
��4����KSCN���������������ӣ�����Ϊ��Һ��ΪѪ��ɫ���ʴ�Ϊ��KSCN��Һ����Һ��ΪѪ��ɫ��
��5��Fe��H20��һ�������·�Ӧ�Ļ�ѧ����ʽ��3Fe+4H20��g��?����?.?Fe3O4+4H2���ʴ�Ϊ��3Fe+4H20��g��?����?.?Fe3O4+4H2��
���������
�����Ѷȣ�һ��