��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� X��Y��Z��M��Q�����ֶ���������Ԫ�أ�ԭ�������������� X��Y���γ�����ܼ���X��Y��Z��Ϧ�������֮��Ϊ8��Y��M�γɵ���̬�������ڱ�״���µ��ܶ�Ϊ2.86g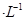 ����ش��������⣺
����ش��������⣺
��1��Y��Z��M����Ԫ��ԭ�Ӱ뾶��С�����˳��Ϊ��дԪ�ط��ţ�________________��
��2��Q�����ڱ��е�λ����____________��
��3��X��Y��Q����Ԫ�ء��γɵ���ԭ�ӷ��ӽṹʽΪ______________��M��QԪ���γɵ�����������Ӧ��ˮ�����н�ǿ�����ǣ�д��ѧʽ��_____________��
��4��Y��Z�γɵĻ�����A�Ⱥ����Ӽ��ֺ����ۼ�,A�ĵ���ʽΪ______________________��
��A����ʢ�з�̪��Һ���Թ��й۲쵽������Ϊ_________________________________��������Ӧ�Ļ�ѧ����ʽΪ_________________��
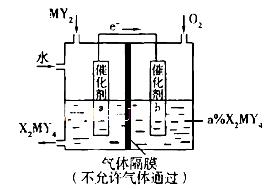
��5����������װ�ÿɽ�������MY2ת��Ϊ��Ҫ����ԭ��H2MY4���缫a�Ĵ������淢���ĵ缫��Ӧ����ʽΪ__________________________________��������ͨ��MY2��O2�����ʵ�����ѱ�ֵΪ________________��
�ο��𰸣���1��H,O,Cl,S,Na����2���������ڣ���VIIA�塣��3��H-O-Cl��HClO4����4��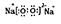 ����Һ��죬����ɫ��������Ӧ�Ļ�ѧ����ʽΪ2Na2O2 + 2H2O =" 4NaOH" + O2����5��SO2 + 2H2O -2e- = SO42- + 4H+��2��1��
����Һ��죬����ɫ��������Ӧ�Ļ�ѧ����ʽΪ2Na2O2 + 2H2O =" 4NaOH" + O2����5��SO2 + 2H2O -2e- = SO42- + 4H+��2��1��
���������X��Y��Z��M��Q�����ֶ���������Ԫ�أ�ԭ�������������� X��Y���γ�����ܼ���Ϊˮ���ӣ���֪X��Y�ֱ�Ϊ�����Ԫ�ء���������Ϧ�������֮��Ϊ8���Ƶ�ZΪ�ơ�Y��M�γɵ���̬�������ڱ�״���µ��ܶ�Ϊ2.86g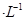 ������Է�������Ϊ64����֪MΪ��Ԫ�أ������Ƕ�����Ԫ�أ�QԪ�ص�ԭ��������M�Ĵ��Ƶ�QΪ�ȡ���1��Y��Z��M����Ԫ��ԭ�Ӱ뾶��С�����˳��Ϊ��дԪ�ط��ţ�H,O,Cl,S,Na����2��Q�����ڱ��е�λ���ǵ������ڣ���VIIA�塣��3��X��Y��Q����Ԫ�ء��γɵ���ԭ�ӷ����Ǵ����ᣬ�ṹʽΪH-O-Cl��M��QԪ���γɵ������������Cl2O7�����Ӧ��ˮ�����н�ǿ�����Ǹ����ᣬ��ѧʽΪHClO4����4��Y��Z�γɵĻ�����A�ǹ������ƣ��Ⱥ����Ӽ��ֺ����ۼ�,A�ĵ���ʽΪ
������Է�������Ϊ64����֪MΪ��Ԫ�أ������Ƕ�����Ԫ�أ�QԪ�ص�ԭ��������M�Ĵ��Ƶ�QΪ�ȡ���1��Y��Z��M����Ԫ��ԭ�Ӱ뾶��С�����˳��Ϊ��дԪ�ط��ţ�H,O,Cl,S,Na����2��Q�����ڱ��е�λ���ǵ������ڣ���VIIA�塣��3��X��Y��Q����Ԫ�ء��γɵ���ԭ�ӷ����Ǵ����ᣬ�ṹʽΪH-O-Cl��M��QԪ���γɵ������������Cl2O7�����Ӧ��ˮ�����н�ǿ�����Ǹ����ᣬ��ѧʽΪHClO4����4��Y��Z�γɵĻ�����A�ǹ������ƣ��Ⱥ����Ӽ��ֺ����ۼ�,A�ĵ���ʽΪ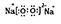 ������������ˮ��Ӧ�������������ƺ���Դ:91������ 91exam.org�������⣬����������Ư���ԣ��ʽ�A����ʢ�з�̪��Һ���Թ��й۲쵽������Ϊ��Һ��죬����ɫ��������Ӧ�Ļ�ѧ����ʽΪ2Na2O2 + 2H2O =" 4NaOH" + O2����5��������MY2�Ƕ�������ת��Ϊ��Ҫ����ԭ��H2MY4�����ᣬ��ͼ��֪�缫a����ʧ���ӣ��缫��Ӧ����ʽΪSO2 + 2H2O -2e- = SO42- + 4H+�����ݵ�ʧ�����غ㣬������ͨ��MY2��O2�����ʵ�����ѱ�ֵΪ2��1��
������������ˮ��Ӧ�������������ƺ���Դ:91������ 91exam.org�������⣬����������Ư���ԣ��ʽ�A����ʢ�з�̪��Һ���Թ��й۲쵽������Ϊ��Һ��죬����ɫ��������Ӧ�Ļ�ѧ����ʽΪ2Na2O2 + 2H2O =" 4NaOH" + O2����5��������MY2�Ƕ�������ת��Ϊ��Ҫ����ԭ��H2MY4�����ᣬ��ͼ��֪�缫a����ʧ���ӣ��缫��Ӧ����ʽΪSO2 + 2H2O -2e- = SO42- + 4H+�����ݵ�ʧ�����غ㣬������ͨ��MY2��O2�����ʵ�����ѱ�ֵΪ2��1��
�����Ѷȣ�һ��
2��ѡ���� �������е�A��B��C��D��E����Ԫ�أ�ԭ��������������A��D��C��E�ֱ�ͬ���壬AΪ�ǽ���Ԫ�أ���A��B��ԭ������֮�͵���C��ԭ��������C2����D���ĺ����������ȡ�������˵����ȷ����
A��B��Aֻ���γɻ�����BA3?
B��C��ԭ�Ӱ뾶�����Ӱ뾶���ֱ�С��D��ԭ�Ӱ뾶�����Ӱ뾶
C��A��B��C�γɵĻ�������ܴٽ�ˮ�ĵ��룬Ҳ��������ˮ�ĵ���?
D��A��D������C�γ�ԭ�Ӹ�����Ϊ1�U1��2�U1�Ļ������A2C2��D2C2�Ļ�ѧ��������ͬ
�ο��𰸣�C
�����������C��Eͬ���壬����C2������C��O��E��S��C2����D���ĺ����������ȣ�D��Na��A��Dͬ���壬AΪ�ǽ���Ԫ�أ�A��H��A��B��ԭ������֮�͵���C��ԭ��������B��N��A��B��A�γɻ�����NH3��N2H4�ȣ�B��Na��ԭ�Ӱ뾶����O��Na+���Ӱ뾶С��O2-�뾶��C��A��B��C�γɵĻ�����ΪHNO3��HNO2�ܴٽ�ˮ�ĵ��룬NH4NO3��NH4NO2������ˮ�ĵ��룻D��H2O2��ѧ�������Ǽ��Լ��ͷǼ��Լ���Na2O2�Ļ�ѧ�����������Ӽ��ͷǼ��Լ���
�����Ѷȣ�һ��
3��ѡ���� ���и���˳������в���ȷ����(? )
A��ԭ�Ӱ뾶��Na��Mg��Al��H
B�����ȶ��ԣ� HC l��H2S��PH3
C������ǿ����H2SiO3��H2CO3��H3PO4
D�������ԣ�K+��Na+��Mg2+��Al3+
�ο��𰸣�B
���������A��Na��Mg��Al�ǵ������ڵ�Ԫ�أ�Ԫ�ص�ԭ������Խ��ԭ�Ӱ뾶��ԽС����H�ǵ�һ���ڵ�Ԫ�ء�Ԫ�ص�ԭ�Ӻ�����Ӳ���Խ�࣬ԭ�Ӱ뾶��Խ������ԭ�Ӱ뾶��Na��Mg��Al��H����ȷ��B��Ԫ�صķǽ����ԣ�Cl��S��P.�|�ķǽ�����Խǿ�����⻯����ȶ��Ծ�Խǿ��������ȶ��ԣ� HC l��H2S��PH3������C��Ԫ�صķǽ����ԣ�P��C��Si��Ԫ�صķǽ�����Խǿ������۵ĺ���������Ծ�Խǿ����������ǿ����H2SiO3��H2CO3��H3PO4����ȷ��D��Ԫ�صĽ����ԣ�K��Na��Mg��Al.Ԫ�صĽ�����Խǿ������������ӵĽ������Խ������������Խ������������ԣ�K+��Na+��Mg2+��Al3+����ȷ��
�����Ѷȣ�һ��
4��ѡ���� ��3�֣���2012?ɽ�������й���ԭ�ӽṹ��Ԫ�����ʵ�˵����ȷ���ǣ�������
A���ǽ���Ԫ����ɵĻ�������ֻ�����ۼ�
B����A�����Ԫ����ͬ�����н�������ǿ��Ԫ��
C��ͬ��Ԫ�ص�ԭ�Ӿ�����ͬ����������������
D����A��Ԫ�ص������ӻ�ԭ��Խǿ��������������Ӧˮ���������Խǿ
�ο��𰸣�B
���������A���ǽ���Ԫ����ɵĻ�������������ӻ��������Σ�
B��ͬ����������ң������Լ�����
C��ͬ��Ԫ�صIJ�ͬ������������ͬ����������ͬ��
D�������ӻ�ԭ��Խǿ��Ԫ�صķǽ�����Խ��������������Ӧˮ���������Խ����
�⣺A����������ӻ�����������Ӽ����ɷǽ���Ԫ����ɣ���A����
B��ͬ����������ң������Լ������ʢ�A�����Ԫ����ͬ�����н�������ǿ��Ԫ�أ���B��ȷ��
C��ͬ��Ԫ�صIJ�ͬ������������ͬ����������ͬ����C����
D����A�������ӻ�ԭ��Խǿ��Ԫ�صķǽ�����Խ��������������Ӧˮ���������Խ������D����
��ѡB��
���������⿼��ṹ����λ�ù�ϵ���Ѷ��еȣ�ע��Ի���֪ʶ���������գ�
�����Ѷȣ�һ��
5��ѡ���� ���л����ķ��뷽������ȷ����
A.�Ӿƾ���ˮ�Ļ�����з�����ƾ���������
B.ʹ���ǵ�ʳ��ˮ����塪�����˷�
C.����ˮ������塪����Һ��
D.������غ��Ȼ��ش�ͬһ��Һ�з���������������ᾧ��
�ο��𰸣�C
���������A��ƾ���ˮ����Ϊ���ȵ�Һ̬�����ƾ��ķе��ˮ�ķе�ͣ�Ӧ�������Ѿƾ��Ӿƾ���ˮ�Ļ�����з��������
B��ʳ��ˮ���ǣ�˵��ʳ��ˮ����й������ʣ����˷����Գ�ȥ����Һ����Ĺ������ʣ�ʹҺ���ɻ��DZ���壮
C����ˮ�����ˮ�γɵľ��ȵ�Һ̬������Һ�����ܴ���ˮ�з�����壮Ҫ������ȡ��(�����Ȼ�̼���������͵�)�����ˮ����ȡ������Ȼ���ٽ��з�Һ��
D������غ��Ȼ��ض�������ˮ������ص��ܽ�����¶ȱ仯��Ӱ��ϴ��Ȼ��ص��ܽ�����¶ȱ仯��Ӱ���С����ˣ������������ᾧ��������غ��Ȼ��ش�ͬһ��Һ�з��������
�����Ѷȣ���