��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��15�֣�A��B��C��W��X��Y��Z�������ڱ��ж�����Ԫ����ɵ��������ʣ�����A��B��C�����ֹ��嵥�ʣ�W��X��Y��Z��������Ԫ����ɵĻ��������֮���ת����ϵ��ͼ��ʾ�����з�Ӧ����������δ�ڿ�ͼ�У�
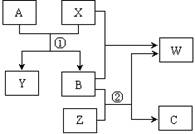
�ش��������⣺
��1��������Z�ľ�����������__________���塣
��2��д������C��һ����;__________________________________��
��3������Ƽ���֪������N�ǽ��Ǵ�����ijɷ�֮һ����ɻ�����N��Ԫ����W��ͬ����֪N������Ԫ�ص�����֮��Ϊ2:1��N�����ԭ������С��80����N�Ļ�ѧʽΪ_____________����֪�÷����е�ÿ��ԭ�Ӷ����������8���ӵ��ȶ��ṹ����д�������ʽ_________________��
��4��д�����з�Ӧ�Ļ�ѧ����ʽ��
��__________________________________��
��__________________________________��
�ο��𰸣���1��ԭ�ӣ�2�֣�
��2�������оƬ�����̫���ܵ�ء��뵼����ϵȣ���2�֣�
��3��C2O3��2�֣�?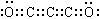 ?��3�֣�
?��3�֣�
��4��2Mg+CO2 2MgO+C��3�֣�? 2C+SiO2
2MgO+C��3�֣�? 2C+SiO2 2CO��+Si��3�֣�
2CO��+Si��3�֣�
�����������
�����Ѷȣ���
2������� ��ͼ�У�A��B��C��D��E�ǵ��ʣ�F��G��H��I��B��C��D��E�ֱ��A�γɵĻ������֪����G��H�Ļ�ѧʽΪ��X2Y3����ʽ��F�Ļ�ѧʽΪ��XY����ʽ����I��һ�ֳ��������壬��ʹ����ʯ��ˮ����ǣ���̬I�����˹����꣬ E������I��ȼ�գ������û���Ӧ����F�е�AԪ�ص���������Ϊ40%���ش����⣺


��1��I��E��Ӧ�Ļ�ѧ����ʽΪ��?����2�֣�
��2��C���������ᷴӦ������������������Һ��Ӧ��C��A�γɵĻ�����H������������Һ��Ӧ�����ӷ���ʽΪ��?����2�֣����H������ȡC, ��Ӧ�Ļ�ѧ����ʽΪ��?����2�֣�
��3��G��һ�ֺ���ɫ��ĩ����һ������G�м����������ᣬ��Ӧ�Ļ�ѧ����ʽΪ��?����2�֣���Ӧ�����Һ�м����������ۣ���Ӧ�����ӷ���ʽΪ��?����2�֣�
��4��G�����ᷴӦ�����ӷ���ʽΪ��?����2�֣��õ�����Һ�м���ͭ�ۣ���Ӧ�����ӷ���ʽΪ��?����2�֣�1.6g?G?�������ᣬ�õ�����Һ��ͭ����ȫ��Ӧ��������ͭ��?g��3�֣���
�ο��𰸣���1��2Mg+CO2 2MgO+C��2�֣���2��Al2O3��2OH����2AlO2����H2O��2�֣�
2MgO+C��2�֣���2��Al2O3��2OH����2AlO2����H2O��2�֣�
2Al2O3 4Al��3O2����2�֣�
4Al��3O2����2�֣�
��3��Fe2O3��3H2SO4��Fe2��SO4��3��3H2O��2�֣�2Fe3����Fe��3Fe2����2�֣�
��4��Fe2O3��6H����2Fe3����3H2O��2�֣�? Cu��2Fe3����Cu2+��2Fe2����2�֣�? 0.64g��1�֣�
���������I��һ�ֳ��������壬��ʹ����ʯ��ˮ����ǣ���̬I�����˹����꣬��˵��I�Ƕ�����̼��E������I��ȼ�գ������û���Ӧ2E+I��2F+D���ƶ�EΪ��������Mg�������ķ�ӦΪ��2Mg+CO2 2MgO+C��FΪMgO��DΪ����C��MgO�е���Ԫ�ص���������Ϊ40%��֤���ƶ���ȷ�����E��þ����A��������D��̼��F������þ��
2MgO+C��FΪMgO��DΪ����C��MgO�е���Ԫ�ص���������Ϊ40%��֤���ƶ���ȷ�����E��þ����A��������D��̼��F������þ��
��1��I��E��Ӧ�Ļ�ѧ����ʽΪ2Mg+CO2 2MgO+C��
2MgO+C��
��2��C���������ᷴӦ������������������Һ��Ӧ��˵��C�ǽ�������C��A�γɵĻ�����H������������������������������������Һ��Ӧ�����ӷ���ʽΪAl2O3��2OH����2AlO2����H2O�����������������ȡ��, ��Ӧ�Ļ�ѧ����ʽΪ2Al2O3 4Al��3O2����
4Al��3O2����
��3��G��һ�ֺ���ɫ��ĩ����G������������һ������G�м����������ᣬ��Ӧ�Ļ�ѧ����ʽΪFe2O3��3H2SO4��Fe2��SO4��3��3H2O���������������������������Ӧ�����Һ�м����������ۣ���Ӧ�����ӷ���ʽΪ2Fe3����Fe��3Fe2����
��4�������������ᷴӦ�����ӷ���ʽΪFe2O3��6H����2Fe3����3H2O������������������ͭ����˵õ�����Һ�м���ͭ�ۣ���Ӧ�����ӷ���ʽΪCu��2Fe3����Cu2+��2Fe2����1.6g?�����������ʵ�����1.6g��160g/mol��0.01mol�����ݷ���ʽFe2O3��6H����2Fe3����3H2O��Cu��2Fe3����Cu2+��2Fe2����֪?Fe2O3��Cu������Ҫͭ�����ʵ�����0.01mol��ͭ�۵�������0.64g��
�����Ѷȣ�һ��
3������� ��16�֣���ͼ����ѧ�������ʼ��ת����ϵ����֪��
a��AΪ����ɫ���壬BΪ���¡�����ЧӦ������Ҫ���ʣ�
b��EΪ����������JΪ���ɫ������
c��G��ʵ�����г����ڼ���B�Ĵ��ڣ�
d��L��һ����Ҫ�Ĺ�ҵԭ�ϣ�����������ըҩ��Ũ��Һ�����治�����ʻ�ɫ��
�ش��������⣺

��1��A�ĵ���ʽΪ?��B��������?���ӣ����ԡ��Ǽ��ԣ���
��2����Ӧ�ٵĻ�ѧ����ʽΪ?��
��Ӧ�ڵ����ӷ���ʽΪ?��
��3�����μӷ�Ӧ��A������Ϊ39g��������CO2�����������£�Ϊ?L��
��4������K�������ӳ��õķ�����?��
��5��LŨ��Һ�ı��淽����?��
�ο��𰸣�(16�֣�����ʽÿ��3�֣�����ÿ��2��)
��1���ԣ��Ǽ��Լ�
��2��2Na2O2+2CO2=2Na2CO3+O2��? Fe3++3OH��=Fe��OH��3��
��3��5��6L��
��4�����Թ���ȡ����K��Һ���μӼ���KSCN��Һ������Һ��ɫ��֤����Fe3+��
��5������ɫ�Լ�ƿ�ӱ��沢�����ڵ��±ܹ
�����������
�����Ѷȣ�һ��
4������� (14��)X��Y��Z��Q��R�����ֶ�����Ԫ�أ�ԭ��������������X��Y��Ԫ����������������֮�;�Ϊ0��Q��Xͬ���壻Z��R�ֱ��ǵؿ��к�����ߵķǽ���Ԫ�غͽ���Ԫ�ء���ش��������⣺
��1������Ԫ��ԭ�Ӱ뾶�ɴ�С��˳���ǣ�дԪ�ط��ţ�?
��2��X��Y���γɶ��ֻ�������мȺ����Լ��ֺ��Ǽ��Լ�������Է���������С�����ʣ�д����ʽ��?
��3��������ijЩԪ����ɵĻ�����A��B��C��D������ת����ϵ
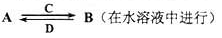
����C������ˮ�����Ե����壻D�ǵ���ɫ���塣
д��C�Ľṹʽ?��D�ĵ���ʽ??��
�����A��B��������Ԫ����ɣ�BΪ���Ի�����Ҳ�����ˮ������Aת��ΪB�����ӷ���ʽΪ?��
�����A������Ԫ����ɣ�B������Ԫ����ɣ�A��B��Һ���Լ��ԡ������ӷ���ʽ��ʾA��Һ�Լ��Ե�ԭ��?��
A��BŨ�Ⱦ�Ϊ0.1mol/L������Ļ����Һ�У�����Ũ���ɴ�С��˳��Ϊ?��
�ο��𰸣���1��Na��Al���ã��ϣ���?����2���ã��ȣ�?��3�� 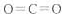
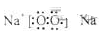
��AlO2-+2H2O+CO2=Al(OH)3��+HCO3-?��2 AlO2-+3 H2O+CO2="2" Al(OH) 3 ��+CO32-
��CO32-+H2O HCO3-+OH-,? c(Na+)�� c(HCO3-)�� c(CO32-)�� c(OH-) ��c(H+)
HCO3-+OH-,? c(Na+)�� c(HCO3-)�� c(CO32-)�� c(OH-) ��c(H+)
���������X��Y��Z��Q��R�����ֶ�����Ԫ�أ�ԭ��������������, Z��R�ֱ��ǵؿ��к�����ߵķǽ���Ԫ�غͽ���Ԫ�أ���ZΪ��Ԫ�ء�RΪAlԪ�أ�X��Y��Ԫ����������������֮�;�Ϊ0����Q��Xͬ���壬��Ϊ��������������֮��Ϊ0��Ԫ�ؿ���ΪH��C��Si������XΪ��Ԫ�أ�QΪNaԪ�أ�YΪ̼Ԫ�ء�
��1��ͬ�����������ԭ�Ӱ뾶��С�����Ӳ�Խ�࣬ԭ�Ӱ뾶Խ��ԭ�Ӱ뾶�ɴ�С��˳��Ϊ��Na��Al��C��O��H��
��2��H��C�γɶ��ֻ���������������ʣ����мȺ����Լ��ֺ��Ǽ��Լ�������Է���������С��C2H2��
��3��C������ˮ�����Ե����壬��CΪCO2��D�ǵ���ɫ���壬��DΪNa2O2����
CO2�ĽṹʽΪO=C=O��Na2O2�ĵ���ʽΪ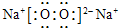 ��
��
�����A��B��������Ԫ����ɣ�BΪ���Բ�������ת����ϵ��֪��AΪƫ�����ơ�BΪ����������ƫ������������̼��ˮ��Ӧ��������������̼�����̼���������Ӧ���ӷ���ʽΪ��AlO2-+2H2O+CO2=Al(OH)3��+HCO3-?��2 AlO2-+3 H2O+CO2="2" Al(OH) 3 ��+CO32-
���A������Ԫ����ɣ�B������Ԫ����ɣ�A��B��Һ���Լ��ԣ����ת����ϵ��֪��AΪ̼���ơ�BΪ̼�����ƣ���Һ��̼���ˮ��CO32-+H2O HCO3-+OH-�� �ƻ�ˮ�ĵ���ƽ�⣬��Һ�ʼ��ԣ�̼���ơ�̼�����ƾ�Ϊ0.1mol?L-1�Ļ����Һ�У�������Ũ�����̼�����̼�����ˮ�⣬��Һ�ʼ��ԣ�̼�����ˮ��̶ȴ���̼�������������Ũ���ɴ�С��˳����c(Na+)�� c(HCO3-)�� c(CO32-)�� c(OH-) ��c(H+)��
HCO3-+OH-�� �ƻ�ˮ�ĵ���ƽ�⣬��Һ�ʼ��ԣ�̼���ơ�̼�����ƾ�Ϊ0.1mol?L-1�Ļ����Һ�У�������Ũ�����̼�����̼�����ˮ�⣬��Һ�ʼ��ԣ�̼�����ˮ��̶ȴ���̼�������������Ũ���ɴ�С��˳����c(Na+)�� c(HCO3-)�� c(CO32-)�� c(OH-) ��c(H+)��
�����Ѷȣ�����
5������� �����ֽ�������A��B��C������A����ɫ��ӦΪ��ɫ��B��C�dz������������ֽ�������A��B��C��������ס��ҡ���������D��E��F��G��H֮�䷢������ת����ϵ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ���������
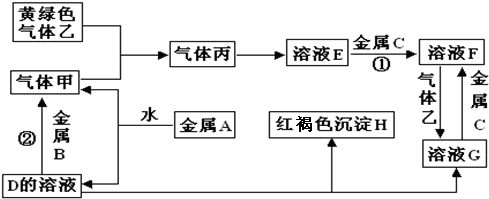
�����������Ϣ�ش��������⣺
��1��д���������ʵĻ�ѧʽ��
A______��H______��?G______����______��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ��Ӧ��______��Ӧ��______��
�ο��𰸣���1��A����ɫ��ӦΪ��ɫ������Aһ���ǽ����ƣ��ƺ�ˮ��Ӧ�����������������ƣ�����������D����Һ���������ƣ����岢���Ȼ��⣬����E�����ᣬ���ɫ�ij���Hһ�����������������Խ���C������F���Ȼ��������ܺ��������Ʒ�Ӧ���������Ľ���ֻ����������B������
�ʴ�Ϊ��Na��Fe��OH��3��FeCl3��Cl2��
��2����������ķ�ӦΪ��Fe+2HCl�TFeCl2+H2�������������ܺ�����Ӧ������ʽΪ��2NaOH+2Al+2H2O�T2NaAlO2+3H2����
�ʴ�Ϊ��Fe+2HCl�TFeCl2+H2����2NaOH+2Al+2H2O�T2NaAlO2+3H2����
���������
�����Ѷȣ�һ��