微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 现有常见金属单质A和气体甲、乙及物质B、C、D、E、F,它们之间能发生如下反应,已知B加入硫氰化钾溶液显血红色,气体乙显红棕色,(图中有些反应的产物和反应的条件没有全部标出).
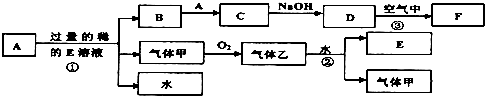
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A______,C______
(2)写出反应①的化学方程式______;
(3)写出反应②的化学方程式______;
(4)B物质的阳离子用于制作印刷电路板的原理是(用离子方程式表示)______
(5)缺铁性贫血患者应补充C物质的阳离子,而B物质的阳离子则无这种药效.当用C物质的阳离子制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是______如果药片已经失效,应如何检验?写出主要操作与现象:______.
参考答案:依据转化关系分析可知,已知B加入硫氰化钾溶液显血红色,证明含铁离子,气体乙显红棕色证明为NO2,气体甲为NO,E为HNO3,金属单质A为Fe;B为Fe(NO3)3,C为Fe(NO3)2,D为Fe(OH)2,F为Fe(OH)3;
(1)A、C的化学式分别为:Fe、Fe(NO3)2,故答案为:Fe;Fe(NO3)2;
(2)反应①是铁和稀硝酸反应生成硝酸铁、一氧化氮和水的反应,反应的化学方程式为:Fe+4HNO3=Fe(NO3)3+NO↑+2H2O,
故答案为:Fe+4HNO3=Fe(NO3)3+NO↑+2H2O;
(3)反应②是二氧化氮和水的反应,反应的化学方程式为:3NO2+H2O=2HNO3+NO,故答案为:3NO2+H2O=2HNO3+NO;
(4)B为Fe(NO3)2物质的阳离子为Fe3+用于制作印刷电路板的原理是铁离子和铜反应,反应的离子方程式为:2Fe3++Cu=2Fe2++Cu2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+;
(5)铁性贫血患者应补充C物质的阳离子,而B物质的阳离子则无这种药效.当用C物质的阳离子制成药片时外表包有一层特殊的糖衣,亚铁离子具有还原性,易被氧化,糖衣是为了避免亚铁离子被氧化;如果药片已经失效可以根据铁离子检验方法进行检验,FeSO4易被空气中的氧气氧化,被氧化生成Fe3+离子,可用KSCN溶液检验,实验操作为取少量研碎的药片放入试管中,加适量的水溶解,然后滴加数滴KSCN溶液,反应后溶液显红色,则表明该药片已部分或全部失效,
故答案为:保护FeSO4不被空气中的氧气氧化;取少量研碎的药片放入试管中,加适量的水溶解,然后滴加数滴KSCN溶液,反应后溶液显红色,则表明该药片已部分或全部失效.
本题解析:
本题难度:一般
2、填空题 (10分)短周期主族元素A、B、C、D的原子序数依次增大,A与D同主族,B与C在同一周期,B原子最外层电子数比C原子少2个, A、C单质在常温下均为气体,它们在一定条件下以体积比2∶1完全反应,生成物在常温下是液体。此液体与D单质在常温下能剧烈反应生成A的单质。所得溶液滴入酚酞显红色。回答下列问题:
⑴写出元素符号A?,B?,C?,D?。
⑵写出B与C两种单质完全反应后所得生成物的电子式?,该分子空间构型为?。
⑶ C、D两种单质在点燃条件下形成的化合物的电子式?,判断其中的化学键的类型?。
⑷写出两种由A、B、C、D四种元素组成的化合物的化学式?、?。
参考答案:

本题解析:略
本题难度:一般
3、填空题 (12分)中学化学中常见的几种物质存在如下关系,其中甲是黑色非金属单质,乙是生活中常见的金属单质,C在常温下为无色的液体,D是红棕色气体。(图中部分产物和反应条件已略去)
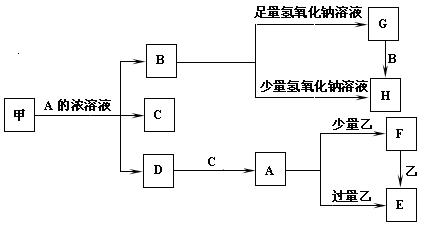 ?
?
回答下列问题:
(1)写出甲与A的浓溶液反应的化学方程式_________________________________。
(2)C的电子式是___________________________。
(3)除去G固体中含有H杂质采用的方法是_____________________。
(4)A溶液与一种能使湿润的红色石蕊试纸变蓝的气体反应,生成一种盐,该盐的溶液呈酸性,其原因是(用离子方程式表示)_____________________________。
(5)写出由F转化为E的离子方程式____________________________________;
(6)写出由G转化为H的离子方程式____________________________________。
参考答案:(12分)(1)C+4HNO3(浓)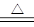 CO2↑+4NO2↑+2H2O (2分)
CO2↑+4NO2↑+2H2O (2分)
(2)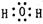 (2分)?(3)加热(2分)
(2分)?(3)加热(2分)
(4)NH + H2O
+ H2O NH3・H2O + H+ (2分)
NH3・H2O + H+ (2分)
(5)2Fe3+ +Fe 3Fe2+(2分)?
3Fe2+(2分)?
(6)CO32- +H2O +CO2=2HCO3-(2分)
本题解析:综合各物质的颜色状态及各物质的转化关系,可判定甲为碳、A为硝酸:
C+4HNO3(浓) CO2↑+4NO2↑+2H2O (2分)其中的D为NO2、C为H2O、B为CO2;
CO2↑+4NO2↑+2H2O (2分)其中的D为NO2、C为H2O、B为CO2;
硝酸和金属乙的产物与乙的乃是多少有关,可知乙为变价金属,可猜定为铁。
本题难度:一般
4、简答题 某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出),其中E为白色沉淀,I为红褐色沉淀.(此转化关系中所用的试剂都是足量的)
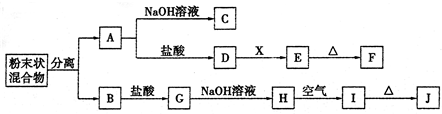
(1)写出下列物质的化学式:F______,G______.
(2)将混合物中两种金属分离开的最简单的方法是______.
(3)D→E的转化中,加入过量的X可能是______.
A.饱和NaCl溶液?B.NaOH溶液?C.氨水?D.Ba(OH)2溶液
(4)写出下列转化的化学方程式:
A→C:______;
H→I:______.
参考答案:(1)依据判断FG的化学式为:F为Al2O3,G为FeCl2,故答案为:Al2O3;FeCl2;
(2)混合物中两种金属分离开的最简单的方法是利用铁可以被磁铁吸引,方法为:用磁铁靠近粉末状混合物,将铁粉吸附在磁铁表面,
故答案为:用磁铁靠近粉末状混合物,将铁粉吸附在磁铁表面;
(3)D→E的转化中是X和氯化铝反应生成氢氧化铝的反应,依据实验室制取氢氧化铝的方法和氢氧化铝的性质分析,氢氧化铝能溶于过量强碱溶液中,所以加入过量的X可能是氨水,
故答案为:C;
(4)A→C是Al和氢氧化钠反应生成偏铝酸钠和氢气,反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑;H→I是氢氧化亚铁被氧化为氢氧化铁,该反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
本题解析:
本题难度:一般
5、推断题 A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质.B、E均为组成空气的成分.F的焰色反应呈黄色.?在G中,非金属元素与金属元素的原子个数比为1∶2.在一定条件下,各物质之间的相互转化关系如图所示(图中部分产物未列出)
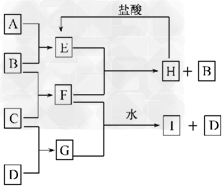
请填写下列空白:
(1)A是________,C是________.
(2)H与盐酸反应生成E的化学方程式是________________________________.
(3)E与F反应的化学方程式是________________.
(4)F与G的水溶液反应生成I和D的离子方程式是__________________________.
参考答案:(1)碳(或C);钠(或Na)
(2)Na2CO3+2HCl===2NaCl+H2O+CO2↑
(3)2CO2+2Na2O2===2Na2CO3+O2
(4)Na2O2+S2-+2H2O===4OH-+S↓+2Na+
本题解析:
本题难度:一般