��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���л�ѧ��Ӧ�У����ڻ��Ϸ�Ӧ����������������ԭ��Ӧ���ǣ�������
A��2CO+O2
2CO2
B��Na2O+H2O=2NaOH
C��2H2O2H2��+O2��
D��2H2O+2Na2O2=4NaOH+O2��
�ο��𰸣�A������������ԭ��Ӧ�����ǻ��Ϸ�Ӧ����A����
B�����ڻ��Ϸ�Ӧ����������������ԭ��Ӧ����B��ȷ��
C�����ڷֽⷴӦ������������ԭ��Ӧ����C����
D�������ڻ��Ϸ�Ӧ��������������ԭ��Ӧ����D����
��ѡB��
���������
�����Ѷȣ�һ��
2������� ��������ȫʡ��Χ���Ӵ����ϲ�ƺ�ݳ������ȣ�����˾���ƺ�ݳ����ɶ��������������м�������������õĻ�ѧ��Ӧ���£�
2CrO3?����ɫ��+3C2H5OH+3H2SO4=Cr2��SO4��3����ɫ��+3CH3CHO+6H2O������������ɷ���______��������Ӧ�л��ϼ۽��͵�Ԫ����______�����ϼ����ߵ�Ԫ����______��
����ɫ�Լ���˫��ˮ����Ϊ�ɿ�ҵ��Һ�����������Ҫ�����ɿ�ҵ��Һ�е��軯���KCN������ѧ��Ӧ����ʽΪ��KCN+H2O2+H2O=A+NH3����
��1��������A�Ļ�ѧʽΪ______��
��2����Ӧ�з���������Ӧ������Ϊ______��
��3��H2O2����Ϊ��ɫ��������������______��
��4���õ����ű�ʾ���÷�Ӧ����ת�Ƶķ������Ŀ______��?����2.5mol?NH3����ʱ����ת�Ƶ���______����
��ij��Һ�к���H+��Mg2+��Fe2+��S2-��I-��������֪��ԭ��S2-��I-��Fe2+��ֻ�������Ե���______��ֻ�л�ԭ�Ե���______���������������л�ԭ�Ե���______������Һ�м���þ�ۣ����õ��Ļ�ԭ������______������Һ��ͨ��Cl2�����ȵõ�������������______���ѧʽ����
�ο��𰸣���������֪���������������Ҵ����÷�Ӧ2CrO3?����ɫ��+3C2H5OH+3H2SO4=Cr2��SO4��3����ɫ��+3CH3CHO+6H2O�У�Ԫ�صĻ��ϼ۱仯���£�CrO3��Cr2��SO4��3��CrԪ����+6�ۡ�+3�ۣ��õ��ӻ��ϼ۽��ͣ�C2H5OH��CH3CHO��CԪ����-2�ۡ�-1�ۣ�ʧ���ӻ��ϼ����ߣ�
�ʴ�Ϊ��C2H5OH��Cr��C��
��1������ԭ���غ��������A�Ļ�ѧʽΪKHCO3 ���ʴ�Ϊ��KHCO3 ��
��2��KCN��KHCO3��CԪ����+2�ۡ�+4�ۣ�KCNʧ��������ԭ��������������Ӧ���ʴ�Ϊ��KCN��
��3��˫��ˮ������Ӧ������ˮ���Ի�������Ⱦ���ʴ�Ϊ����Ӧ��һ�㱻��ԭΪˮ������Ⱦ��
��4���÷�Ӧ��ת��2�����ӣ�
KCN+H2O2+H2O=KHCO3+NH3��? ת�Ƶ���
? 1mol? 2NA
? 2.5mol? 5 NA
�ʴ�Ϊ��
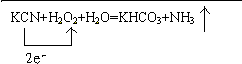
�� 5NA��
�����̬Ԫ��ֻ�������ԣ���ͼ�ֻ̬�л�ԭ�ԣ��м��̬�������������л�ԭ�ԣ�����ֻ�������Ե���H+��Mg2+��ֻ�л�ԭ�Ե���S2-��I-���������������л�ԭ�Ե���Fe2+��?����Һ�м���þ�ۣ�þ����ԭ����H+��Fe2+������������?H+��������������Fe2+���������������Ժ�õ��Ļ�ԭ������Fe������Һ��ͨ��Cl2��Cl2����������Fe2+��S2-��I-�л�ԭ�ԣ���ԭ��S2-��I-��Fe2+���������ȵõ�������������S��
�ʴ�Ϊ��H+��Mg2+��S2-��I-��Fe2+��Fe��S��
���������
�����Ѷȣ�һ��
3��ѡ���� �ڷ�Ӧ11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4�У�ͭԪ���ɷ�Ӧǰ��+2�۱�Ϊ��Ӧ���+1�ۣ����ֳ������ԣ���P�ڷ�Ӧ�б��ֳ���������
A��ֻ�л�ԭ��
B��ֻ��������
C����������������ԭ��
D���������������л�ԭ��
�ο��𰸣���11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4�У�CuSO4��Cu3P��ͭԪ����+2�۱�Ϊ+1�ۣ����ֳ������ԣ�
��P��Cu3P����Ԫ�صĻ��ϼ���0����Ϊ-3�������ֳ������ԣ�
P��H3PO4����Ԫ�صĻ��ϼ���0���ߵ�+5�ۣ����ֳ���ԭ�ԣ�
���ڸ÷�Ӧ��PԪ�صĻ��ϼۼ������ֽ��ͣ�P�������������л�ԭ�ԣ�
��ѡD��
���������
�����Ѷȣ���
4��ѡ���� ���������е����������뻯ѧ��Ӧ�йأ�����������������ԭ��Ӧ�ص��ǣ�������
A��ͭ�������ϳ���ͭ��[Cu2��OH��2CO3]
B���ֹ��Ʊ�������
C��FeCl3��Һ��ʴͭӡˢ��·��
D�����ú�Al��OH��3��θҩ����θ�����
�ο��𰸣�A��ͭ�������ϳ���ͭ�̣�CuԪ�صĻ��ϼ����ߣ�OԪ�صĻ��ϼ۽��ͣ�����������ԭ��Ӧ����A��ѡ��
B���ֹ��Ʊ������裬SiԪ�صĻ��ϼ۽��ͣ�����������ԭ��Ӧ����B��ѡ��
C��FeCl3��Һ��ʴͭӡˢ��·�壬FeԪ�صĻ��ϼ۽��ͣ�CuԪ�صĻ��ϼ����ߣ�����������ԭ��Ӧ����C��ѡ��
D�����ú�Al��OH��3��θҩ����θ����࣬Ϊ����кͷ�Ӧ����Ԫ�ػ��ϼ۱仯������������ԭ��Ӧ����Dѡ��
��ѡD��
���������
�����Ѷȣ�һ��
5��ѡ���� ���з�Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ1��2���ǣ�������
��O3+2KI+H2O�T2KOH+I2+O2����SiO2+2C
Si+2CO��?��SiO2+3CSiC+2CO������4HCl��Ũ��+MnO2MnCl2+Cl2��+2H2O��
A������
B�����Тڢ�
C���٢ڢۢ�
D�����Тڢۢ�
�ο��𰸣���O3+2KI+H2O�T2KOH+I2+O2��Ӧ��O3�е���Ԫ�ػ��ϼ۽��ͣ���Ԫ�صĻ��ϼ����ߣ���O3Ϊ��������KIΪ��ԭ���������ʵ���֮��Ϊ1��2��
��SiO2+2C?����?.?Si+2CO���й�Ԫ�صĻ��ϼ۽��ͣ�̼Ԫ�صĻ��ϼ����ߣ���SiO2Ϊ��������CΪ��ԭ���������ʵ���֮��Ϊ1��2��
��SiO2+3C?����?.?SiC+2CO����̼Ԫ�صĻ��ϼۼ������ֽ��ͣ�̼�������������ǻ�ԭ������1��̼ԭ�ӻ��ϼ۽��ͣ�2��̼ԭ�ӵĻ��ϼ����ߣ����������뻹ԭ�������ʵ���֮��Ϊ1��2��
��4HCl��Ũ��+MnO2?��?.?MnCl2+Cl2��+2H2O��MnԪ�صĻ��ϼ۽��ͣ���Ԫ�صĻ��ϼ����ߣ���MnO2Ϊ��������HClΪ��ԭ�����ɷ�Ӧ��֪��HCl��һ������ԭ�������������뻹ԭ�������ʵ���֮��Ϊ1��2��
��Ȼ�٢ڢܾۢ��������⣬��ѡC��
���������
�����Ѷȣ���