��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��ȸʯ��Ҫ��Cu2��OH��2CO3����������Fe��Si�Ļ����ʵ�����Կ�ȸʯΪԭ���Ʊ�CuSO4?5H2O��CaCO3���������£�
�Իش��������⣺
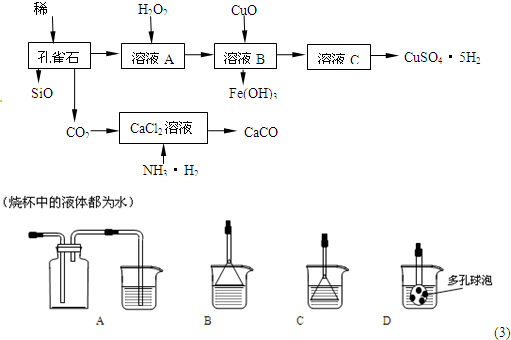
��1����δ����H2O2����ҺA�У����ڵĽ���������Cu2+��Fe2+��Fe3+�����������Һ��Fe3+��ѡ������ʵ��Լ���______������ţ���
A��KMnO4��Һ������B��Fe��?C��?Na2CO3��Һ?D��KSCN��Һ
����ҺA�м���H2O2��H2O2�ڸ÷�Ӧ������������ʵ����ѡ��H2O2������Cl2���������������ǻ��������⣬��һԭ���Dz���������______���ӣ�
��2������ҺC���CuSO4?5H2O����Ҫ��������Ũ����______�����˵Ȳ��������ձ���©���⣬���˲��������õ���һ�����������������ڴ˲����е���Ҫ������______��
��3���Ʊ�CaCO3ʱ��������Ӧ�Ļ�ѧ����ʽ��______����ʵ��������а����ݳ�����ѡ������װ���е�______������ţ�װ�����հ�����
��4�����ⶨ��ҺA��Fe2+��Ũ�ȣ�������100mL?0.1mol�MLKMnO4����Һ�����Ƹ���Һʱ�����ձ�������������ͷ�ι��⣬�����һ�ֲ���������______�������ò��������м�����ˮ���ӽ��̶���1-2cmʱ��Ӧ����______�μ�����ˮ����Һ�İ�Һ��������̶�����ƽ��
�ο��𰸣���1����������Һ��Fe3+��ʹ�õ��Լ���KSCN��Һ����Һ���Ѫ��ɫ����Fe3+��������Ӧ����
H2O2+2Fe2++2H+=2Fe3++2H20��Cl2+2Fe2+=2Fe3++2Cl-��H2O2��Fe2+��Ӧ���ɵ�H20Ϊ�ܼ���Cl2��Fe2+��Ӧ
���ɵ�Cl-���������ӣ��ʴ�Ϊ��D��Cl-��
��2������Һ��ȡ���壬�辭������Ũ������ȴ�ᾧ�ſɵõ����ڹ��˲����У����ձ�������������ͷ�ι��⣬�����һ�ֲ��������Dz������������������������ʴ�Ϊ����ȴ�ᾧ��������
��3��������̼���Ȼ��Ʋ���Ӧ��������������ˮ��ʹ��Һ�ʼ��ԣ������������������̼��Ӧ����̼��泥�̼��狀��Ȼ��Ʒ������ֽⷴӦ������̼��Ƴ�����������������ˮ���Ұ����д̼�����ζ����ֹ��Ⱦ������Ҫ��β������װ�ã�ѡ�õ��õ�©���ҽ���ˮ�棬Ŀ���Ƿ�ֹ�������ʴ�Ϊ��CO2+CaCl2+2NH3?H2O=CaCO3��+2NH4Cl+H2O��B��
��4��һ�����ʵ���Ũ����Һ�����ã����ձ�������������ͷ�ι��⣬�����һ�ֲ�������������ƿ������ƿ�Ĺ����100ml��250ml��500ml��1000ml��ѡȡ����ƿ�Ĺ��Ӧ���ڵ���������Һ������������ò��������м�����ˮ���ӽ��̶���1-2cmʱ��Ӧ���ý�ͷ�ιܵμ�����ˮ���ʴ�Ϊ��100mL����ƿ�� ��ͷ�ιܣ�
���������
�����Ѷȣ�һ��
2������� �Ķ��������Ϣ���ƶ�Ԫ�ؼ��й����ʣ���Ҫ��ش����ʣ�
��Ϣ�٣�X��Y��Z��W�dz����Ķ�����Ԫ�أ���ԭ����������������ԭ�Ӻ���������������������2��
��1��������Ϣ�٣�Xһ������______������ţ���
A��?B��̼?C����?D����
��Ϣ�ڣ���������Ԫ�صĵ��ʾ�����������������ȼ�գ����ɵ������������У�������������ϡ���ᣬ����������Ũ����������Һ�����������Է�������������26��
��2��������Ԫ�����Ƿ������һ������Ԫ�أ�______������ܻ��ܣ���
��Ϣ�ۣ�����������Ԫ�ص�����ɵĻ�����м�������������Һ�����岿���ܽ⣬���ˣ�����Һ�м���������ռ���Һ��������Һ��������ɫ������
��3����ɫ������Ļ�ѧʽΪ______��
��Ϣ�ܣ�����������Ԫ�ص�����ɵĻ�����м��������ռ���Һ�����岿���ܽ⣬���ˣ�����Һ�м��������������Һ��������Һ��������ɫ������
��4�����ɰ�ɫ����������ӷ���ʽΪ______��
��Ϣ�ݣ�X��Wͬ����
��5��X��Ũ�������ʱ��Ӧ�Ļ�ѧ����ʽΪ______��
�ο��𰸣���1��X��Ϊ��ʱ��������������Ϊ1����������X��Ϊ��ԭ��������X���Y��Z��W�����ܶ��Ƕ�����Ԫ�أ���������XΪ̼����ʱ�������ʴ�Ϊ��AD��
��2��Al���Т���Ԫ�ص����ʣ�����Ԫ�ؿ�����1������Ԫ�أ��ʴ�Ϊ�����ܣ�
��3�������ж�����Ԫ�ؽ�����̽��Ψ��þԪ�ط��Ϣ������ʣ���֪��ɫ������Ļ�ѧʽΪMg��OH��2���ʴ�Ϊ��Mg��OH��2��
��4��Ψ�й�Ԫ���ڢܱ仯�����յõ���ɫ����H2SiO3����H4SiO4�������ɸð�ɫ���������ӷ���ʽΪSiO32-+2H+=H2SiO3������SiO32-+2H++H2O=H4SiO4������
�ʴ�Ϊ��SiO32-+2H+=H2SiO3������SiO32-+2H++H2O=H4SiO4������
��5����֪X��Y��Z��W����Ԫ���е�3��ΪMg��Al��Si��ֻ��XΪ̼ʱ�ŷ���X��Wͬ������Xԭ��������С��������X��ŨH2SO4��Ӧ�Ļ�ѧ����ʽΪC+2H2SO4��Ũ��?��?.??CO2��+2SO2��+2H2O��
�ʴ�Ϊ��C+2H2SO4��Ũ��?��?.??CO2��+2SO2��+2H2O��
���������
�����Ѷȣ�һ��
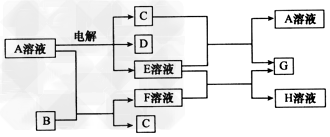
3���ƶ��� ��֪AΪ��ѧ��ѧ�е�һ���Σ�B��CΪ�ճ������г����Ľ�����ͨ�������£�DΪ��ɫ��ζ���壬��ɫ����G�����������ɫ����֪�ö��Ե缫���A��Һһ��ʱ�����ֻ��C��D��E��ϡ��Һ��������֮���ת����ϵ��ͼ�����ַ�Ӧ��������ȥ����
��ش��������⣺
��1��A�Ļ�ѧʽΪ________��
��2��A��Һ��Na2O2��Ӧ���ܻ�ѧ����ʽΪ____________
��3��E��ϡ��Һ��F��Һ��Ӧ�����ӷ���ʽΪ________________
��4�����100mL��A����Һһ��ʱ��Ͽ���·��ȡ���缫��������õ�������D�ڱ�״���µ����Ϊ5.6mL���������Һ��pHΪ__________����������Һ������䣩
��5������100mL��A����Һ�м���10g��������B�ķ�ĩ����ֽ�����ˣ���ɵ�10.16g���壬����Һ�����ʵ����ʵ���Ũ��Ϊ___________����������Һ������䣩
�ο��𰸣���1��Cu(NO3)2
��2��2Cu(NO3)2+2Na2O2+2H2O=2Cu(OH)2��+4NaNO3+O2��
��3��3Fe2++4H++NO3-=3Fe3++NO��+2H2O
��4�����ԡ�
��5��0.2mol/L
���������
�����Ѷȣ�һ��
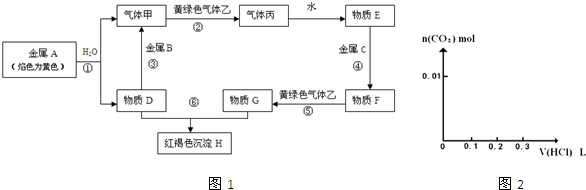
4������� ���н�������A��B��C������ס��ҡ����Լ�����D��E��F��G��H������֮����ת����ϵ��ͼ1��ʾ��ͼ����Щ��Ӧ��������ͷ�Ӧ������û�б������
��ش��������⣺
��1��д���������ʵĻ�ѧʽ��B______����______����______��
��2��д�����з�Ӧ�����ӷ���ʽ��
��Ӧ��______��
��Ӧ��______��
��Ӧ��______��
��3����0.4gD��1.06gNa2CO3��ϲ������Һ������Һ�еμ�0.1mol?L-1ϡ���ᣮ����ͼ2��ʾ������ϵ�л�������ȷ��ʾ������������������CO2�����ʵ����Ĺ�ϵͼ��______��
�ο��𰸣�����A��ɫ��ӦΪ��ɫ֤��ΪNa����ˮ��Ӧ���������ΪH2��DΪNaOH������B������������Һ��Ӧ��˵��BΪAl�������������Ӧ���ɱ�ΪHCl������EΪ������Һ������D�������ƺ�����GΪ��Ӧ���ɺ��ɫ����HΪFe��OH��3��GΪFeCl3���ƶ�����FΪFeCl2��CΪFe��
��1��������������֪��BΪAl����ΪHCl����ΪCl2���ʴ�Ϊ��Al��HCl��Cl2��
��2����Ӧ��Ϊ2Na+2H2O=2Na++2OH-+H2������Ӧ��ΪCl2+2Fe2+=2Fe3++2Cl-����Ӧ��ΪFe3++3OH-=Fe��OH��3����
�ʴ�Ϊ��2Na+2H2O=2Na++2OH-+H2����Cl2+2Fe2+=2Fe3++2Cl-��Fe3++3OH-=Fe��OH��3����
��3��0.4gNaOH��1.06gNa2CO3��ϲ������Һ������Һ�еμ�0.1mol?L-1ϡ���ᣬ�ȷ���NaOH+HCl=NaCl+H2O������0.1L���ᣬȻ����Na2CO3+HCl=NaCl+NaHCO3������0.1L���ᣬ�Ҳ����ɶ�����̼�������NaHCO3+HCl=NaCl+H2O+CO2��������0.1L��������0.01mol������̼����ͼ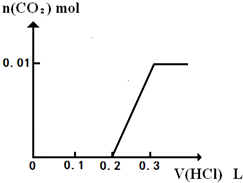 ��
��
�ʴ�Ϊ�� ��
��
���������
�����Ѷȣ�һ��
5������� ��ҵ���ÿ���M������X��Y��Z����Ԫ�أ��ڿ����и������գ�X��Y��Z�ֱ�ת����A��B��C���ֲ��A��B��C�����ʵ���֮��Ϊ1��1��2������AΪ���ʣ�9.6g?A����ϡ����������״����2.24L����G��G�������ʺ���ɫ��������Һ�еμ�Ũ��ˮ���������Ȳ���������������ܽ⣻B��YԪ������Ԫ�ص�������Ϊ7��2��B����������ϡ����õ���ҺW����ɫ����G��W��Һ�е������軯����Һ��Ѫ��ɫ��?CΪ����������ҳ����³���̬����Cͨ���Ȼ�����Һ�У������Ա仯�����ٵμ�˫��ˮ������ɫ������
��1��ָ��ZԪ�������ڱ��е�λ��______��Z�봦��ͬһ������ԭ�Ӱ뾶����Ԫ�أ���ϡ�����壩���γɵ��ȶ����������ʽΪ______��
��2��д��C��˫��ˮ���Ȼ�����Һ�������������ӷ�Ӧ����ʽ______��
��3������Ӿ����ͨ����X��������������ɱ������˵��������������ɱ�����õı���ԭ����______�����ƶ�M�Ļ�ѧʽΪ______��
��4����X�ĵ�������N2O4������������Һ�п��Ƶ�Y����ˮ�����Σ�ͬʱ����G����д�����Ϸ�Ӧ�Ļ�ѧ����ʽ______��
�ο��𰸣���ҵ���ÿ���M������X��Y��Z����Ԫ�أ��ڿ����и������գ�X��Y��Z�ֱ�ת����A��B��C���ֲ��A��B��C�����ʵ���֮��Ϊ1��1��2������AΪ���ʣ�9.6g A����ϡ����������״����2.24L����G��G�������ʺ���ɫ���ж�GΪNO��������Һ�еμ�Ũ��ˮ���������Ȳ���������������ܽ⣬�ƶ�AΪCu��B����������ϡ����õ���ҺW����ɫ����G��W��Һ�е������軯����Һ��Ѫ��ɫ��֤��M�к������������ӣ�B��YԪ��Ϊ��Ԫ������Ԫ�ص�������Ϊ7��2������õ�BΪ��������FeO��WΪFe��NO3��3�� CΪ����������ҳ����³���̬����Cͨ���Ȼ�����Һ�У������Ա仯�����ٵμ�˫��ˮ������ɫ�����������ж�����C�Ƕ�������������������Ϊ������Ȼ�����Ӧ���ɳ���������M��������Ӧ����ABC��A��B��C�����ʵ���֮��Ϊ1��1��2������ԭ���غ�͵����غ㣬�ƶϳ�MΪCuFeS2��XΪͭԪ�أ�YΪ��Ԫ�أ�ZΪ��Ԫ�أ�
��1��ZԪ������Ԫ�أ������ڱ��е�λ��Ϊ����3���ڣ���A�壻Z�봦��ͬһ������ԭ�Ӱ뾶����Ԫ��ΪNaԪ�أ����γɵ��ȶ�������Ϊ���ƣ�����ʽΪ
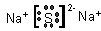
��
�ʴ�Ϊ����3���ڣ���A�壻
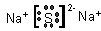
��
��2��CΪSO2����˫��ˮ���Ȼ�����Һ��������Ϊ���ᱵ�����ԭ���غ�͵����غ�д����Ӧ�����ӷ�Ӧ����ʽ��H2O2+SO2+Ba2+=BaSO4��+2H+��
�ʴ�Ϊ��H2O2+SO2+Ba2+=BaSO4��+2H+��
��3������Ӿ����ͨ����XΪͭԪ�أ�ͭ��������������ɱ������˵��������������ɱ�����õı���ԭ���ǣ�Cu2+ʹ�����ʱ��ԣ�����M��������Ӧ����ABC��A��B��C�����ʵ���֮��Ϊ1��1��2������ԭ���غ�͵����غ㣬2CuFeS2+5O2=2Cu+2FeO+4SO2�����ƶϳ�M�Ļ�ѧʽΪΪ��CuFeS2��
�ʴ�Ϊ��Cu2+ʹ�����ʱ��ԣ�CuFeS2��
��4����X�ĵ���ΪCu������N2O4������������Һ�п��Ƶ�A��Cu��NO3��2������ˮ�����Σ�ͬʱ����G��NO������Ӧ�Ļ�ѧ����ʽΪ��Cu+2N2O4=Cu��NO3��2+2NO����
�ʴ�Ϊ��Cu+2N2O4=Cu��NO3��2+2NO����
���������
�����Ѷȣ�һ��