微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 下图中所有物质均为中学化学常见物质,F、H是气体单质,Z是固体金属单质,Y中阳离子与阴离子个数比为2:1 ,化合物X、Y、A、D、E、G的焰色反应为黄色,I是白色沉淀。
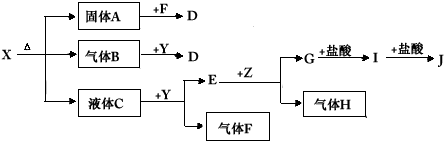
(1)写出X、E、I的化学式。X___________E____________I_____________。
(2)写出Y的电子式___________________。
(3)关于Y的说法正确的是_____________。
A.Y是氧化物
B.Y是过氧化物
C.Y是含有非极性键的离子化合物
D.Y是碱性氧化物
(4)写出B和Y反应的化学方程式:_____________________________。
(5)X和G的溶液能反应吗?如能反应,写出反应的离子方程式;如不能反应,请说明理由:
____________________________________
参考答案:(1)X:NaHSO3;E:NaOH;I:Al(OH)3
(2)
(3)ABC
(4)Na2O2+SO2==Na2SO4
(5)HSO3-+AlO2-+H2O==SO42-+Al(OH)3↓
本题解析:
本题难度:困难
2、推断题 A是一种无色透明的晶体,进行如下实验
①取少量A晶体做焰色反应实验,透过蓝色钴玻璃观察,火焰呈紫色。
②取少量A晶体溶于水可以得到无色的溶液,该溶液使石蕊变红。
③取少量A的溶液加过量氨水,有白色沉淀B生成。
④过滤除去③中的B后,在滤液中滴加氯化钡溶液,有白色沉淀C生成,C不溶于稀硝酸。
⑤取少量B滴加氢氧化钠溶液,得无色溶液D。
⑥取少量B滴加盐酸,得无色溶液E。
⑦将47.4gA晶体在120℃下加热脱水,剩余物的质量为25.8g。
根据上述实验现象和结果确定A、B、C、D、E,写出它们的化学式。
A ________ B ________ C ________ D ________ E _________
参考答案:A:KAl(SO4)2・12H2O;B:Al(OH)3;C:BaSO4;D:NaAlO2;E:AlCl3
本题解析:
本题难度:一般
3、填空题 (12分)A―J是中学化学中常见的几种物质,它们之间的转化关系如图所示。已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F合成,J可用作杀菌消毒剂。回答下列问题:
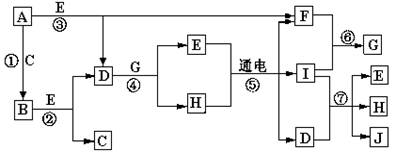
(1)B中的化学键有?,(填“离子键”、“极性键”或“非极性键”) E的电子式?。
(2)写出反应⑦的离子方程式__________________________
(3)向AlCl3溶液中加入少量固体B,写出反应的化学方程式_____________________
(4)以Pt为电极电解滴加有少量酚酞的H饱和溶液,则在_____________(填“阴或阳”)
极附近溶液由无色变为红色,其原因是?
参考答案:
(1)离子键、非极性键?(2分)?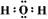 (2分)
(2分)
(2)Cl2+2OH-=Cl-+ClO-+H2O(2分)
(3)4AlCl3+6Na2O2+6H2O=4Al(OH)3↓+12NaCl+3O2↑ (3分)
(4)阴极(2分),在阴极由于H+得到电子产生H2,破坏了水的电离平衡,促进水继续电离,导致溶液中c(OH-)>c(H+),溶液呈碱性,所以阴极附近溶液变为红色(3分)
本题解析:考查钠及其化合物的转化
固体单质A、气体单质C可化合生成淡黄色粉末B,则可肯定A为Na、B为Na2O2、C为O2;E在常温下为液体,即水;钠、Na2O2分别与水反应:2Na+2H2O=2NaOH+H2↑? 2Na2O2+2H2O=4NaOH+O2↑,即D为NaOH,F为H2;
H与E(水)在“通电”的条件下电解生成三个物质:水、NaOH及气体单质I,可知H为NaCl,G为盐酸,I为氯气;
(1)Na2O2为离子化合物,一定含有离子键,过氧酸根离子中是O―O非极性键
水的电子式为: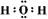 (2分)
(2分)
(2)氯气在碱性溶液中发生自身氧化还原反应:Cl2+2OH-=Cl-+ClO-+H2O(2分)
(3)2Na2O2+2H2O=4NaOH+O2↑产生少量的NaOH,AlCl3再与NaOH反应生成Al(OH)3沉淀:4AlCl3+6Na2O2+6H2O=4Al(OH)3↓+12NaCl+3O2↑
(4)阴极2H++2e―=H2↑,破坏了水的电离平衡:H2O H++OH-,促进水继续电离,导致溶液中c(OH-)>c(H+),溶液呈碱性,所以阴极附近溶液变为红色
H++OH-,促进水继续电离,导致溶液中c(OH-)>c(H+),溶液呈碱性,所以阴极附近溶液变为红色
本题难度:简单
4、填空题 (10分)已知:①A、B、C、D四种物质均含有元素X,有的还有可能含有元素Y、Z。且元素Y、X、Z的原子序数依次递增。②X在A、B、C、D四种物质中都不呈现其最高化合价。③室温下单质A与某种常见一元强碱溶液反应,可得到B和C。④化合物D受热分解,可制得元素Y的单质。试根据以上叙述回答:
(1)写出A、B、C、D的化学式::A_______B_______C_______D______。
(2)写出③、④中的两个化学方程式:
③,?④ ?。
参考答案:Cl2? KCl? KClO? KClO3
本题解析:由题意可知,X元素具有多种价态(至少4种),可得X元素一定为非金属元素,在非金属元素单质中能与某种常见一元强碱溶液反应的物质为CL2,即X元素为CL元素。化合物D受热分解,又含CL元素,所以为KCLO3,即B和C必为KCL和KCLO中的一种,综上所述:A:CL2? B与C为KCL或KCLO? D:KCLO3
③CL2+2NaOH=NaCL+NaCLO+H2O;④2KCLO3=====2KCL + 3O2↑
本题难度:一般
5、填空题 (10分)
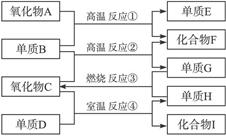
已知:①单质E可作为半导体材料;②化合物F是不能生成盐的氧化物;③化合物I能溶于水呈酸性,它能够跟氧化 物A起反应。
物A起反应。
据此,请填空:
⑴化合物F的化学式为__________,化合物I的化学式为_____________,氧化物A的晶体类型为_____________。
⑵反应①的化学方程式为___________________________________。
⑶氧化物A与烧碱溶液反应的离子方程式为___________________________________。
参考答案:
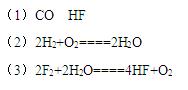
本题解析:

本题难度:一般