微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应: SO2(g)+NO2(g)  SO3(g)+NO(g) 达到平衡,正反应速率随时间变化如右图所示。则正确的结论是
SO3(g)+NO(g) 达到平衡,正反应速率随时间变化如右图所示。则正确的结论是
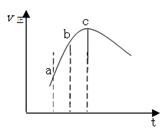
A.逆反应速率:a点小于点c
B.反应物浓度:a点小于点b
C.反应在c点时SO2的转化率最大
D.反应物的总能量低于生成物的总能量
参考答案:A
本题解析:本题主要结合坐标图考查化学反应速率。
选项A、a点的正反应速率比c点小,反应向正反应方向进行,故逆反应速率a<c;
选项B、a点的正反应速率比b点小,反应向正反应方向进行,故b点的反应物浓度应较小;
选项C、c点时正反应的速率达到最大值,并不意味着反应物的转化率就最大;
选项D、此题中没有给出反应过程中能量的变化,因此无法的出反应物与生成物总能量的大小;
点评:本题是对反应速率及化学平衡的相关考查,其难点在于以坐标图的形式,综合考查了图形分析能力。读懂图形,是解题的关键,可将数学中的数形结合思想应用到化学中。
本题难度:简单
2、选择题 下列变化过程需要吸收能量的是(?)
A.2H2+O2=2H2O
B.CaO+H2O=Ca(OH)2
C.Cl+Cl→Cl2
D.N2→N+N
参考答案:D
本题解析:略
本题难度:简单
3、选择题 在烃分子中去掉2个氢原子形成一个双键是吸热反应,大约需要117 kJ ・mol-1~125 kJ ・mol-1 的热量,但1,3-环己二烯失去2个氢原子形成苯是放热反应,反应热是23.4 kJ ・mol-1 ,这表明?
A.苯比1,3-环己二烯稳定
B.苯加氢生成环己烷是吸热反应
C.1,3-环己二烯比环己烷稳定
D.1,3-环己二烯加氢是吸热反应
参考答案:A
本题解析:A、1,3-环已二烯失去两个氢原子变成苯是放热反应,说明1,3-环已二烯的能量高于苯的,能量越低越稳定,所以苯更稳定,故A正确;
D、根据题意信息:烃分子中去掉两个氢原子形成一个双键是吸热反应,所以1,3-环已二烯加上两个氢原子是放热反应,故D错误;
B、根据题意信息可知,烃分子中去掉两个氢原子形成一个双键是吸热反应,所以烃分子中一个双键加上两个氢原子是放热反应,故B错误;
C、1,3-环已二烯失去两个氢原子变成苯是放热反应,说明1,3-环已二烯的能量高于苯的,能量越低越稳定,所以苯更稳定,故C错误。
故选A。
点评:本题考查学生吸热反应和放热反应的有关知识,可以根据所学知识来回答,难度不大。
本题难度:简单
4、简答题 已知A(g)+B(g)?C(g)+D(g)?反应过程中的能量变化如图所示,回答下列问题.
(1)该反应是______反应(填“吸热”、“放热”).当反应达到平衡时,升高温度,A的转化率______(填“增大”、“减小”或“不变”),
(2)在反应体系中加入催化剂,反应速率增大,E的变化是______,(填“增大”、“减小”或“不变”)理由是______;?E的大小对该反应的反应热有无影响?______.
(3)一定条件下,向体积为2L的恒容密闭容器中充入1mol?A(g)?和3mol?B(g),判断该反应达到平衡状态的依据是(填序号)______.
①c?(A)=c?(C)?②容器中压强不变
③混合气体的平均相对分子质量不变?④v(逆)(D)=v?(正)(B)
(4)在某温度下,反应物的起始浓度分别为:c(A)=1mol?L-1,c(B)=2.4mol?L-1,达到平衡后,A的转化率为60%,此时B?的转化率为______.
(5)若反应温度不变,反应物的起始浓度分别为:c(A)=4mol?L-1,c(B)=amol?L-1,达到平衡后,c(C)=2mol?L-1,列出计算式并求出a值.
参考答案:(1)由图象可以看出反应物总能量大于生成物的总能量,则该反应的正反应为放热反应.
升高温度平衡向吸热反应移动,即向逆反应移动,A的转化率减小.
故答案为:放热;减小.
(2)催化剂改变了反应的历程降,低活化能,加快反应速率,反应热取决于反应物总能量与生成物的总能量,催化剂不能影响反应热.
故答案为:减小;?因为催化剂改变了反应的历程使活化能E降低;?无影响.
(3)①平衡时A、C浓度可能相等,但c?A)=c(C)不能说明反应到达平衡,故①错误;
?②由方程式可知,反应前后气体体积不变,恒容下压强不发生变化,故②错误;
③混合物的总质量不变,总的物质的量不变,混合气体的平均相对分子质量始终不变,故③错误;
?④v(逆)(D)=v?(正)(B),速率之比等于化学计量数之比,说明反应到达平衡,故④正确.
故选:④.
(4))△c(A)=60%×1mol?L-1=0.6mol?L-1,浓度变化量之比等于化学计量数之比,所以△c(B)=△c(A)=0.6mol?L-1,故此时B的转化率0.6mol/L2.4mol/L×100%=25%.
故答案为:25%
(5)由(4)可知平衡时,各物质的浓度为c(A)=0.4mol/L,c(B)=2.4mol/L-0.6mol/L=1.8mol/L,c(C)=c(D)=△c(B)=△c(A)=0.6mol/L,所以平衡常数k=0.6×0.60.4×1.8=12.
反应物的起始浓度分别为:c(A)=4mol?L-1,c(B)=amol?L-1;达到平衡后,c(C)=2mol?L-1,则生成的D为2mol?L-1,平衡时c(A)=2mol?L-1,c(B)=(a-2)mol?L-1;
温度不变,则平衡常数不变,则2×22×(a-2)=12,a=6.
故答案为:6.
本题解析:
本题难度:一般
5、选择题 下列说法不正确的是
A.NH3・H2O NH4++OH-达到平衡后,升高温度平衡正向移动
NH4++OH-达到平衡后,升高温度平衡正向移动
B.在海轮的外壳上镶入锌块,可减缓船体的腐蚀速率
C.明矾水解生成Al(OH)3胶体,可用作净水剂
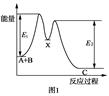
D.如图所示的反应过程中A+B→X的△H<0,X→C的△H>0
参考答案:D
本题解析:A.电解质的电离过程是吸热过程。当达到平衡后,升高温度,平衡吸热方向即向正向移动。正确。B.在海轮的外壳上镶入锌块,由于活动性Zn>Fe,Zn作原电池的负极,就可以对轮船起到保护作用,因此可减缓船体的腐蚀速率。正确。C.明矾KAl(SO4)2是强酸弱碱盐。Al3+水解生成Al(OH)3胶体,表面积大,吸附力强,可以吸附水中悬浮的固体颗粒,当重力大于浮力时就从水中沉淀出去,从而达到净化水的目的。因此可用作净水剂。正确。D.由图可以看出反应过程中A+B→X中的反应物的能量不如生成物的X的能量高,所以该反应的△H>0,而反应X→C由于反应物X的能量高,生成物C的能量低,所以该反应的△H<0。错误。
本题难度:一般