��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �ܹ������������д�����Ԫ�ص�ʵ�������
A������������ֱ�Ӽ���AgNO3��Һ
B��������ˮ����ֽ������AgNO3��Һ
C������NaOH��Һ�����Ⱥ����ϡ�����ữ��Ȼ�����AgNO3��Һ
D������NaOH���Ҵ���Һ�����Ⱥ����AgNO3��Һ
�ο��𰸣�C
��������������鲻��ֱ�ӵ���������ӣ���Ҫͨ���������ˮ�ⷴӦ���������ӣ�Ȼ����ͨ����������������ɡ�����ˮ�ⷴӦ���ڼ��������½��еģ��������ӵļ�����Ҫ����������������ȷ�Ĵ�ѡC��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣����Ĺؼ����ڼ�����������Һ֮ǰ��Ҫ���Ƚ����ữ����������������ѧ�����ۺ�ʵ���������Ͻ�����˼ά������
�����Ѷȣ���
2��ѡ���� ���б�ʾ����ȷ����
A.1mol H2
B.1molFe
C.1mol��
D.1mol NH3
�ο��𰸣�C
���������
�����Ѷȣ���
3��ѡ���� ������طֽ����������ʣ�����л��ն������̵IJ���˳����ȷ����
[? ]
A���ܽ⡢���ˡ�����������
B���ܽ⡢���ˡ�ϴ�ӡ�����
C���ܽ⡢������ϴ�ӡ�����
D���ܽ⡢ϴ�ӡ����ˡ�����
�ο��𰸣�B
���������
�����Ѷȣ�һ��
4��ʵ���� �Ȼ����dz�����ˮ�����������÷���м���Ʊ���ˮ�Ȼ�����ʵ�����Ʊ�װ�ú�ҵ�Ʊ�����ͼ���£�
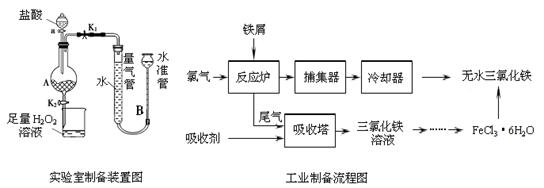
��֪��(1)��ˮFeCl3���۵�Ϊ555 K���е�Ϊ588 K��
(2) ����м�е����ʲ������ᷴӦ
(3)��ͬ�¶�����ˮ���Ȼ�����ˮ�е��ܽ�����£�
�¶�/��
| 0
| 20
| 80
| 100
|
�ܽ��(g/100 g H2O)
| 74.4
| 91.8
| 525.8
| 535.7
|
?
ʵ�����Ʊ������������£�
��.���ɼ�K1���رյ��ɼ�K2��������a�������μ����ᡣ
��.��?ʱ���رյ��ɼ�K1�����ɼ�K2����A����Һ��ȫ�����ձ���رջ���a��
��.���ձ�����Һ����һϵ�в�����õ�FeCl3��6H2O���塣
��ش�
��1���ձ���������H2O2��Һ��������?��
��2��Ϊ�˲ⶨ����м�����������������������С���������������__________��
��3����FeCl3��Һ�Ƶ�FeCl3?6H2O����IJ��������ǣ�����?_?��?_?�����ˡ�ϴ�ӡ����
��4����д���������з�Ӧ�����ӷ���ʽ��?��
��5���������¶ȳ���673 Kʱ��������Է�������Ϊ325�������Ȼ�������ʵķ���ʽΪ?��
��6��FeCl3����������ͨ�����õ������ⶨ����ȡm g��ˮ�Ȼ�����Ʒ������ϡ���ᣬ���Ƴ�100mL��Һ��ȡ��10.00mL�������Թ�����KI��Һ����ַ�Ӧ���뼸�ε�����Һ������c?mol?L-1?Na2S2O3��Һ�ζ�������V?mL����֪��I2+2S2O32-�T2I-+S4O62-����
�ٵζ��յ�������ǣ�?_??
����Ʒ���Ȼ�������������?_?
�ο��𰸣���1������������ȫ������������������?��2�֣�
��2��װ��A�в��������ݻ������ܺ�ˮ��Һ�治�䣨����������Ҳ���֣���2�֣�
��3�����ᣨ1�֣�?����Ũ������ȴ�ᾧ��1�֣�
��4��2Fe2+ + Cl2 = 2Fe3+?��2�֣�
��5��Fe2Cl6��2�֣�
��6���� ��Һ����ɫ����ɫ���Ұ�����ڲ���ɫ��2�֣�
��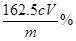 ��2�֣�
��2�֣�
�����������1������ʵ��װ�úͲ��������֪��ʵ�����Ʊ���ˮFeCl3���������������ᷴӦ����FeCl2��Ȼ���FeCl2������FeCl3�����Ƶ�FeCl3��6H2O���壬���ѽᾧˮ�Ƶ���ˮFeCl3���ձ���������H2O2��Һ����������������������ȫ�����������������ӣ�
��2���������ᷴӦ��ȫʱ�����ٲ�������������װ��A�в��������ݻ������ܺ�ˮ�ܵ�Һ�治�ٱ仯����ʱ���ɽ�A��FeCl2��Һ�����ձ��н���������
��3����FeCl3��Һ�Ƶ�FeCl3?6H2O����IJ��������ǣ�����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����
��4���ӹ�ҵ�Ʊ�����ͼ������֪����Ӧ¯�н��еķ�Ӧ�� 2Fe + 3Cl2 = 2FeCl3����ˣ������������е�β����û�вμӷ�Ӧ���������������������������ռ����գ���Ӧ������2FeCl3��Һ���������ռ�Ӧ��2FeCl2��Һ����Ӧ�����ӷ���ʽΪ��2Fe2+ + Cl2 = 2Fe3+��
��5���������ռ�������̬FeCl3��FeCl3����Է���������162.5������Է�������Ϊ325�������Ȼ�������Ƴ������¶ȳ���673 Kʱ����������̬FeCl3���Ծۺ�����˫����Fe2Cl6������ע��FeCl3�������ͻ�������������ѡ���ͪ���л��ܼ�����673K��������˫���壬1023K���Ϸֽ�Ϊ�����ӣ���
��6���ٳ�ȡm g��ˮ�Ȼ�����Ʒ������ϡ���ᣬ���Ƴ�100mL��Һ��ȡ��10.00mL�������Թ�����KI��Һ����ַ�Ӧ���뼸�ε�����Һ����ʱ��Һ����ɫ����?Na2S2O3��Һ�ζ����������һ��Na2S2O3��Һ����ƿ�ڵ���Һ����ɫ��Ϊ��ɫ���Ұ�����ڲ���ɫ�����Եζ��յ�������ǣ���Һ����ɫ��Ϊ��ɫ���Ұ�����ڲ���ɫ��
�� ����Ʒ���Ȼ�������������
�ɷ�Ӧ��2Fe3+ + 2I - = 2Fe2+ + I2��? I2+2S2O32-�T2I-+S4O62-���ɵù�ϵʽ��
2Fe3+? ��? I2 ��? 2S2O32-
1? 1
n? cV��10-3?
���n(Fe3+) = cV��10-3 mol��?����Ʒ���Ȼ�������������Ϊ��
��(Fe3+) = cV��10-3 mol��10��162.5g/mol��100% = 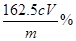
�����Ѷȣ�����
5��ѡ���� ���г�ȥ���ʵķ�����ȷ����
[? ]
A����ȥ��������������ϩ������������ͨ��Cl2����Һ����
B����ȥ�����Ҵ�������������ñ���̼������Һϴ�ӡ���Һ
C����ȥCO2��������SO2������ͨ��ʢ�б���̼������Һ��ϴ��ƿ
D����ȥ�Ҵ��������������������ʯ�ң�����
�ο��𰸣�B
���������
�����Ѷȣ�һ��