��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ���¶��½�1molCO��1molH2O(g)ͨ��һ���ܱ������з�Ӧ��CO(g)+H2O(g) CO2(g)+H2(g)���ﵽƽ���CO2�����ʵ���Ϊ0��6mol����ͨ��4molH2O(g)�ﵽƽ���CO2�����ʵ���������
CO2(g)+H2(g)���ﵽƽ���CO2�����ʵ���Ϊ0��6mol����ͨ��4molH2O(g)�ﵽƽ���CO2�����ʵ���������
[? ]
A������0��6mol
B������1mol
C������1mol
D������0��6mol����1mol
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2������� ��ѧ��Ӧԭ���ڿ��к��������й㷺Ӧ��
��1�����á���ѧ����ת�Ʒ����Ʊ�TaS2���壬�������·�ӦTaS2(s)+2I2(g) TaI4(g)+S2(g)? ��H��0?����Ӧ����ƽ�ⳣ������ʽK=?����K=1����ij�����ܱ������м���1mol I2��g��������TaS2��s����I2��g����ƽ��ת����Ϊ ?��
TaI4(g)+S2(g)? ��H��0?����Ӧ����ƽ�ⳣ������ʽK=?����K=1����ij�����ܱ������м���1mol I2��g��������TaS2��s����I2��g����ƽ��ת����Ϊ ?��
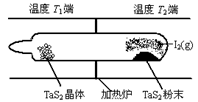
��2����ͼ��ʾ����Ӧ������ʯӢ��չ��н��У������¶�ΪT2��һ�˷���δ�ᴿ��TaS2��ĩ������I2��g����һ��ʱ������¶�ΪT1��һ�˵õ��˴�����TaS2���壬���¶�T1?T2���������������=������������Ӧ��ϵ��ѭ��ʹ�õ�������?��
��3������I2�������Կɲⶨ��������ĺ����������ǽ������е���ת��Ϊ H2SO3��Ȼ����һ��Ũ�ȵ�I2��Һ���еζ�������ָʾ��Ϊ?���ζ���Ӧ�����ӷ���ʽΪ?��
��4��25��ʱ��H2SO3 HSO3-+H+�ĵ��볣��Ka=1��10-2mol/L������¶���NaHSO3��ˮ��ƽ�ⳣ��Kh=?mol/L������NaHSO3��Һ�м���������I2������Һ��
HSO3-+H+�ĵ��볣��Ka=1��10-2mol/L������¶���NaHSO3��ˮ��ƽ�ⳣ��Kh=?mol/L������NaHSO3��Һ�м���������I2������Һ��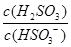 ��?���������С�����䡱����
��?���������С�����䡱����
�ο��𰸣�
��1�� ��66.7%��
��66.7%��
��2������ I2��
��3�����ۣ� H2SO3+I2+H2O=2I��+SO42��+4H����
��4��1.0��10��12������
���������
��1����������Ļ�ѧ����ʽ��TaS2��s��+2I2��g�� TaI4��g��+S2��g������֪K=
TaI4��g��+S2��g������֪K= ������K=1����ƽ��ʱTaI4��S2�����ʵ���Ϊx�������ƽ�ⳣ������ʽ����x/V��2=����1-2x��/V��2������x2=��1-2x��2�����x=1/3����I2��g����ƽ��ת����Ϊ��(2/3)��100%=66.7%��
������K=1����ƽ��ʱTaI4��S2�����ʵ���Ϊx�������ƽ�ⳣ������ʽ����x/V��2=����1-2x��/V��2������x2=��1-2x��2�����x=1/3����I2��g����ƽ��ת����Ϊ��(2/3)��100%=66.7%��
��2����������Ļ�ѧ����ʽ��TaS2��s��+2I2��g�� TaI4��g��+S2��g��? ��H��0���÷�Ӧ�������ȣ����ڷ�Ӧ����T2�˿�ʼ��һ��ʱ�����T1�˵õ����壬˵����Ӧ���ɵ�������T1���¶Ƚ���ƽ�����ƣ����¶�T1��T2���������仯������I2����ѭ��ʹ�ã�
TaI4��g��+S2��g��? ��H��0���÷�Ӧ�������ȣ����ڷ�Ӧ����T2�˿�ʼ��һ��ʱ�����T1�˵õ����壬˵����Ӧ���ɵ�������T1���¶Ƚ���ƽ�����ƣ����¶�T1��T2���������仯������I2����ѭ��ʹ�ã�
��3������I2�������Կɲⶨ��������ĺ���ʱ��ָʾ���ǵ��ۣ���Ӧ�����ӷ���ʽΪ��H2SO3+I2+H2O= 2I��+SO42��+4H����
��4������NaHSO3��ˮ�ⷽ��ʽ��HSO3-+H2O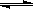 H2SO3+OH������ˮ��ƽ�ⳣ���ı���ʽΪ��Kh=c(H2SO3)��c(OH��)/c(HSO3-)����Ka��Kh= c(H+)��c(OH��)=Kw�������Kh =1.0��10��12������NaHSO3��Һ�м���������I2����Һ�з�����Ӧ��HSO32-+I2+H2O=SO42-+2I-+3H+�������ӽ�����������ӣ�ʹƽ�������ƶ��������Һ��
H2SO3+OH������ˮ��ƽ�ⳣ���ı���ʽΪ��Kh=c(H2SO3)��c(OH��)/c(HSO3-)����Ka��Kh= c(H+)��c(OH��)=Kw�������Kh =1.0��10��12������NaHSO3��Һ�м���������I2����Һ�з�����Ӧ��HSO32-+I2+H2O=SO42-+2I-+3H+�������ӽ�����������ӣ�ʹƽ�������ƶ��������Һ��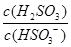 ����
����
�����㶨λ�������ۺϿ����˻�ѧƽ�ⳣ��������ƽ�ⳣ����ˮ��ƽ�ⳣ����ƽ��ת���ʡ���ѧƽ����ƶ����ζ�ָʾ����ѡ���֪ʶ��
�����Ѷȣ�һ��
3��ѡ���� �ϳɰ���Ӧ��N2 + 3H2 2NH3?��H����92.4 kJ��mol������ͼ�Ǹ÷�Ӧ�����ʡ�ʱ��ͼ��һ�������£�t1ʱ����ƽ�⣬? t2ʱ�ı�ijһ������t3ʱ�ֽ�����ƽ�⣬t2ʱ�ı������������
2NH3?��H����92.4 kJ��mol������ͼ�Ǹ÷�Ӧ�����ʡ�ʱ��ͼ��һ�������£�t1ʱ����ƽ�⣬? t2ʱ�ı�ijһ������t3ʱ�ֽ�����ƽ�⣬t2ʱ�ı������������
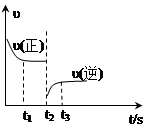
A�������¶�
B����������ְ���
C������ѹǿ
D������Ӧ��Ũ��
�ο��𰸣�B
�������������ͼ���֪��t2ʱ����Ӧ���ʲ��䣬���淴Ӧ����ͻȻ���ͣ�ƽ��������Ӧ�����ƶ������Ըı������Ӧ���Ƿ�������ְ�������������������Ũ�ȣ���ѡB��
�����������ǻ���������Ŀ��飬��Ҫ�ǿ���ѧ�����������Ӱ�췴Ӧ���ʺ�ƽ��״̬���˽����������ּ������ѧ��������û���֪ʶ���ʵ�����������������������ѧ���������������ͳ���˼ά������
�����Ѷȣ�һ��
4������� ��ˮ��Һ�гʳȺ�ɫ��Cr2O72-��ʻ�ɫ��CrO42-������ƽ���ϵ��Cr2O72-��H2O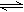 2CrO42-��2H�������ظ���أ�K2Cr2O7������ˮ���ϡ��Һ�ʳ�ɫ��
2CrO42-��2H�������ظ���أ�K2Cr2O7������ˮ���ϡ��Һ�ʳ�ɫ��
��1��ȡ����������Һ����NaOH��Һ����Һ��_________ɫ����Ϊ___?________��
��������ټ������ϡH2SO4������Һ��__?__ɫ����Ϊ__________?_________��
��ȡ����ԭ��Һ�������м���Ba(NO3)2��Һ����֪BaCrO4Ϊ��ɫ����������ƽ��_____?____����Һ��ɫ��_____?____��
�ο��𰸣���1����?����NaOH�к���H+,ʹc(H+)���ͣ�ƽ��������Ӧ�����ƶ���c(Cr2O72-)��С��c(CrO42-)����
��2���Ⱥ�?����H2SO4����Һ��c(H+)����ƽ�����淴Ӧ�����ƶ���c(CrO42-)���ͣ�c(Cr2O72-)����
��3��������Ӧ�����ƶ�?��dzֱ����ɫ
���������������������Ի�ѧƽ���Ӱ�졣
��1�������������ƣ��к���Һ�е������ӣ�������Ũ�Ƚ���ƽ��������Ӧ�����ƶ���c(Cr2O72-)��С��c(CrO42-)������Һ�Ի�ɫ��
��2���ټ������ᣬ��Һ��c(H+)����ƽ�����淴Ӧ�����ƶ���c(CrO42-)���ͣ�c(Cr2O72-)���������ԳȺ�ɫ��
��3������Ba(NO3)2��Һ��������BaCrO4��ɫ������c(CrO42-)���ͣ�ƽ��������Ӧ�����ƶ�����Һ����ɫ����dz��ֱ����ɫ��
�����Ѷȣ�һ��
5��ѡ���� (2011��ɽ��ݷ�ظ߶���ĩ)ͼ����NO2(g)��CO(g)? ?CO2(g)��NO(g)��Ӧ�����������仯ʾ��ͼ��һ�������£��ڹ̶��ݻ����ܱ������и÷�Ӧ�ﵽƽ��״̬�����ı�����һ������X��Y��X�ı仯��ϵ������ͼ��
?CO2(g)��NO(g)��Ӧ�����������仯ʾ��ͼ��һ�������£��ڹ̶��ݻ����ܱ������и÷�Ӧ�ﵽƽ��״̬�����ı�����һ������X��Y��X�ı仯��ϵ������ͼ��
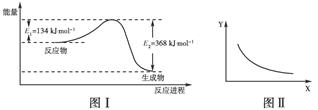
�����й�˵����ȷ����(����)
A���÷�Ӧ���ʱ䦤H����234 kJ��mol��1
B����X��ʾ��ϵ��ѹǿ����Y��ʾ�Ŀ�����NO2��ת����
C����X��ʾ�¶���Y��ʾ�Ŀ�����CO2���ʵ���Ũ��
D������CO����ʼŨ�ȣ�ƽ��������Ӧ�����ƶ�����Ӧ������
�ο��𰸣�C
�����������ͼ���֪���÷�Ӧ���ʱ�Ϊ��H����234 kJ��mol��1��A��������ѹǿ��ƽ�ⲻ�ƶ���NO2��ת���ʲ��䣬B��������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ���CO2���ʵ���Ũ�ȼ�С��C��ȷ������CO����ʼŨ�ȣ���Ȼƽ��������Ӧ�����ƶ����ų����������ӣ�����Ӧ�Ȳ��䣬D����
�����Ѷȣ�һ��