微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知25℃时,电离常数Ka(HF)=3.6×10-4,溶度积常数Ksp(CaF2)=1.46×10-10。现向1 L 0.2mol・L-1HF溶液中加入1 L 0.2 mol・L-1CaCl2溶液,则下列说法中,正确的是(?)
A.25℃时,0.1 mol・L-1HF溶液中pH=1
B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中有CaF2沉淀产生
D.加入CaCl2溶液后体系中的c(H+)浓度不变
参考答案:C
本题解析:A、电离常数Ka(HF)=3.6×10-4,HF为弱电解质,不能完全电离,25℃时,0.1mol?L-1HF溶液中c(H+)=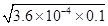 mol/L=6×10-3mol/L,pH>1,故A错误;B、溶度积只受温度的影响,不随浓度的变化而变化,故B错误;C、向1L?0.2mol?L-1HF溶液中加入1L?0.2mol?L-1CaCl2溶液,混合后,c(H+)=c(F-)=
mol/L=6×10-3mol/L,pH>1,故A错误;B、溶度积只受温度的影响,不随浓度的变化而变化,故B错误;C、向1L?0.2mol?L-1HF溶液中加入1L?0.2mol?L-1CaCl2溶液,混合后,c(H+)=c(F-)=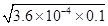 mol/L=6×10-3mol/L,c(Ca2+)=0.1mol/L,c2(F-)×c(Ca2+)=3.6×10-5×0.1=3.6×10-6>1.46×10-10,该体系中有CaF2沉淀产生,故C正确;D、溶液中存在HF
mol/L=6×10-3mol/L,c(Ca2+)=0.1mol/L,c2(F-)×c(Ca2+)=3.6×10-5×0.1=3.6×10-6>1.46×10-10,该体系中有CaF2沉淀产生,故C正确;D、溶液中存在HF H++F-,CaF2(s)
H++F-,CaF2(s) Ca2+(aq)+2F-(aq),加入CaCl2溶液后,Ca2+浓度增大,平衡向生成沉淀的方向移动,则F-浓度减小,促进HF的电离,c(H+)浓度增大,故D错误,答案选C。
Ca2+(aq)+2F-(aq),加入CaCl2溶液后,Ca2+浓度增大,平衡向生成沉淀的方向移动,则F-浓度减小,促进HF的电离,c(H+)浓度增大,故D错误,答案选C。
本题难度:一般
2、选择题 下列电离方程式正确的是( )
A.NaHSO4 Na++HSO4―
Na++HSO4―
B.NaHCO3 Na++H++CO3―
Na++H++CO3―
C.H3PO4 3H++PO43―
3H++PO43―
D.HF H++F-
H++F-
参考答案:D
本题解析:
选项
错因分析
正确写法
A
HS是强酸根,在水溶液中完全电离
NaHSO4 Na++H++SO42―
Na++H++SO42―
B
NaHCO3是强电解质,应写“ ”,且C是弱酸根,不能拆开
”,且C是弱酸根,不能拆开
NaHCO3 Na++HCO3―
Na++HCO3―
C
H3PO4是三元弱酸,应分步书写
H3PO4 H++H2PO4―
H++H2PO4―
H2PO4― H++HPO42―
H++HPO42―
HPO42― H++PO43―
H++PO43―
本题难度:一般
3、选择题 下列叙述中,错误的是( )
A.虽然固体氯化钠不能导电,但氯化钠是电解质
B.纯水的pH随温度的升高而减小
C.在醋酸钠溶液中加入少量氢氧化钠,溶液中c(OH-)增大
D.在纯水中加入少量硫酸铵,可抑制水的电离
参考答案:D
本题解析:
本题难度:简单
4、选择题 欲使0.1 mol・L-1NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减少的方法是
[? ]
A. 通入二氧化碳气体
B. 加入NaOH固体
C. 通入HCl气体
D. 加入饱和石灰水
参考答案:D
本题解析:
本题难度:一般
5、简答题 (22分)研究碳及其化合物的性质和用途是中学化学的任务之一。
I.某兴趣小组在实验室中制备碳酸钠溶液。方案如下:步骤一,取25 mL一定浓度的NaOH溶液,通人CO2气体至过量;步骤二,加热煮沸步骤一所得溶液;步骤三,另取25 mL相同浓度的NaOH溶液与步骤二所得溶液混合,即得碳酸钠溶液。
(1)完成步骤一可选的化学试剂有:稀盐酸、NaOH溶液、大理石、饱和碳酸钠溶液、稀硫酸、饱和碳酸氢钠溶液等,需要的装置如下所示。
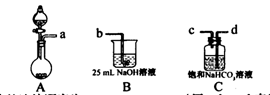
①各装置正确的连接顺序为?(用a、b、c、d表示)。
②检查整套装置气密性的方法是?。
③装置A中常用药品为?;装置C中化学药品的作用是?。
(2)写出步骤三中发生反应的离子方程式?。
(3)有同学提出“步骤二”没有必要,请你简述自己的看法?。
Ⅱ.实验室用纯碱和盐酸处理某种蛇纹石(已知蛇纹石中含有MgO、SiO2.CaO、Fe2O3、Al2O3等氧化物)模拟制备氧化镁的流程如下:
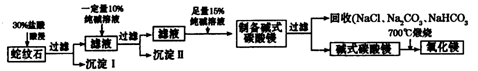
(1)过滤需要的玻璃仪器有?。
(2)沉淀Ⅱ的成分为?,请用离子方程式表示生成沉淀的过程?(写出一个即可)。
(3)纯碱溶液中所有离子浓度的大小关系为?。
(4)已知l0%的纯碱溶液密度为1.06g/cm3,则其物质的量浓度为____?,
参考答案:I.(1)①a d
d c
c b。②关闭分液漏斗活塞,向烧杯中加水至没过导管口,微热烧瓶,导管口有气泡冒出,停止加热,导管内形成一段水柱,说明装置气密性良好。③稀盐酸和大理石;除去二氧化碳中的氯化氢。(2)OH-+HCO3―====CO32―+H2O。(3)步骤二的目的为除去溶解的过量的二氧化碳,否则将使碳酸钠不纯。
b。②关闭分液漏斗活塞,向烧杯中加水至没过导管口,微热烧瓶,导管口有气泡冒出,停止加热,导管内形成一段水柱,说明装置气密性良好。③稀盐酸和大理石;除去二氧化碳中的氯化氢。(2)OH-+HCO3―====CO32―+H2O。(3)步骤二的目的为除去溶解的过量的二氧化碳,否则将使碳酸钠不纯。
Ⅱ.(1)烧杯、漏斗、玻璃棒。(2)根据上述分析知,沉淀Ⅱ的成分为CaCO3、Fe(OH)3、Al(OH)3,CO32- + Ca2+====CaCO3↓,2Fe3+ + 3CO32- + 3H2O ="===" 2Fe(OH)3↓ + 3CO2↑,2Al3+ + 3CO32- + 3H2O====2Al(OH)3↓ + 3CO2↑;(3)c(Na+)>c(CO32―)>c(OH-)>c(HCO3―)>c(H+)。(4)1 mo1・L-1。
本题解析:I.根据题意知,该小组制备碳酸钠溶液的原理为:CO2(过量)+NaOH====NaHCO3,NaOH+NaHCO3====Na2CO3+H2O。(1)分析题给装置知,A为二氧化碳的发生装置,B中发生二氧化碳与氢氧化钠溶液的反应,C装置除去二氧化碳中的氯化氢;①为制得纯净的碳酸氢钠溶液,要先除去二氧化碳中的氯化氢,各装置正确的连接顺序为a d
d c
c b。②检查整套装置气密性的方法是关闭分液漏斗活塞,向烧杯中加水至没过导管口,微热烧瓶,导管口有气泡冒出,停止加热,导管内形成一段水柱,说明装置气密性良好。③实验室制备二氧化碳的原理为碳酸钙和稀盐酸反应,装置A中常用药品为稀盐酸和大理石;装置C中化学药品的作用是除去二氧化碳中的氯化氢。?(2)步骤三中发生反应的离子方程式为OH-+HCO3―====CO32―+H2O。?(3)步骤二的目的为除去溶解的过量的二氧化碳,否则将使碳酸钠不纯。
b。②检查整套装置气密性的方法是关闭分液漏斗活塞,向烧杯中加水至没过导管口,微热烧瓶,导管口有气泡冒出,停止加热,导管内形成一段水柱,说明装置气密性良好。③实验室制备二氧化碳的原理为碳酸钙和稀盐酸反应,装置A中常用药品为稀盐酸和大理石;装置C中化学药品的作用是除去二氧化碳中的氯化氢。?(2)步骤三中发生反应的离子方程式为OH-+HCO3―====CO32―+H2O。?(3)步骤二的目的为除去溶解的过量的二氧化碳,否则将使碳酸钠不纯。
Ⅱ.根据题给流程分析,蛇纹石用30%盐酸酸浸,MgO、CaO、Fe2O3、Al2O3和盐酸反应溶解,反应方程式分别为:MgO+2HCl=MgCl2+H2O,CaO+2HCl=CaCl2+H2O,Fe2O3+6HCl=2FeCl3+3H2O,Al2O3+6HCl=2AlCl3+3H2O;而SiO2不与盐酸反应,过滤得沉淀Ⅰ为二氧化硅,滤液为MgCl2、CaCl2、FeCl3、AlCl3和盐酸的混合液,向滤液中加入一定量10%纯碱溶液,Ca2+、Fe3+、Al3+和碳酸钠溶液反应转化为氢氧化铁、氢氧化铝和碳酸钙沉淀经过滤而除去,反应方程式为CO32- + Ca2+====CaCO3↓,2Fe3+ + 3CO32- + 3H2O ="===" 2Fe(OH)3↓ + 3CO2↑,2Al3+ + 3CO32- + 3H2O====2Al(OH)3↓ + 3CO2↑;向滤液中加足量15%纯碱溶液制得碱式碳酸镁,过滤,回收氯化钠、碳酸钠和碳酸氢钠,碱式碳酸镁煅烧得氧化镁。(1)过滤需要的玻璃仪器有烧杯、漏斗、玻璃棒。(2)根据上述分析知,沉淀Ⅱ的成分为CaCO3、Fe(OH)3、Al(OH)3,用离子方程式表示生成沉淀的过程CO32- + Ca2+====CaCO3↓,2Fe3+ + 3CO32- + 3H2O ="===" 2Fe(OH)3↓ + 3CO2↑,2Al3+ + 3CO32- + 3H2O====2Al(OH)3↓ + 3CO2↑;(3)纯碱溶液中所有离子浓度的大小关系为c(Na+)>c(CO32―)>c(OH-)>c(HCO3―)>c(H+)。(4)利用公式c=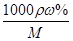 ?将题给数据代入计算,纯碱溶液的物质的量浓度为1 mo1・L-1。
?将题给数据代入计算,纯碱溶液的物质的量浓度为1 mo1・L-1。
本题难度:一般