微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 从下列现象可以判断某一元酸是强酸的是( )
A.加热该酸至沸腾也不分解
B.该酸溶液可与石灰石反应放出CO2
C.该酸溶液可以溶解Al(OH)3沉淀
D.该酸溶液浓度为0.1mol/L时pH=1
参考答案:A.弱酸也可以沸腾不分解,如:乙酸是弱酸,但它在440℃的高温下,乙酸分解才分解生成甲烷和二氧化碳或乙烯酮和水.有的一元强酸沸腾时,反而分解.如:硝酸,硝酸是一元强酸,浓硝酸硝酸在0℃下就会慢慢分解,室温下也是,温度温度高的时候分解速度明显加快.浓硝酸硝酸见光分解分4HNO3=4NO2↑+O2↑+H2O,故A错误;
B.石灰石的主要成分为CaCO3,CaCO3+2CH3COOH=Ca(CH3COO)2 +CO2↑+H2O醋酸酸性比碳酸强比碳酸强,能与石灰石反应放出CO2,但醋酸是弱酸,故B错误;
C.溶解Al(OH)3沉淀的不一定是一元强酸,一元弱酸,只要电离出的c(H+)较大,即可以使Al(OH)3溶解,故C错误;
D.pH=1,指酸溶液中c(H+)=0.1 mol?L-1,当0.1 mol?L-1的一元酸溶液中c(H+)=0.1 mol?L-1时,说明该一元酸完全电离,是一元强酸,故D正确;.
故选D.
本题解析:
本题难度:简单
2、选择题 将l00ml?1mol/L?的NaHCO3溶液等分为两份,其中一份加入少许冰醋酸,另外一份加入少许Ba(OH)2固体,忽略溶液体积变化.两份溶液中c(CO32-)的变化分别是( )
A.减小、减小
B.减小、增大
C.增大、增大
D.增大、减小
参考答案:B
本题解析:
本题难度:简单
3、填空题 某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验:常温下将pH=2的两种酸溶液HA、HB和pH=12的MOH碱溶液各1 mL,分别加水稀释到1 000 mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:
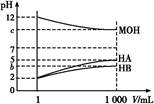
(1)HA为?酸,HB为?酸(填“强”或“弱”)。
(2)若c=9,则稀释后的三种溶液中,由水电离的氢离子浓度的大小顺序为?(用酸、碱化学式表示)。
(3)若c=9,将稀释后的HA溶液和MOH溶液取等体积混合,则所得溶液中c(A-)与c(M+)的大小关系为c(A-)?(填“大于”、“小于”或“等于”)c(M+)。
(4)若b+c=14,则MOH为?碱(填“强”或“弱”)。将稀释后的HB溶液和MOH溶液取等体积混合,所得混合溶液的pH?7(填“大于”、“小于”或“等于”)。
参考答案:(1)强?弱? (2)MOH=HA>HB
(3)等于? (4)弱?等于
本题解析:(1)pH相同的两种酸稀释相同的倍数,弱酸的pH变化小,由图可知pH=2的酸溶液稀释1 000倍,HA的pH=5,则HA是强酸,而HB溶液稀释后pH<5,则HB是弱酸。
(2)若c=9,则MOH是强碱,则溶液中由水电离出的c(H+)=10-9 mol/L,而HA溶液pH=5,c(H+)=10-5 mol/L,则c(OH-)=c(H+)水电离=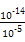 ?mol/L=10-9 mol/L,因HB溶液pH<5,则c(H+)>10-5 mol・L-1,溶液中水电离出的
?mol/L=10-9 mol/L,因HB溶液pH<5,则c(H+)>10-5 mol・L-1,溶液中水电离出的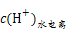 =c(OH-)<10-9 mol/L,则由水电离的c(H+)大小顺序为MOH=HA>HB。
=c(OH-)<10-9 mol/L,则由水电离的c(H+)大小顺序为MOH=HA>HB。
(3)若c=9,相当于强酸HA溶液和强碱MOH溶液等体积等浓度混合,两者恰好完全反应,则pH=7,即c(H+)=c(OH-),再根据电荷守恒可知,c(H+)+c(M+)=c(OH-)+c(A-)可得出c(A-)=c(M+)。
(4)若b+c=14,而b<5,则c>9,可判断MOH为弱碱,又因稀释前HB溶液中c(H+)=10-2 mol・L-1,稀释后HB溶液中c(H+)=10-b mol・L-1,而稀释前MOH溶液中c(OH-)=10-2 mol・L-1,稀释后MOH溶液中c(OH-)=10-14+c mol・L-1=10-b mol・L-1,故两者稀释前后,c(H+)与c(OH-)分别对应相等,据此可知:HB与MOH的强弱相当,故两溶液混合相当于等体积等浓度等电离程度的HB与MOH混合,两者恰好完全反应生成MB,且M+与B-的水解程度相同,故所得混合溶液pH=7。
本题难度:一般
4、选择题 pH相同的盐酸(甲)和醋酸(乙),分别与锌反应,若最后锌粒全部溶解且放出气体一样多,为此下列说法正确的是( )
A.反应开始时的速率:甲<乙
B.反应开始时,酸的物质的量浓度:甲<乙
C.反应所需时间:甲<乙
D.反应后溶液的pH:甲<乙
参考答案:B
本题解析:
本题难度:一般
5、填空题 (6分)下列物质:①水②醋酸③盐酸④烧碱⑤硝酸钾⑥酒精⑦汽油⑧蔗糖
(用编号回答)其中属于弱电解质的有?;属于强电解质的有?;强电解质在水中?电离。
参考答案:①②;④⑤;完全(几乎完全;全部)
本题解析:略
本题难度:简单