微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性.下述为相关实验步骤和实验现象:

请回答:
(1)写出A、B和C的化学式:A______,B______,C______;
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:______,______;
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:______;
(4)写出由F→H的化学方程式:______.
参考答案:钠盐A能和AgNO3溶液反应生成一种难溶于HNO3的黄色沉淀,可确定A为NaI,C为AgI;黄绿色气体F是Cl2;F和NaOH溶液反应生成钠盐B,根据B呈碱性并具有氧化性,可知B为NaClO(NaCl、NaClO3溶液均呈中性);NaClO具有强氧化性,能氧化NaI,少量NaClO将NaI氧化成I2,进一步反应生成NaIO3,其中I为+5价;Cl2氧化FeCl2生成FeCl3,FeCl3又能氧化SO2生成SO42-,则
(1)由以上分析可知A为NaI,B为NaClO,C为AgI,故答案为:NaI;?NaClO;?AgI;
(2)NaClO具有强氧化性,能氧化NaI,少量NaClO将NaI氧化成I2,反应的离子方程式为2I-+ClO-+H2O=I2+Cl-+2OH-,
进一步反应可把I2氧化为NaIO3,反应的离子方程式为I2+5ClO-+2OH-=2IO3-+5Cl-+H2O,
故答案为:2I-+ClO-+H2O=I2+Cl-+2OH-;?I2+5ClO-+2OH-=2IO3-+5Cl-+H2O;
(3)FeCl3能氧化SO2生成SO42-,反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,
故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
(4)F→H为Cl2与NaOH的反应,反应的方程式为Cl2+2NaOH=NaClO+NaCl+H2O,故答案为:Cl2+2NaOH=NaClO+NaCl+H2O.
本题解析:
本题难度:一般
2、填空题 (15分)
A、B、C、D、E、F、G、H、和I、是中学化学中常见的气体,它们均由短周期元素组成,具有如下性质:
①A、B、E、F、G能使湿润的蓝色石蕊试纸变红,I能使湿润的红色石蕊试纸变蓝,C、D、H不能使湿润的石蕊试纸变色;
②A和I相遇产生白色烟雾;
③B和E都能使品红溶液褪色;
④将红热的铜丝放入装有B的瓶中,瓶内充满棕黄色的烟;
⑤将点燃的镁条放入装有F的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
⑥C和D相遇生成红棕色气体;
⑦G在D中燃烧可以产生E和H2O;
⑧将B和H在瓶中混合后于亮处放置几分钟,瓶内壁出现油状液滴并产生A。
回答下列问题:
(1)A的化学式是,②中烟雾的化学式是;
(2)④中发生反应的化学方程式是 ;
;
(3)⑤中发生反应的化学方程式是;
(4)C的化学式是,D的化学式是;
(5)⑦中发生反应的化学方程式是;
(6)H的化学式是。
参考答案:
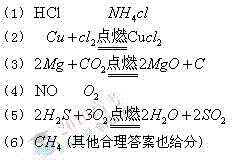
本题解析:略
本题难度:简单
3、填空题 (10分)甲、乙、丙为常见单质,乙、丙两元素在周期表中位于同一主族。x、 A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,G的焰色反应为黄色。在一定条件下,各物质相互转化关系如下图:

(1)用化学式表示:丙为?,C为 ??
(2)X的电子式为?。
(3)写出A与H2O反应的化学方程式:??
(4)写出B与G溶液反应的离子方程式:??
参考答案:(1) O2? Na2SO4? (2)
. .
本题解析:略
本题难度:简单
4、简答题 A~J是中学化学中常见的几种物质,它们之间的转化关系如图所示.已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F化合生成,J可作杀菌消毒剂.
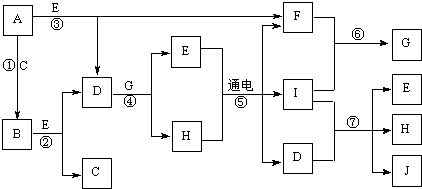
(1)写出B的电子式______.
(2)写出反应⑤的化学方程式:______.
(3)写出反应⑦的离子方程式:______.
(4)向AlCl3溶液中加入少量固体B,写出反应的化学方程式:______.
(5)以Pt为电极电解滴加有少量酚酞的H饱和溶液,则______极(填“阴”或“阳”)附近溶液先由无色变为红色,请说明理由:______.
参考答案:常温下A为固体单质,B为淡黄色粉末,C是气体,A和C反应生成B,则B是过氧化钠,A是钠,C是氧气;E在常温下为液体,E是水,钠和水反应生成 氢氧化钠和氢气,过氧化钠和水反应生成氢氧化钠和氧气,C是氧气,D是氢氧化钠,F是氢气;H的水溶液通电生成氢气、I气体和氢氧化钠,且J可作杀菌消毒剂,为次氯酸盐,所以I是氯气,电解饱和食盐水制取氯气,所以H是氯化钠,氢气和氯气反应生成G,所以G是氯化氢;氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,所以J是次氯酸钠.
(1)通过以上分析知,B是过氧化钠,电子式为
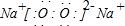
,故答案为:
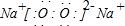
;
(2)电解饱和氯化钠溶液生成氯气、氢气和氢氧化钠,电解方程式为:2NaCl+2H2O?电解?.?2NaOH+Cl2↑+H2↑,
故答案为:2NaCl+2H2O?电解?.?2NaOH+Cl2↑+H2↑;
(3)氯气和强碱反应生成氯化物、次氯酸盐和水,离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(4)过氧化钠和水反应生成氢氧化钠和氧气,少量氢氧化钠和氯化铝反应生成氢氧化铝和氯化钠,反应方程式为:
6Na2O2+4AlCl3+6H2O=4Al(OH)3↓+12NaCl+3O2↑,故答案为:6Na2O2+4AlCl3+6H2O=4Al(OH)3↓+12NaCl+3O2↑;
(5)电解饱和氯化钠溶液时,阳极上氯离子放电生成氯气,在阴极氢离子不断放电,破坏了水的电离平衡,促使水继续电离,导致溶液中氢氧根离子浓度大于氢离子浓度,所以阴极附近溶液变红,
故答案为:阴;在阴极氢离子不断放电,破坏了水的电离平衡,促使水继续电离,导致溶液中氢氧根离子浓度大于氢离子浓度,所以阴极附近溶液变红.
本题解析:
本题难度:一般
5、选择题 下列反应现象“先变红后褪色”的是
A.SO2与紫色石蕊溶液
B.过量的Cl2与KI淀粉溶液
C.硫化氢与醋酸铅试纸
D.Na2O2与酚酞溶液
参考答案:D
本题解析:A中SO2与紫色石蕊溶液只变红。 B中过量的Cl2与KI淀粉溶液发生反应生成了碘单质,碘与淀粉变成了蓝色。C中硫化氢与醋酸铅试纸出现黑色。 D中Na2O2与酚酞溶液时,过氧化钠先和水反应生成过氧化氢和氢氧化钠,溶液呈碱性溶液变红,但过氧化氢有漂白性,红色又褪去。
本题难度:一般