微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 能促进水的电离,并使溶液中c(H+)>c(OH-)的操作是( )
①将水加热煮沸?
②向水中投入一小块金属钠?
③向水中通CO2④向水中通NH3?
⑤向水中加入明矾晶体?
⑥向水中加入NaHCO3固体
⑦向水中加NaHSO4固体.
A.①③⑥⑦
B.①③⑤⑥
C.⑤⑦
D.⑤
参考答案:①加热时能促进水的电离,但是c(H+)=c(OH-),溶液呈中性,故①错误;
②加入金属钠,和水电离出的氢离子反应生成氢氧化钠和氢气,从而促进水的电离,但溶液中c(H+)<c(OH-),故②错误;
③二氧化碳溶于水生成碳酸,溶液中的c(H+)>c(OH-),但酸对水的电离起抑制作用,故③错误;
④NH3?溶于水生成氨水,溶液中的c(H+)<c(OH-),导致溶液呈碱性,且氨水抑制水电离,故?④错误;?
⑤向水中加入明矾,铝离子水解对水的电离起促进作用,电离后的溶液显酸性,溶液中的c(H+)>c(OH-),故⑤正确;?
⑥向水中加入NaHCO3,碳酸氢钠中的碳酸氢根水解而使溶液显碱性,即溶液中的c(H+)<c(OH-),故⑥错误;
⑦向水中加NaHSO4固体,硫酸氢钠在水中完全电离出钠离子、氢离子、硫酸根离子,溶液中的c(H+)>c(OH-),但氢离子抑制水电离,故⑦错误,
故选D.
本题解析:
本题难度:简单
2、选择题 下列操作或反应所对应的图象正确的是
[? ]
A.将pH=5的醋酸释释1 000倍 
B.向1 L 0.1 mol/L的NH4Cl溶液中加入足量的Ba(OH)2溶液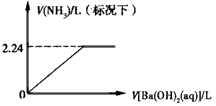
C.向1 L 0.1 mol/L的FeSO4溶液中加入足量的NaOH溶液? 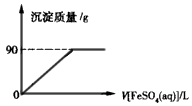
D.将CO通过灼热的CuO后气体的物质的量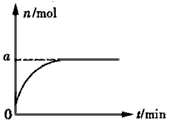 ?
?
参考答案:B
本题解析:
本题难度:一般
3、选择题 下列叙述正确的是( )
A、物质的量浓度相等的H2S和NaHS混合溶液中:
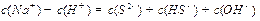
B、相同物质的量浓度的下列溶液中:① 、②
、②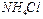 、③
、③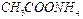 、
、
④
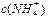 由大到小的顺序是:①>②>③>④
由大到小的顺序是:①>②>③>④
C、某二元酸(H2A)在水中的电离方程式是: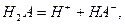
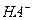
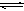
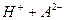 则在NaHA溶液中:
则在NaHA溶液中: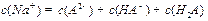
D、pH=12氨水溶液与pH=2盐酸溶液等体积混合:
参考答案:B
本题解析:略
本题难度:简单
4、选择题 下列表述或判断正确的是( )
A.25℃时,pH=10的NaOH溶液与pH=10的氨水中:c(Na+)=c(NH4+)
B.相同条件下等物质的量浓度的①NaCl?溶液;②NaOH溶液;③HCl溶液中由水电离出的c(H+):③>①>②
C.在Na2CO3、NaHCO3两种溶液中,离子种类不相同
D.25℃时,浓度为0.2?mol?L-1的Na2CO3溶液中只存在水解平衡,不存在电离平衡
参考答案:A.相同温度时,相同pH的氢氧化钠和氨水中都存在电荷守恒,c(Na+)+c(H+)=c(NH4+)+c(H+)=c(OH-),溶液的PH相等,则氢离子浓度相等,相同温度时两种溶液中氢氧根离子浓度相等,所以c(Na+)=c(NH4+),故A正确;
B.氢氧化钠和盐酸都抑制水电离,且氢氧化钠和氯化氢都是强电解质,所以等浓度的盐酸和氢氧化钠溶液抑制水电离程度相等,故B错误;
C.碳酸钠溶液中存在CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-,碳酸氢钠溶液中存在HCO3-+H2O?H2CO3+OH-、HCO3-?H++CO32-,只要是溶液中都含有氢离子,所以两种溶液中离子种类相同,故C错误;
D.碳酸钠溶液中水是弱电解质,存在电离平衡,碳酸根离子存在水解平衡,故D错误;
故选A.
本题解析:
本题难度:简单
5、选择题 下物质分类组合正确的是
?
| A
| B
| C
| D
|
强电解质
| HCl
| FeCl3
| H3PO4
| HClO
|
弱电解质
| HF
| CH3COOH
| BaSO4
| Ba(OH)2
|
非电解质
| NH3
| Cu
| H2O
| C2H5OH
|
?
参考答案:A
本题解析:根据电解质是在水溶液中或在熔融状态下就能够导电化合物,酸、碱、盐、活泼金属氧化物都是电解质;强电解质是指在水中完全电离成离子的化合物,包括强酸、强碱和活泼金属氧化物以及大部分盐;弱电解质是指在水中不完全电离,只有部分电离的化合物,包括弱酸、弱碱和水;在水溶液里和熔融状态下都不导电的化合物是非电解质,包括非金属氧化物、氨气、大多数有机物等;A、HCl在水中能完全电离,所以是强电解质;HF在水中只有部分电离,所以属于弱电解质;NH3是非电解质,故A正确;B、FeCl3在水中能完全电离,所以是强电解质;CH3COOH在水中只有部分电离,所以属于弱电解质;Cu是单质,既不是电解质也不是非电解质,故B错误;C、H3PO4在水中只有部分电离,所以属于弱电解质;BaSO4在水中溶解的部分能完全电离,所以属于强电解质;H2O是弱电解质,故C错误;D、HClO在水中只有部分电离,所以属于弱电解质;Ba(OH)2在水中能完全电离,所以属于强电解质;C2H5OH是非电解质,故D错误;故选:A。
本题难度:简单