微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用食用白醋(醋酸浓度约为1 mol/L)进行下列实验,能证明醋酸为弱电解质的是
A.白醋中滴入石蕊试液呈红色
B.白醋加入豆浆中有沉淀产生
C.蛋壳浸泡在白醋中有气体放出
D.pH试纸显示醋酸的pH为2~3
参考答案:D
本题解析:A.白醋中滴入石蕊试液呈红色,能证明白醋的溶液显酸性,但是不能证明是弱酸。错误。B.白醋加入豆浆中有沉淀产生,是因为白醋是酸,能使蛋白质变性而产生沉淀,与溶液的酸性强弱无关。错误。C.蛋壳浸泡在白醋中有气体放出,能证明酸性醋酸强于碳酸,但是也不能证明醋酸是弱酸。错误。白醋(醋酸浓度约为1 mol/L),若未强酸,则pH=0.但是测定溶液pH,试纸显示醋酸的pH为2~3,证明c(H+)<<c(HAc)。因此可以证明醋酸是弱酸。
本题难度:一般
2、选择题 下列判断正确的是
A.在水电离出来的c(H+)=1×10-13mol/L的溶液中Fe3+、NH4+、NO一定不能大量共存
B.AlCl3溶液蒸干后得到的固体是AlCl3
C.在0.1 mol/L CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
D.pH=3的醋酸溶液跟pH=11的氢氧化钡溶液等体积混合后,溶液pH=7
参考答案:C
本题解析:A、该溶液可能为酸性也可能为碱性,在酸性溶液中可以共存;
B、氯化铝在加热过程中,水解程度增大,且生产HCl挥发,故最终得到三氧化二铝;
C、该等式为质子守恒,正确;
D、醋酸为弱酸,混合后醋酸过量,溶液呈酸性。
本题难度:一般
3、选择题 已知某温度下,以下酸的电离常数如下:Ka(HCN)= 6.2×10-10 mol・L-1、Ka(HF)= 6.8×10-4 mol・L-1、Ka(CH3COOH)= 1.8×10-5 mol・L-1、、Ka(HNO2)= 6.4×10-6mol・L-1。物质的量浓度都为0.1 mol・L-1的下列溶液中,pH最小的是?
A.HCN
B.HF
C.CH3COOH
D.HNO2
参考答案:B
本题解析:弱酸的电离常数大小可以用来说明所对应的酸酸性强弱,电离常数越大,所对应的弱酸酸性相对较强,溶液中,pH最小即所对应的酸酸性最强的酸,即为HF,正确选项为B;
本题难度:一般
4、选择题 已知醋酸、醋酸根离子在溶液中存在下列平衡:
CH3COOH+H2O 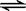 ?CH3COO―+H3O+? K1=1.75×10-5
?CH3COO―+H3O+? K1=1.75×10-5
CH3COO―+H2O 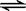 ?CH3COOH+OH―? K2=5.71×10-10
?CH3COOH+OH―? K2=5.71×10-10
现有50 mL 0.2 mol・L-1醋酸与50 mL 0.2 mol・L-1醋酸钠混合制得溶液甲,下列叙述正确的是
A.甲溶液的pH >7
B.对甲进行微热,K1、K2?同时增大
C.若在甲中加入很少量的NaOH溶液,溶液的pH几乎不变
D.若在甲中加入5 mL 0.1 mol・L-1的盐酸,则溶液中醋酸的K1会变大
参考答案:BC
本题解析:A、K1大于K2,所以混合溶液中以醋酸的电离为主,溶液为酸性,错误;?B、均为吸热反应,升高温度k值增大,正确;C、 若在甲中加入很少量的NaOH溶液,醋酸电离平衡正向移动,溶液的pH几乎不变,正确;D、温度不变,平衡常数不变,错误。
本题难度:一般
5、选择题 某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示。据图判断错误的是

A.a的数值一定大于9
B.I为氢氧化钠溶液稀释时溶液的pH变化曲线
C.完全中和稀释后相同体积的两溶液时,消耗相同浓度的稀硫酸的体积V( NaOH)<V(氨水)
D.稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大
参考答案:D
本题解析:根据题意知,一水合氨为弱电解质,氢氧化钠为强电解质,pH相同的氨水和氢氧化钠溶液,氨水的物质的量浓度大于氢氧化钠溶液;加水稀释相同的倍数,一水合氨的电离平衡正向移动,溶液的pH变化较小。B、根据题给图像可知,开始二者pH相同,在稀释过程中促进氨水的电离,则氨水的pH变化较小,即I为氢氧化钠溶液稀释时溶液的pH变化曲线,正确;C、根据题给图像可知,开始二者pH相同,一水合氨为弱电解质,氢氧化钠为强电解质,pH相同的氨水和氢氧化钠溶液,氨水的物质的量浓度大于氢氧化钠溶液;加水稀释相同的倍数,氨水的物质的量浓度仍较大,完全中和稀释后相同体积的两溶液时,消耗相同浓度的稀硫酸的体积V( NaOH)<V(氨水),正确;D、碱溶液分析水的电离即判断溶液中氢离子浓度大小,稀释后氨水的pH大于NaOH溶液的pH,稀释后氨水中水的电离程度比NaOH溶液中水的电离程度小,错误。
本题难度:一般