微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法不正确的是(? )
①钠、氢气都能在氯气中燃烧生成白色的烟雾
②铜丝在氯气中燃烧,生成蓝绿色的氯化铜
③液氯就是氯气的水溶液,它能使干燥的有色布条褪色
④久置的氯水,因氯气几乎完全挥发掉,剩下的就是水
A.只有①
B.①和②
C.①和④
D.①②③④
参考答案:D
本题解析:①钠在氯气中燃烧生成白色的烟;氢气在氯气中燃烧生成白色的雾。错误。②铜丝在氯气中燃烧,生成棕黄色烟。错误。③液氯就是液态的氯气,它不能使干燥的有色布条褪色。氯水是氯气的的水溶液,它能使干燥的有色布条褪色。错误。④氯水久置,因反应产生的次氯酸光照分解产生盐酸和氧气,氧气逸出,所以最后得到的是稀盐酸。错误。
本题难度:一般
2、选择题 下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是
[? ]
A.将NaHCO3固体加入新制的氯水中,有无色气泡(H+)
B.向FeCl2溶液中滴加新制氯水,再滴加KSCN溶液,发现呈红色(Cl2)
C.将AgNO3溶液滴加到新制氯水中,有白色沉淀产生(Cl-)
D.新制氯水使红色布条褪色(HCl)
参考答案:D
本题解析:
本题难度:简单
3、填空题 新制的氯水,呈浅黄绿色,说明氯水中含有?分子(填化学式);向新制氯水中,加入AgNO3溶液有白色沉淀产生,说明氯水中含?离子(填离子符号);向新制氯水中,放入一块有色布条,一段时间后取出,发现有色布条褪色,说明氯水具有?性。
参考答案:Cl2 Cl- 漂白
本题解析:新制的氯水,呈浅黄绿色,说明氯水中含有Cl2分子;向新制氯水中,加入AgNO3溶液有白色沉淀产生,说明氯水中含有Cl-离子;向新制氯水中,放入一块有色布条,一段时间后取出,发现有色布条褪色,说明氯水具有强氧化性。
点评:该题是基础性试题的考查,也是高考中的常见考点,侧重对基础性知识的巩固与训练。有利于引导学生注重教材基础知识,提高学生灵活运用基础知识解决实际问题的能力。
本题难度:一般
4、实验题 某化学小组用下列装置抽取收集纯净的氯气,并研究其性质。请回稳下列问题。
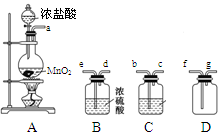
(1)装置A中发生反应的离子方程式为_______________________________。
(2)按照气流方向各仪器接口的连接顺序为a→___________________→g。
(3)装置B中浓硫酸的作用是____________________________________________________________,装置C的试剂最好是___________________________________。
(4)某同学认为上述方案缺少尾气吸收装置,请在下面的方框中画出该装置并注明试剂。
?
(5)装制取的氯气通入下图所示装置中,甲装置溶液中具有氧化性的含氯粒子是_______;如何证明乙装置中FeCl2溶液与Cl2发生了反应?(只回答需要的试剂和现象)___________________________。
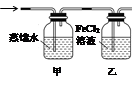
参考答案:(1)MnO2+4H++2Cl- Mn2++Cl2+2H2O(2分)?(2)bcedf(2分)
Mn2++Cl2+2H2O(2分)?(2)bcedf(2分)
(3)吸收水蒸气,干燥氯气(1分)?饱和食盐水(1分)?(4) (2分)
(2分)
(5)Cl2、HClO、ClO-(2分)? KSCN溶液(1分)?溶液变成红色(1分)
本题解析:(1)根据装置特点以及试剂可知,装置A是用来准备氯气的,所以A中发生反应的离子方程式为MnO2+4H++2Cl- Mn2++Cl2+2H2O。
Mn2++Cl2+2H2O。
(2)由于盐酸易挥发,所以生成的氯气中含有氯化氢以及水蒸气,因此在收集氯气之前需要首先除去氯化氢和水蒸气。首先除去的是氯化氢,所用试剂是饱和食盐水,然后在通过盛有浓硫酸的洗气瓶除去水蒸气。氯气的密度大于空气的,应该用向上排空气法收集,所以按照气流方向各仪器接口的连接顺序为a→b→c→e→d→f→g。
(3)根据以上分析可知,装置B中浓硫酸的作用是吸收水蒸气,干燥氯气;由于氯化氢极易溶于水,而氯气你溶于水,所以要除去氯气中的氯化氢气体最好选用饱和食盐水。
(4)氯气有毒,属于大气污染物,需要尾气处理。氯气能被氢氧化钠溶液吸收,所以可以用氢氧化钠溶液吸收,装置图为 。
。
(5)甲装置中盛有蒸馏水,氯气溶于水部分氯气与水反应生成盐酸和次氯酸,次氯酸是弱酸电离出氢离子和ClO-,所以甲装置溶液中具有氧化性的含氯粒子是Cl2、HClO、ClO-;氯气具有强氧化性,乙装置中盛有氯化亚铁溶液,能和氯气反应生成氯化铁。铁离子能和KSCN溶液反应而使溶液显红色,据此可以检验乙装置中FeCl2溶液与Cl2发生了反应。
本题难度:一般
5、选择题 向含有NaBr、KI的溶液中通入过量的Cl2,然后将溶液蒸干,并灼烧固体,最后得到的物质是(?)
A.KCl
B.NaCl和KCl
C.NaCl和KBr
D.NaCl、KCl和I2
参考答案:B
本题解析:通入过量Cl2,发生反应2NaBr+Cl2====2NaCl+Br2,2KI+Cl2====2KCl+I2,蒸干灼烧时Br2挥发,I2升华。
本题难度:简单