微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10分)甲醇(CH3OH)的用途广泛,摩托罗拉公司也开发出一种由甲醇、氧气以及强碱做电解质溶液的新型手机电池,容量达氢镍电池或锂电池的10倍,可连续使用一个月才充一次电.请完成下列与甲醇有关的问题.
(1)工业上用3克氢气与二氧化碳反应生成气态甲醇和水蒸气,放出24.5千焦的热量。
①请写出该反应的热化学反应方程式:?利用该反应,在温度和容积相同的A、B两个容器中,按不同方式投入反应物,保持恒温恒容,经10秒钟后达到平衡,达到平衡时的有关数据如下表:?
②从反应开始到达到平衡时,A中用CO2来表示的平均反应速率为?。
③A中达到平衡时CO2的转化率为?, B中a=?。
(2)某同学设计了一个甲醇燃料电池,其装置如图:
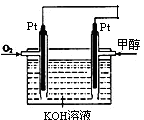
①写出图中通入甲醇这一极的电极反应式?。
②反应一段时间后,正极附近的碱性?(增强。减弱?不变)
参考答案:(1)①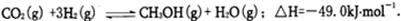 ? (2分)
? (2分)
② 0.1c1 mol/(L・s) 或0.1c2 mol/(L・S)(任答对一个得分)(1分)
③ 60%? (2分)?19.6(2分)
(2)① CH3OH - 6e-+ 8OH- = CO32-+ 6H2O? (2分)?② 增强(1分)
本题解析:(1)①考查热化学方程式的书写②甲醇的浓度变化未c1,则根据方程式可知,CO2的浓度变化也是c1,所以反应速率为0.1c1 mol/(L・s)。放出的热量是29.4kJ,所以消耗的CO2是 ,所以转化率是60%。根据反应物投入量可知A和B是等效的,所以B中吸收的热量是49kJ-29.4kJ=19.6kJ。
,所以转化率是60%。根据反应物投入量可知A和B是等效的,所以B中吸收的热量是49kJ-29.4kJ=19.6kJ。
(3)甲醇失去电子,发生氧化反应,在负极通入。氧气在正极通入,得到电子发生还原反应,生成OH-,所以正极周围碱性增强。
本题难度:一般
2、计算题 某温度下N2O4和NO2之间建立起如下的平衡N2O4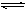 2NO2,测得平衡混合物对空气的相对密度为2.644,求N2O4的分解率。
2NO2,测得平衡混合物对空气的相对密度为2.644,求N2O4的分解率。
参考答案:N2O4的分解率为20%。
本题解析:设N2O4的起始物质的量为1
转化了的N2O4物质的量为x
?N2O4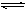 2NO2
2NO2
起始物质的量?1?0
转化物质的量?x?2x
平衡物质的量?1-x?2x
平衡时混合气体的总物质的量为
n总=1-x+2x=1+x
∵ =29・D=29×2.644=76.68
=29・D=29×2.644=76.68
已知N2O4和NO2的相对分子质量分别为92,46,则有:
76.68=(92×(1-x)+46×2x/1+x)
解得x=0.2mol
∴N2O4的分解率为:(0.2/1)×100%=20%
本题难度:简单
3、填空题 在T℃条件下,向1L固定体积的密闭容器M中加入2?mol?X和1?mol?Y,发生如下反应:? 2X(g)?+?Y(g)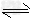 a?Z(g)?+?W(g)?△H?=?-Q?kJ・mol-1?(Q>0) 当反应达到平衡后,反应放出的热量为Q1?kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则:
a?Z(g)?+?W(g)?△H?=?-Q?kJ・mol-1?(Q>0) 当反应达到平衡后,反应放出的热量为Q1?kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则:
(1)化学计量数a的值为?____________?。此反应的逆反应△S ___________( “<”、“>”或“=”)0。
(2)下列说法中能说明该反应达到了化学平衡状态的是_____________。
A.容器内压强一定?
B.容器内气体的密度一定
C.容器内Z分子数一定?
D.容器内气体的质量一定
(3)维持温度不变,若起始时向容器中加入的物质的量如下列各项,则反应达到平衡后放出的热量仍为Q1?kJ的是________?(稀有气体不参与反应)与之是等效平衡的是_____ 。
A.2?molX、1mol?Y、1molAr? ?
B.a?molZ、1mol?W ?
C.1?molX、0.5mol?Y、0.5a?molZ、0.5?mol?W? ?
D.2?molX、1mol?Y、1molZ
(4)维持温度不变,若起始时向容器中加入4mol?X和6mol Y,若达到平衡时容器内的压强减小了15%,则反应中放出的热量为___________kJ。
(5)维持T℃条件不变,若在一个和原容器体积相等的恒压容器N中,加入2?mol?X和1mol?Y发生如上反应并达到平衡,则____________(选填M或N)容器中的反应先达到平衡状态,容器中X的质量分数:M___________(选填“>”、“<”或“=”)N。
(6)已知:该反应的平衡常数随温度的变化如下表:若在某温度下,2?molX和1?mol?Y在该容器中反应达到平衡,?X的平衡转化率为50%,则该温度为_____________℃。

参考答案:(1)1?;>
(2)ABC
(3)A ;ABC
(4)1. 5Q
(5)N?;?>
(6)300
本题解析:
本题难度:一般
4、选择题 A、B混合气体在密闭容器中发生如下反应: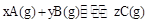 ?
?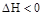 ,达到化学平衡后测得A气体的浓度为
,达到化学平衡后测得A气体的浓度为 ;当恒温下将密闭容器的容积扩大一倍并再次达到平衡时,测得A气体的浓度为
;当恒温下将密闭容器的容积扩大一倍并再次达到平衡时,测得A气体的浓度为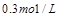 。则下列叙述正确的是(?)
。则下列叙述正确的是(?)
A.平衡向右移动?B.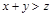 ?
?
C.B的转化率提高?D.C的体积分数增加
参考答案:B
本题解析:假设平衡不发生移动,当恒温下将密闭容器的容积扩大一倍,则A气体的浓度应该为以前的一半,为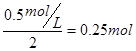 ,但是现在A气体的浓度为
,但是现在A气体的浓度为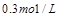 ,经过对比可以确定平衡向作移动,即当容积扩大一倍时平衡向左移动;容积扩大一倍相当于降低压强,所以可以得到降低压强平衡向左移动,又降低压强平衡向气体体积增大的方向进行,所以
,经过对比可以确定平衡向作移动,即当容积扩大一倍时平衡向左移动;容积扩大一倍相当于降低压强,所以可以得到降低压强平衡向左移动,又降低压强平衡向气体体积增大的方向进行,所以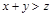 ,B正确;平衡向左移动B的转化率降低,C的体积分数减小,所以答案选B。
,B正确;平衡向左移动B的转化率降低,C的体积分数减小,所以答案选B。
本题难度:一般
5、选择题 已知反应:2CH3COCH3(l)  CH3COCH2COH(CH3)?2(l)。?取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如下图所示。下列说法正确的是
CH3COCH2COH(CH3)?2(l)。?取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如下图所示。下列说法正确的是

A.b代表0℃下CH3COCH3的Y-t曲线
B.反应进行到20min末,H3COCH3的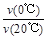 >1
>1
C.升高温度可缩短反应达平衡的时间并能提高平衡转化率
D.从Y=0到Y=0.113,CH3COCH2COH(CH3)2的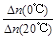 =1
=1
参考答案:D
本题解析:b曲线达到平衡需要的时间少,b温度高,应代表20℃下CH3COCH3的Y-t曲线,A错误;温度越高,反应速率越快,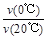 <1,B错误;由图像可知温度越高,反应物转化率越小,说明正反应是放热反应,所以升高温度可缩短达到平衡所需的时间但反应物转化率降低,C错误;从Y=0到Y=0.113转化的CH3COCH3相同,生成的CH3COCH2COH(CH3)2也相同,D正确。
<1,B错误;由图像可知温度越高,反应物转化率越小,说明正反应是放热反应,所以升高温度可缩短达到平衡所需的时间但反应物转化率降低,C错误;从Y=0到Y=0.113转化的CH3COCH3相同,生成的CH3COCH2COH(CH3)2也相同,D正确。
点评:从图像中挖掘出隐含信息。
本题难度:一般