��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ij�о���ѧϰС��ѧϰ�˹�ҵ�������Ƽ����ԭ����
[�������]�ܷ���ʵ����ģ�⡰�����Ƽ������ȡNaHCO3�Ĺ����أ�
[ʵ��ԭ��]д�������Ƽ��Ӧ�Ļ�ѧ����ʽΪ______��[ʵ����֤]��ͼ�Ǹ�ѧϰС�����ģ��ʵ��ʱ���õ��IJ�����Ҫװ�ã�
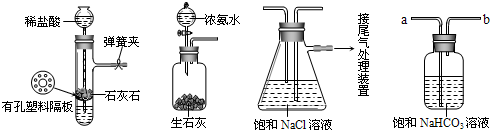
��ش��������⣺
��1������Aװ�������Եķ����ǣ�����������©�����������н����ɼк�©��ע��һ������ˮ��ʹ©���ڵ�ˮ������Թ��ڵ�ˮ�棬ֹͣ��ˮ����______��˵��װ�ò�©����
��2��D��������װ��A��װ��C֮������徻��װ�ã���������______����a��b����D�������dz�ȥ______���壮�ɷ�ƿ���Լ���Ϊ̼������Һ______����ɡ�������
��3��ʵ��ʱ����NaCl��Һ��ͨ��϶��______����ͨ��������______����ԭ����______������д��ţ�
��ʹCO2���ױ�����?��NH3��CO2������ȡ?��CO2���ܶȱ�NH3��
��4����______�ķ��������ɵ�NaHCO3����ӻ�����з��������
���Ҫ�Ƶô�����跢���ķ�Ӧ�ǣ�д����Ӧ�Ļ�ѧ����ʽ����______��
[�ó�����]���á������Ƽ����ʵ���ҿ�����ȡNaHCO3��
�ο��𰸣������Ƽ���ö�����̼ͨ�백���ı����Ȼ�����Һ�з�Ӧ����̼�����ƾ��壬��Ӧ�Ļ�ѧ����ʽ��NaCl+NH3+CO2+H2O=NaHCO3��+NH4Cl��
�ʴ�Ϊ��NaCl+NH3+CO2+H2O=NaHCO3��+NH4Cl
��1����ˮ��ע����ڼ�ѹ����©����Һ�岻���������Թܣ�ʹ����©�������Һ�����Һ������Һ���ֲ��䣬˵��װ�����������ã�
�ʴ�Ϊ������©����ע��ˮ��©�������Թ��е�Һ��ˮ�����ֲ��ٱ仯��©���е�Һ��ˮ���治���½���
��2�������a��ͨ��ʱ����ʹ����ͨ����Һ���ﵽ���������Ŀ�ģ�װ��D��ʢ�ŵ�̼��������Һ������������е�HCl������Ӧ�����Ȼ��ơ�ˮ�Ͷ�����̼���Ӷ���ȥ���������е�HCl��������̼������Һ��������̼Ҳ�ᱻ���գ�
�ʴ�Ϊ��a���Ȼ��⣨��HCl������
��3����ͨ�백����������ˮ�γɳʼ��Եİ�ˮ���������̼��ˮ���ɵ�̼�ᷢ����Ӧ���������ڶ�����̼��������գ�
�ʴ�Ϊ��NH3��CO2���٣�
��4��ͨ�����ˣ��ɰѻ�����Һ�е�̼�����ƾ���������������Ƶô�����Ҫ��̼�����ƹ�����ȷֽ�õ�����Ӧ��ѧ����ʽΪ��2NaHCO3?��?.?Na2CO3+H2O+CO2��
�ʴ�Ϊ�����ˣ�2NaHCO3?��?.?Na2CO3+H2O+CO2��
���������
�����Ѷȣ�һ��
2������� ��ҵ���Դ�ʳ�Σ���������Ca2+��Mg2+���ʣ�������ʯ��ʯ��Ϊԭ�ϣ������Ʊ�Na2CO3�����������ͼ��ʾ��
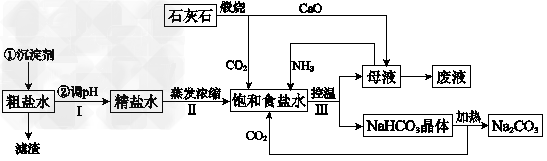
��ش� ?
��1���ڴ�������ˮ�Ĺ����У��ɼ���ʯ����ʹ�����Ϊ�������������������ijɷֳ������ij��������_____________�� ?
��2����CaOͶ�뺬�д�����NH4Cl��ĸҺ�У������ɿ�ѭ��ʹ�õ�NH3���÷�Ӧ�Ļ�ѧ����ʽ��_________________�� ?
��3����ʳ��ˮ������ͨ���������______�����̢�������NaHCO3����ķ�Ӧ�Ļ�ѧ����ʽ��__________________��
��4��̼���ƾ���ʧˮ�������仯ʾ��ͼ���£�?
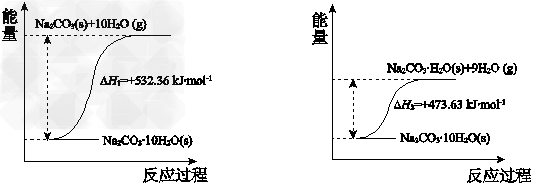
Na2CO3��H2O(s)?��ˮ��Ӧ���Ȼ�ѧ����ʽ��___________�� ?
��5����Ʒ�����г�����NaCl��ȡa?g�����������ϡ�����ַ�Ӧ�����ȡ����ɡ����գ���b?g���塣��ò�Ʒ��Na2CO3������������__________�� ?
��6������Na2CO3��������--����ȼ�ϵ�صĵ���ʣ��õ�ظ����ķ�Ӧʽ��________________________��
�ο��𰸣���1��CaCO3��Mg(OH)2
��2��2NH4Cl+CaO=CaCl2+2NH3��+H2O
��3��NH3��NH3+H2O+CO2+NaCl=NaHCO3��+NH4Cl
��4��Na2CO3��H2O(s)=Na2CO3(s)+H2O(g) ��H=+58.73kJ/mol
��5��106(b��a)/11a
��6��CH4��8e��+4CO32��=5CO2+2H2O
���������
�����Ѷȣ�һ��
3������� ��ʳ��Ϊԭ�Ͻ����������ۺ����õ�ijЩ��������ͼ��ʾ��
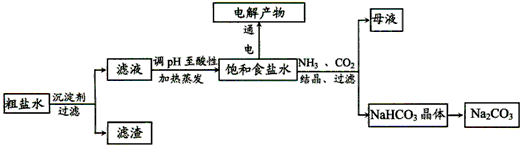
��1����ȥ�����е�Ca2+��Mg2+��SO42-���ӣ��������г�������˳���ǣ�����ţ�_________��
a��Na2CO3 b��NaOH c��BaCl2
��2������Һ��pH�������Գ�ȥ��������_________��
��3����ⱥ��ʳ��ˮ��Ӧ�����ӷ���ʽ��_________��
��4����������NaHCO3������ĸҺ�м��������ʯ�ң���ɻ��һ�ֿ���ѭ��ʹ�õ����ʣ��仯ѧʽ��_________��
��5�������������������й㷺��Ӧ�á�
�� ��������ڳ���̨���ۡ���ԭ���ǣ�������ӷ���ʽ������__________________��
�� �����£���ijpH=11��Na2CO3��Һ�м������ʯ���飬���˺�������ҺpH=13����Ӧǰ����Һ���뷴Ӧ�����Һ��ˮ�������c��OH-���ı�ֵ��_________��
�� ��ҵ�ϣ������ô�������ռ�����ijЩ������Ʒ�����ñ��ʹ�����Һ��Cl2��Ӧ��ȡ��Ч�ɷ�ΪNaClO������Һ���䷴Ӧ�����ӷ���ʽ��__________________������֪̼�������ǿ�ڴ����ᣩ��
�ο��𰸣���1��cab����cba����bca
��2��CO32-��OH-
��3��2Cl- + 2H2O 2OH-+ H2�� + Cl2��
2OH-+ H2�� + Cl2��
��4��NH3
��5����CO32-ˮ���Լ���CO32-+ H2O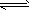 HCO3-+ OH-�������ڼ���������ˮ�⣬�ﵽȥ��Ŀ�ģ�
HCO3-+ OH-�������ڼ���������ˮ�⣬�ﵽȥ��Ŀ�ģ�
��1��1010����2CO32-+ Cl2+H2O��Cl-+ClO-+2HCO3-
���������
�����Ѷȣ�һ��
4������� �ҹ�����ר�Һ�°�ġ������Ƽ����Ϊ�����Ƽҵ������ͻ�����ף�����NaCl��NH3��CO2��Ϊԭ�����Ƶ�NaHCO3����������������йط�Ӧ�Ļ�ѧ����ʽΪ��
NH3+CO2+H2O=NH4HCO3��
NH4HCO3+NaCl=NaHCO3��+NH4Cl��
2NaHCO3?
Na2CO3+CO2��+H2O
��1��̼������뱥��ʳ��ˮ��Ӧ��������̼�����ƾ����ԭ����______
a��̼������������ˮ
b��̼�����������ֽ�
c��̼�����Ƶ��ܽ����Խ�С����������Һ�����Ƚᾧ����
��2��ij̽���С����������Ƽ�ԭ��������̼�����Ƶ��Ʊ�ʵ�飬ͬѧ�ǰ�������Ƶķ���ʵ�飮
��һλͬѧ��������̼����ͨ�뺬���ı���ʳ��ˮ���Ʊ�̼�����ƣ�ʵ��װ������ͼ��ʾ��ͼ�мг֡��̶��õ�����δ��������
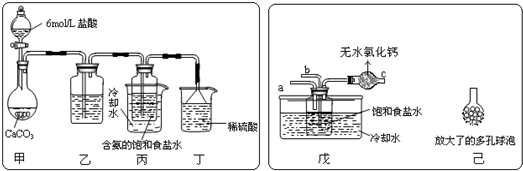
�Իش������й����⣺
������װ���е��Լ���______��
����װ����ϡ�����������______��
����ʵ����������NaHCO3?����IJ�����______���������������ƣ���
����һλͬѧ��ͼ����װ�ã�����װ��δ����������ʵ�飮
����ʵ��ʱ�����ȴ�______��ͨ��______?���壬�ٴ�______����ͨ��______���壻
������ͬѧ��������װ�õ�b���¶����Ӽ�װ�ã�������______��
��3��������д��һ��ʵ������ȡ����̼�����Ƶķ�����______��
�ο��𰸣���1��a��̼������������ˮ����A����
b��̼�����������ֽ⣬��������Һ�����Ƚᾧ�����أ���B����
c��̼�����Ƶ��ܽ��������Ȼ����˵̼�����Ƶ��ܽ�ȸ�СһЩ����������Һ�����Ƚᾧ��������C��ȷ��
��ѡC��
��2���٣�I������������ȡ������̼ʱ���������ӷ������ԣ�������̼�г��Ậ���Ȼ������壬̼�������������ᷴӦ���������̼��Ӧ������ͨ��̼�����Ƶ���Һ�ǿ��Գ���������̼�����е��Ȼ������壬�ʴ�Ϊ������̼��������Һ��
��II��ʵ������а���������ʣ�࣬��ϡ�������백����Ӧ������ϡ���������������ĩ��Ӧ��NH3���ʴ�Ϊ������δ��Ӧ��NH3��
��III�������NaHCO3����IJ����Ƿ��������Һ�壬�����õ�ʵ������ǹ��˲������ʴ�Ϊ�����ˣ�
�ڣ�I����ȡ̼������ʱ��Ҫ�õ������ı���ʳ��ˮ��������������ˮ��������̼������ˮ������Ӧ��ͨ�백��������a��ͨ�룬�Ӷ���֤�˴�bͨ�������̼ʱ��������̼����ַ�Ӧ���ʴ�Ϊ��a��NH3��b��CO2��
��II��װ�øĶ���Ӧ��Ķ�����̼����Һ�ĽӴ�����������˶�����̼�������ʣ��ʴ�Ϊ��������������Һ�Ӵ���������CO2�����ʣ�
��3���������ϢNH4HCO3+NaCl�TNaHCO3��+NH4Cl���ɵ���ȡ̼�����Ƶķ�����ͬʱҲ�ɲ����ռ���Һ��ͨ�����CO2��������Na2CO3 ��Һ��ͨ�����CO2 �ȵõ�̼�����ƣ�
�ʴ�Ϊ����̼���������������ʳ��ˮ��Ӧ�������ռ���Һ��ͨ�����CO2����������Na2CO3?��Һ��ͨ�����CO2?�ȣ�
���������
�����Ѷȣ�һ��
5������� ��ҵ��������Ĺ�������ʾ��ͼ����

���������գ�
��1������ˮ���������A��B�����ʣ�������A��Դ��ʯ��Ҥ������д��A��B�Ļ�ѧʽ��
A_________B_________
��2��ʵ�����ᴿ���ε�ʵ���������Ϊ��ȡ����_________��������_________��_________����ȴ�ᾧ��_________����ɡ�
��3����ҵ��������������У�̼�ữʱ������������__________________��̼�ữʱû������̼���ƾ��壬��ԭ����__________________��
��4��̼�ữ����ˣ���ҺD����Ҫ�ijɷ���_________����д��ѧʽ����������һ�ɷֵ������ӵľ��巽���ǣ�__________________��
��5����������а���ѭ��ʹ�õģ�Ϊ�ˣ���ҺD����ʯ��ˮ����������ʯ��ˮ���������ķ�Ӧ�����ӷ���ʽΪ��__________________��ҺD��ʯ��ˮǰ��Ҫ���ȣ�ԭ����__________________��
��6����Ʒ�����к���̼�����ơ�����ü��ȷֽ�ķ����ⶨ������̼�����Ƶ�����������������̼�����Ƶ����������ɱ�ʾΪ��__________________��ע����ı���ʽ�����õ��йط��ŵĺ��壩
�ο��𰸣���1��Ca(OH)2��CaO��Na2CO3
��2���ܽ⣻���ˣ�����������
��3���о�������������ֻ��ǣ���̼�����ܽ�ȱ�̼�����ƴ�
��4��NH4Cl��ȡ�����������ữ�������������а�ɫ����������������������
��5��NH4++OH-==NH3��+H2O����ֹ��ʯ��ˮʱ����̼��Ƴ���
��6��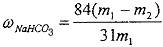 ��m1������ǰ�����������m2�����Ⱥ��������
��m1������ǰ�����������m2�����Ⱥ��������
���������
�����Ѷȣ�����