微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将标准状况下NO2和O2按体积比4∶1混合后充入一干燥烧瓶中,把烧瓶倒置于水中,烧瓶内液体逐渐上升,若不考虑烧瓶内溶液不扩散,最终烧瓶内溶液溶质的物质的量浓度为?( ? )
A.mol・L-1
B.× mol・L-1
C.× mol・L-1
D.mol・L-1
参考答案:C
本题解析:4NO2+O2+2H2O=4来源:91考试网 91exam.orgHNO3?设烧瓶体积是V,那么NO2的体积是4V/5,物质的量为
V×,生成的硝酸的物质的量和NO2相同,最终烧瓶中的溶液是HNO3,物质的量浓度为物质的量除以烧瓶的体积,所以应该是× mol・L-1,故选C。
本题难度:一般
2、选择题 为了测定某铜银合金的成分。将30.0g合金完全溶于80ml 13.5mol/L的浓HNO3中,待合金完全溶解后,收集到NO和NO2的混合气体共6.72L(标准状况),并测得溶液中氢离子浓度为1mol/L。假设反应后溶液的体积仍为80ml。试计算:
(1)被还原的硝酸的物质的量。
(2)合金中银的质量分数。
参考答案:(1)0.3mol?(2)36%
本题解析:略
本题难度:简单
3、选择题 在某100 mL混合溶液中,HNO3和H2SO4的物质的量浓度分别为0.400 mol・L-1和0.100 mol・L-1,向该混合溶液中加入1.92 g铜粉,加热使其充分反应,若反应前后溶液体积视作不变,反应后溶液中Cu2+的物质的量浓度为(?)
A.0.15 mol・L-1
B.0.225 mol・L-1
C.0.3 mol・L-1
D.0.6 mol・L-1
参考答案:B
本题解析:溶液中n(H+)="0.1" L×0.4 mol・L-1+0.1 L×0.1 mol・L-1×2="0.06" mol
n(Cu)=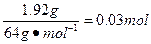
n(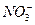 )="0.1" L×0.4 mol・L-1="0.04" mol
)="0.1" L×0.4 mol・L-1="0.04" mol
3Cu? +? 8H++? 2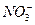 ====3Cu2++2NO↑+4H2O
====3Cu2++2NO↑+4H2O
0.03 mol? 0.06 mol? 0.04 mol
因n(H+)不足,故只消耗Cu: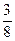 ×0.06="0.0225" mol
×0.06="0.0225" mol
c(Cu2+)=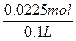 ="0.225" mol・L-1
="0.225" mol・L-1
本题难度:简单
4、选择题 分别向含下列物质的溶液中滴加过量氨水,先有沉淀生成,后沉淀不溶解的是:
A.AlCl3溶液
B.AgNO3溶液
C.CuSO4溶液
D.ZnCl2溶液
参考答案:A
本题解析:A正确,氢氧化铝不溶于弱碱;B错,氢氧化银沉淀还能与氨水继续反应生成银氨溶液;C错,生成的氢氧化铜会继续与氨水反应生成铜氨络离子;D错,生成的氢氧化锌沉淀会继续与氨水反应生成锌氨溶液;
本题难度:一般
5、选择题 在一定条件下,将m体积NO和n体积 同时通入倒立于水中且盛满水的容器内,充分反应后,容器内残留
同时通入倒立于水中且盛满水的容器内,充分反应后,容器内残留 体积的气体,该气体与空气接触变为红棕色,则m与n的比值为:()
体积的气体,该气体与空气接触变为红棕色,则m与n的比值为:()
A.3∶2
B.2∶3
C.8∶3
D.3∶8
参考答案:C
本题解析:电子守恒法

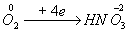
 即得m∶n=8∶3
即得m∶n=8∶3
本题难度:简单