ϴ��
�ο��𰸣�BC
���������B���ϩ�����Ը��������Һ������CO2�����ʶ��������µ����ʣ��ʴ���C���������������������Һ������Ӧ���ʴ�����ѡBC��
������������Ҫ��Ҫ���������ʵij��ӣ�ץס����������Ҫ���������������ټ�����Լ�ֻ�������ʷ�Ӧ��������ԭ���ʷ�Ӧ���ڷ�Ӧ���������µ������ǽ���Ĺؼ���
�����Ѷȣ���
3��ʵ���� ����ͭ��һ��Ӧ�ù㷺�Ļ���ԭ�ϣ�ʵ�����п�ͨ����ͬ;����ȡ����ͭ��Һ�͵���(CuSO4��5H2O)������һ���������£�
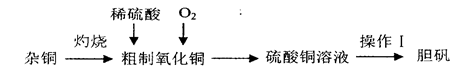
(1)����I����Ϊ__________��___________�����ˡ���ɡ�
(2)��ͭ(�������л���)���պ�IJ��������ͭ��������ͭ��ԭ�������___________(����ĸ����)��
a�����չ����в�������ͭ����ԭ
b�����ղ���֣�ͭδ����ȫ����
c������ͭ�ڼ��ȹ����зֽ�����ͭ
d����������ͭ������������
(3)������ͭ��Ϊ������ͭ�ۣ���ֱ�������м���ϡ�����Fe2(SO4)3��Һ������ͨ����������Ӧ��ȫ�������м������_______________(�ѧʽ����ͬ)������pH��4������_________���������˵�����ͭ��Һ����֪Fe(OH)3��Cu(OH)2��ȫ����ʱ��pH�ֱ�Ϊ3��7��6��4]��
��4)ͨ������ͼ1װ��Ҳ����ȡ����ͭ��Һ(��֪��2NaOH+2NO2��NaNO3+NaNO2+H2O)��

��ƿ�ڷ�����Ӧ�����ӷ���ʽΪ____________________________________________��
ͼ2��ͼ1�ĸĽ�װ�ã����ŵ��Т�__________________________����_________________________��
�ο��𰸣���16�֣���1������Ũ����2�֣�����ȴ�ᾧ��2�֣� ��2��ab��2�֣�ѡ��1��1�֣��д��÷֣�
��3��CuO��2�֣�����������Ҳ�ɣ� Fe(OH)3(2��)
��4��Cu��4H����2NO3����Cu2����2H2O��2NO2����3Cu��8H����2NO3����3Cu2����4H2O��2NO����2�֣�д��1������2�֣� �ٷ�ֹNaOH��Һ�������뷢��װ�ã�2�֣� ��NO��NO2�ж������ܱ���ȫ���գ�2�֣�
�����������1������ͭ������ˮ�����Դ�����ͭ��Һ�еõ�����ͭ����ò���Ӧ��������Ũ������ȴ�ᾧ��Ȼ����˺�ɼ��ɡ�
��2�����պ�IJ��������ͭ��������ͭ����˵��a�����չ����в�������ͭ����ԭ��a��ȷ��b�����ղ���֣�ͭδ����ȫ������b��ȷ��c������ͭ�ȶ����ڼ��ȹ����в����ֽܷ�����ͭ��c����ȷ��d��ͭ���ױ�������������ͭ��d����ȷ����ѡab��
��3�����ڷ�Ӧ�в����������µ����ʣ�����Ҫ������Һ��pHС�ڽ�������ͭ��������ͭ��������������������pHС��������ͭ������pH�������������������������������˵�����ͭ��Һ��
��4���������ǿ�����ԣ��ܰ�ͭ������������ͭ�������ŷ�Ӧ�Ľ��У�����Ũ�����ͣ��仹ԭ���ォ��ΪNO������йط�Ӧ�Ļ�ѧ����ʽ��Cu��4H����2NO3����Cu2����2H2O��2NO2����3Cu��8H����2NO3����3Cu2����4H2O��2NO��������NO2������������Һ��Ӧʱ����Һ����������NO������������Һ����Ӧ������ɻ�����Ⱦ������ͼ2��ͨ��������������NO������ȫ���գ���װ��2���ŵ��Ǣٷ�ֹNaOH��Һ�������뷢��װ�ã���NO��NO2�ж������ܱ���ȫ���ա�
�����Ѷȣ�һ��
4��ʵ���� ��ͼ��һ����ȡ����֤�������ֻ�ѧ���ʵ�ʵ��װ�á�

�ش��������⣺��Ӧ�ķ���ʽ��MnO2+4HCl��Ũ�� MnCl2+2H2O+ Cl2�� MnCl2+2H2O+ Cl2��
(1)װ��A�У�����aʢ�е��Լ�Ϊ__?__��
(2)��Cl2����ͨ��һ��ʱ���װ��B����Һ��pHֵ____7(���������������)��д��Cl2��ˮ��Ӧ�ķ���ʽ?
(3)��������Cl2����ͨ���۲쵽װ��C�е���Һ��Ϊ_?___ɫ��
(4)��Cl2��������ͨ��ʱ��װ��D�и������ɫ�����ܷ���ɫ��Ϊʲô��
____?________��
(5)װ��E��������_____?___����д���÷�Ӧ�Ļ�ѧ����ʽ��?��
��6��д��������ʯ������ȡƯ�۵Ļ�ѧ����ʽ�� ______?______��
�ο��𰸣�(1)Ũ����
(2) ��?Cl2+H2O�PHCl+HClO
(3)��ɫ
(4)�ܣ���Ϊʪ���������Ư����
(5) ���ն��������? Cl2+2NaOH===NaCl+NaClO+H2O
��6��2Cl2+2Ca(OH)2====CaCl2+Ca(ClO)2+2H2O
���������������������ȡ������
��1����Ӧԭ��Ϊ��MnO2��4HCl(Ũ)=MnCl2��Cl2����2H2O���ʷ�Һ©����װ����Ũ����
��2�����ڷ�ӦCl2+H2O�PHCl+HClO�������ᣬ����Һ�����ԣ�pH<7
��3�����ڷ�Ӧ���ɵⵥ�ʣ�Cl2��2I��=2Cl����I2��ʹ���۳���ɫ
��4����������Ϊʪ��ģ����д��������ɣ�����Ư���ԣ��������ɫ��������ɫ.
��5�������ж���һ���ü�Һ���գ�Cl2+2NaOH===NaCl+NaClO+H2O
��6��2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O
�����Ѷȣ�һ��
5�������� ʵ����Ҫ��4 mol��L-1��Ũ��������500 mL 0.2 mol��L-1��ϡH2SO4��Һ��
��1��.ʵ���������õ�����Ҫ���������У���Ͳ���ձ�����������??�� ?�ȡ�
��2��.����Ũ��Ϊ4mol/L��Ũ��������Ϊ����mL��
��3��.ȡ20 mL��ϡ��Һ��Ȼ�����������п���������ɵ��������������£���
�ο��𰸣���1��500ml ����ƿ?�ι�?��2��0.025L?��3��0.896L
�����������1����Ũ��������500mlϡ���ᣬ����Ҫ����������Ͳ���ձ������������Ҫ500ml����ƿ�Ͷ���ʱ�Ľ�ͷ�ιܡ�
��2������C1V1 = C2V2
?��0.5��0.2 ��4��V2
?��� V2��0.025��L��
��3�� Zn? +? H2SO4 ?��? ZnSO4?+? H2 ��
1 mol?22.4L
0.02L��0.2mol/L? VL
��� V��0.896L
�����������ǻ���������Ŀ��飬����ע�ػ������������У�����������ѧ���Ĺ淶�������������ѧ������˼ά���������Ӧ�������������ѶȲ���ѧ�����ѵ÷֡�
�����Ѷȣ�һ��
|