微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 利用图所示装置收集以下6种气体(图中烧瓶的位置不得变化)。 ①H2②Cl2 ③CH4 ④HCl ⑤NH3⑥SO2 若烧瓶是干燥的,则由A口进气,可收集的气体有(写序号); ____? ;
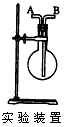
2、选择题 在氯气的制备实验中,有位同学设计了如图所示的制备装置,其中分液漏斗与烧瓶瓶塞之间连接一段橡胶管和玻璃管。下列对其作用的叙述中正确的是(? )

A.防止氯气造成大气污染
B.使反应的氯气循环使用
C.使烧瓶内的压强与大气压保持一致
D.使分液漏斗中的液体更容易注入烧瓶
3、选择题 下列实验方案合理的是(?)?
A.向溴乙烷中滴加硝酸银溶液和稀硝酸时,有淡黄色沉淀产生
B.配制Cu(OH)2悬浊液:在一定量CuSO4溶液中,加入少量NaOH溶液
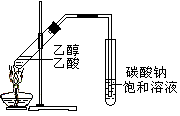
C.制备乙酸乙酯:用右图所示的实验装置
D.鉴别环己烯和苯:将溴的四氯化碳溶液分别滴加到少量环己烯和苯中
4、实验题 加碘食盐中加入的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至560℃开始分解。在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应。
【问题1】工业生产碘酸钾的流程如下:?

(1)已知步骤①反应器发生的反应中,生成的两种还原产物所得电子数相同。请写出反应器中发生反应的化学方程式: ? 。
(2)参照下表碘酸钾的溶解度,操作③得到碘酸钾晶体,你建议的方法是 ? 。
温度/℃
| 20
| 40
| 60
| 80
|
KIO3g/100g水
| 8.08
| 12.6
| 18.3
| 24.8
|
【问题2】已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;? I2+2S2O32-=2I-+S4O62-。
(1)检验加碘食盐中的碘元素,学生甲利用碘酸钾与碘化钾在酸性条件下发生反应。用四氯化碳检验碘单质时,看到的明显现象有? ?。
(2)测定加碘食盐中碘的含量,学生乙设计的实验步骤如下:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol/L的Na2S2O3溶液10.0mL
恰好反应完全。则加碘食盐样品中的碘元素含量是?mg/kg(以含w的代数式表示)。
(3)学生丙又对纯净的NaCl(不含KIO3)进行了下列实验:
操作步骤
| 实验现象
|
取1g纯净的NaCl,加3mL水配成溶液。
| 溶液无变化
|
滴入5滴淀粉溶液和1mL 0.1mol/L KI溶液,振荡。
| 溶液无变化
|
然后再滴入1滴1mol/L的H2SO4,振荡。
| 溶液变蓝色
|
①请推测实验中产生蓝色现象的可能原因,用离子方程式表示?。
②根据学生丙的实验结果,请对学生乙的实验结果作出简要评价:?。
5、实验题 氮化铝(AIN)是一种新型无机材料,广泛应用于集成电路生产领域。某化学研究小组利用氮气、氧化铝和活性炭制取氮化铝,设计下图实验装置。
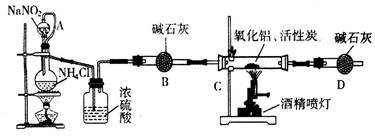
试回答:
(1)实验中用饱和NaNO2与 NH4C溶液制取氮气的化学方程式为?。
(2)装置中分液漏斗与蒸馏烧瓶之间的导管A的作用是?(填写序号)。
a.防止NaNO2饱和溶液蒸发? b.保证实验装置不漏气? c.使NaNO2饱和溶液容易滴下
(3)按图连接好实验装置,检查装置气密性的方法是?。
(4)化学研究小组的装置存在严重问题,请说明改进的办法?。
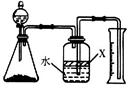
(5)反应结束后,某同学用下图装置进行实验来测定氮化铝样品的质量分数(实验中导管体积忽略不计)。已知:氮化铝和NaOH溶液反应生成Na[Al(OH)4]和氨气
 。
。
①广口瓶中的试剂X最好选用?(填写序号)。
a.汽油? b.酒精? c.植物油? d.CCl4
②广口瓶中的液体没有装满(上方留有空间),则实验测得NH3的体积将?(填“偏大”、“偏小”、“不变”)。
③若实验中称取氮化铝样品的质量为10.0g,测得氨气的体积为3.36L(标准状况),则样品中AlN的质量分数为?。