微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 同温同压下,气体A与氧气的质量比为1∶2,体积比为1∶4,气体A的相对分子质量是(? )
A.16
B.17
C.44
D.64
参考答案:D
本题解析:同温同压下,气体的体积之比等于其对应的物质的量之比,将抽象条件具体化则有:假定A为1 mol,氧气为4 mol,则它们的质量分别为:MA g、128 g,即MA g∶128 g=1∶2,则MA=64。
本题难度:简单
2、实验题 (14分)室温下,将一定浓度的Na2CO3溶液滴入CuSO4溶液中得到了蓝色沉淀。为了确定该沉淀的组成,某研究性学习小组进行了以下实验和研究。
(一)【提出假说】
假设一:两者反应只生成CuCO3沉淀;
假设二:两者反应只生成Cu(OH)2沉淀;
假设三:?。
(二)【理论探究】
假设二中只生成Cu(OH)2的原因是??(用一个离子方程式表示)。
查阅资料:CuCO3和Cu(OH)2均不带结晶水;
(三)【实验探究】
步骤一:将CuSO4溶液加入到等浓度等体积的Na2CO3溶液中并搅拌,有蓝色沉淀生成。
步骤二:将沉淀从溶液中分离出来。
步骤三:利用下图所示装置,选择必要的试剂,定性探究生成物的成分。
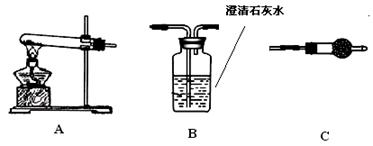
(1)各装置连接顺序为 ??。
(2)装置C中装有试剂的名称是?。
(3)能证明生成物中有CuCO3的实验现象是?。
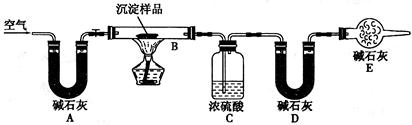
步骤四:?步骤三:利用下图所示装置,进行定量分析:
(4)①A装置中玻璃仪器的名称是?。
②实验开始时和实验结束时都要通入过量的空气其作用分别是?
?和?。
数据记录:
?
| B装置中样品的质量(g)
| C装置的质量(g)
| D装置的质量(g)
|
实验前
| 33.3
| 262.1
| 223.8
|
试验后
| 24
| 264.8
| 230.4
|
(四)【实验结论】
利用上述数据初步判断该沉淀的成分是CuCO3和Cu(OH)2,若所得沉淀是纯净物而不是混合物,通过计算写出该物质的化学式?。
参考答案:(14分)
(一)【提出假说】:生成的是CuCO3和Cu(OH)2的混合物(1分)
(二)【理论探究】:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑(2分);
(三)【实验探究】:(1)A→C→B (2分)
(2)无水硫酸铜 (2分)
(3)装置B中澄清石灰水变浑浊(2分)
(4)①U 形管;(1分)
②将装置中原有含水蒸气和CO2的空气排出;(1分)
将B中分解产生的水蒸气和CO2全部排出,被C、D装置完全吸收。(1分)
(四)【实验结论】:Cu2(OH)2CO3 (2分)。
本题解析:根据假设1和假设2推出假设3。氢氧化铜应为水解产物。
点评:本题属于难度较大综合性较强的物质推断题,完成此类题目,要注意分析题干所提供的信息,明确各种物质的性质,以及哪些因素对实验结果有影响,认真分析实验数据,仔细作答,还要注意平时知识的积累。
本题难度:简单
3、填空题 (10分)已知某白色混合物粉末中含有CuSO4、K2SO4、NH4HCO3、NH4Cl、NaCl五种物质中的两种,且物质的量之比为1:1。请完成下述探究混合物组成的实验。
仅限选择的仪器、用品和试剂:烧杯、试管、玻璃棒、量筒、胶头滴管、药匙、酒精灯、火柴、试管夹、镊子;红色石蕊试纸、淀粉碘化钾试纸;1mol/L硫酸、1mol/L硝酸、1mol/L盐酸、1mol/L NaOH溶液、Ba(NO3)2溶液、AgNO3溶液、蒸馏水。
一、初步探究
取适量固体混合物于烧杯中,加入蒸馏水搅拌,混合物完全溶解,得到无色透明溶液A,同时闻到有轻微的刺激性气味。用胶头滴管取少量溶液A于试管中,再滴加稀硝酸,溶液中有无色气泡产生;继续滴加过量稀硝酸至溶液中不再产生气泡,得到无色透明溶液B。
(1)用?(填实验用品名称)取固体混合物于烧杯中。
(2)上述实验可以得到的初步结论是?。
二、进一步探究
(3)请设计实验方案进一步确定该固体混合物的组成。叙述实验操作、预期现象和结论。
实验操作
| 预期现象和结论
|
?
| ?
|
?
| ?
参考答案:
(1)药匙(1分)
(2)该混合物中肯定含有NH4HCO3(1分),肯定不含有CuSO4(1分)
(3)
实验操作
预期现象和结论
向溶液B中滴加少量Ba(NO3)2溶液。(1分)
如果产生白色沉淀,说明原固体混合物中含有K2SO4;(1分)
如果没有白色沉淀产生,说明原固体混合物中不含K2SO4,(含有NaCl或NH4Cl。)
(1分)
取少量原固体混合物于试管底部,(1分)?将试管套入试管夹,用火柴点燃酒精灯,充分加热试管。(1分)
如果试管底部有固体残留,说明混合物中含有NaCl;(1分)
如果试管底部无固体残留,说明混合物中含有NH4Cl;(1分)
其他答案合理亦可。
本题解析:(1)用药匙取固体混合物于烧杯中。
(2)固体物质加水溶解,得到无色透明溶液,肯定不含Cu2+,闻到有轻微的刺激性气味,说明含有NH4+,再滴加稀硝酸,有气泡产生,说明生成了CO2,由此可以得到的初步结论是混合物中肯定含有NH4HCO3,肯定不含有CuSO4。
(3)
实验操作
预期现象和结论
向溶液B中滴加少量Ba(NO3)2溶液。
如果产生白色沉淀,说明原固体混合物中含有K2SO4;
如果没有白色沉淀产生,说明原固体混合物中不含K2SO4,(含有NaCl或NH4Cl。)
取少量原固体混合物于试管底部,(1分)?将试管套入试管夹,用火柴点燃酒精灯,充分加热试管。
如果试管底部有固体残留,说明混合物中含有NaCl;
如果试管底部无固体残留,说明混合物中含有NH4Cl;
本题难度:简单
4、实验题 (16分)某班学生在老师指导下探究氮的化合物的某些性质。
(1)同学甲在实验室利用下列装置(后面有图)制取氨气和氧气的混合气体,并完成氨的催化氧化。
A中加入浓氨水,D中加入碱石灰,E内放置催化剂(铂石棉),请回答:
①仪器B的名称:__________。B内只需加 入一种固体试剂,该试剂的名称为_________,B中能产生氨气和氧气混合气体的原 入一种固体试剂,该试剂的名称为_________,B中能产生氨气和氧气混合气体的原 因(结合化学方程式回答)_?__。 因(结合化学方程式回答)_?__。
②按气流方向连接各仪器?(填接口字母)
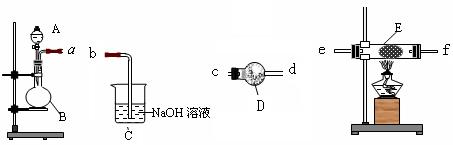
(2)同学乙拟用甲同学得到的混合气体X(NO及过量的NH3),验证NO能被氨气还原并测算其转化率(忽略装置内空气的影响)。装置如下:
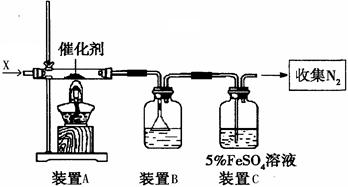
①装置C的作用可能是 ____________。
②若进入装置A的NO共268.8mL(已折算为标准状况,下同),氨气过量,最后收集到标准状况下190.4 mL N2,则NO的转化率为?。
(3)N2O3是一种新型硝化剂。一定温度下,在恒容密闭容器中N2O3可发生下列反应:2N2O3+O2 4NO2(g);△H>0,下表为反应在某温度下的部分实验数据: 4NO2(g);△H>0,下表为反应在某温度下的部分实验数据:
t/s
| 0
| 500
| 1000
| c(N2O3)/mol・L-1
| 5.00
| 3.52
| 2.48
|
?
计算在t=500s时,NO2的反应速率为?。
参考答案:(1)①圆底烧瓶?过氧化钠
2Na2O2+2NH3・H2O=4NaOH+O2↑+2NH3↑过氧化钠与氨水反应消耗水,增大了氨水浓度;过氧化钠与水反应生成氧气,反应放热减小了氨气的溶解度;过氧化钠与水反应生成NaOH,电离出OH―,使NH3・H2O的电离平衡逆向移动(3分)?②a c d e f b或a c d f e b
(2)①吸收未反应的NO?②85%(3分)(3)0.00592mol・L-1・s-1(不写单位不得分)
本题解析:略
本题难度:一般
5、实验题 (15分)化学世界奥妙无穷,物质之间的反应更是神秘莫测,善于透过现象看本质是学习化学、研究物质性质的基本能力。请我们一起进行探索。
(1)课堂上化学老师将干燥的氯气依次通过干燥红布条和潮湿的红布条,结果:干燥红布条无明显变化,而潮湿的红布条褪色。
①某学生立即发言:结论一、?,
结论二、氯气与水反应生成的次氯酸具有漂白性。
②老师提示说:还需要补充一个实验才能得知结论二,该实验是?
③请写出氯气与水反应的离子方程式?
(2)某实验小组用铜和浓硝酸反应制备NO2,并收集一试管NO2气体,将集气瓶倒置于水槽中,并轻微振荡,发现一些典型现象,并对此现象进行探究。
①请写出NO2与水反应化学方程式,并用单线桥表示电子转移方向和数目
?
②该小组成员积极探讨,得出结论,NO2与水一定发生了化学反应,并设计了两个实验操作对产物进行了验证,得出产物是NO 和HNO3。请填写下表中的甲、乙、丙三处。
实验操作
| 实验现象
| 实验结论
| 用玻璃片将水槽中的试管口盖住,轻轻将试管取出
| 试管内约有2/3体积的水溶液,且无色
| NO2与水发生了化学反应,而不是溶于水
| 将试管正立,取下玻璃片
| 甲
| NO2和水反应生成了NO气体
| 乙
| 丙
| NO2和水反应生成了硝酸
参考答案:
(1)①干燥的氯气没有漂白性? ………………………2分,
②取红布条置于盐酸溶液中,红布条不褪色? …………2分
③Cl2 + H2O = H+ + Cl― + HClO? .................................2分,写化学方程式不给分
(2)
①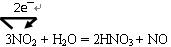 ? ................3分,方程式、电子转移方向及数目各1分 ? ................3分,方程式、电子转移方向及数目各1分
②甲、试管口无色气体变红棕色 ............................................................2分
乙、用胶头滴管在试管内溶液中滴加几滴紫色石蕊试剂......................................... 2分
丙、溶液变红色........................................................................................ 2分
本题解析:略
本题难度:简单
|
|