微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知c(NH4Cl)<0.1?mol/L时,溶液的pH>5.1,现用0.1?mol/L盐酸滴定10?mL?0.05?mol/L氨水,用甲基橙作指示剂,达到终点时所用盐酸的量应是
[? ]
A.10?mL?
B.5?mL
C.大于5?mL?
D.小于5?mL
参考答案:C
本题解析:
本题难度:一般
2、选择题 中和滴定实验中,下列说法正确的是
[?]
A.滴定时视线必须注视滴定管中液面刻度的变化
B.锥形瓶必须用待测液润洗
C.滴定前必须使滴定管尖嘴部分充满液体
D.滴定管不能用标准液润洗
参考答案:C
本题解析:
本题难度:简单
3、简答题 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:
步骤一:配制250mL?0.10mol/L?NaOH标准溶液.
步骤二:取20.00mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞溶液作指示剂,用自己配制的标准NaOH溶液进行滴定.重复上述滴定操作4次,记录数据如下.
| 实验编号 | NaOH溶液的浓度
(mol/L) | 滴定完成时,消耗NaOH溶液的体积(mL) | 待测盐酸溶液的体积(mL)
1
0.10
20.02
20.00
2
0.10
20.00
20.00
3
0.10
19.00
20.00
4
0.10
19.98
20.00
|
(1)步骤一需要称量氢氧化钠固体的质量为______g,配制标准溶液需要用到玻璃棒,烧杯外,还需要的玻璃仪器有______.
(2)步骤二中量取20.00mL的稀盐酸用到的仪器是______.滴定达到终点的现象是______.
(3)根据上述数据,可计算出该盐酸的浓度为______.
(4)排去滴定管中气泡的方法应采用如图的______操作,然后轻轻挤压玻璃球使尖嘴部分充满碱液.
(5)在上述实验中,下列操作(其他操作正确)会造成测定结果(待测液浓度值)偏高的有______(多选扣分):
A.配制标准溶液定容时,加水超过刻度
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸溶液润洗
D.滴定到达终点时,仰视读出滴定管读数;
E.碱式滴定管尖嘴部分有气泡,滴定后消失.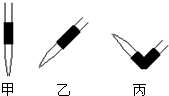
参考答案:(1)m=nM=0.25L×0.1moL/L×40g/mol=1.0g,实验时需用到的玻璃仪器除玻璃棒、烧杯外,还需要250mL容量瓶,并用胶头滴管定容,
故答案为:1.0;250mL容量瓶,胶头滴管;
(2)量取20.00mL的稀盐酸需用酸式滴定管,滴加2~3滴酚酞溶液作指示剂,最后一滴NaOH溶液加入时,溶液颜色恰好由无色变为(浅)红色,
故答案为:酸式滴定管;最后一滴NaOH溶液加入时,溶液颜色恰好由无色变为(浅)红色,且半分钟内不褪色;
(3)根据c(酸)×V(酸)=c(碱)×V(碱),需要V(NaOH)=20.02+20.00+19.983mL=20mL,实验3误差较大,可舍弃,则该盐酸的浓度为20mL×0.10mol/L20mL=0.10mol/L,故答案为:0.10mol/L;
(4)碱式滴定管的气泡通常橡皮管内,只要将滴定玻璃头朝上,并挤橡皮管中的玻璃珠就可以将气泡冲排出,故答案为:丙;
(5)A.配制标准溶液定容时,加水超过刻度,导致溶液浓度偏小,滴定时体积偏大,则待测液浓度偏大,故A正确;
B.锥形瓶水洗后直接装待测液,对实验无影响,故B错误;
C.酸式滴定管水洗后未用待测稀盐酸溶液润洗,会导致盐酸浓度偏小,需要NaOH体积偏小,测定值偏小,故C错误;
D.滴定到达终点时,仰视读出滴定管读数,会导致NaOH体积偏大,测定溶液浓度变大,故D正确;
E.碱式滴定管尖嘴部分有气泡,滴定后消失,会导致测定NaOH体积偏大,测定值偏大,故E正确.
故答案为:ADE.
本题解析:
本题难度:一般
4、选择题 用0.2000mol/L?NaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合液中两种酸的浓度均约为0.1mol/L;用酚酞作指示剂),判断下列说法正确的是( )
A.当锥形瓶中溶液由红色变成无色,且在半分钟内不变红,即达到滴定终点
B.滴至终点时,消耗NaOH溶液的体积约为所取混合酸溶液体积的一半
C.滴至终点后,俯视读取液面读数会造成测定结果偏低
D.本实验可测出原混合酸中H+总浓度约为0.2000mol/L
参考答案:C
本题解析:
本题难度:简单
5、实验题 用酸碱中和滴定法测定某烧碱的纯度。
(1)配制待测溶液将已称好的2.100g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成250ml溶液,所需的主要仪器有_______________。
(2)滴定
①盛装0.1890mol/L盐酸标准液应该用_______式滴定管,滴定管装液前,先用蒸馏水洗涤,再用要盛放的溶液__________。
②准确量取待测液25.00 mL于洁净锥形瓶中,再向锥形瓶中加入1-2滴指示剂,进行滴定操作,达到滴定终点时有关数据记录如下。
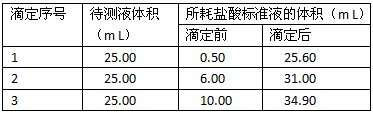
(3)计算 NaOH溶液的物质的量浓度为 _________,烧碱样品的纯度为_________。
(4)下列几种操作对c(NaOH)的影响(填“偏高” 、“偏低”或“无影响” )
①若用蒸馏水冲洗锥形瓶,则会使c(NaOH)_______;
②若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使c(NaOH)_______;
③若刚见到指示剂局部的颜色有变化就停止滴定,则会使c(NaOH)_______;
④读数时,若开始时仰视读数,滴定结束时俯视读数,则会使c(NaOH)_______;
参考答案:(1)250mL容量瓶, 烧杯, 玻璃棒, 胶头滴管
(2) ①酸 ;润洗
(3)0.189mol/L ;90%
(4)①无影响; ②偏高; ③偏低; ④偏低
本题解析:
本题难度:一般