微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (15分)氮化硅是一种重要的结构陶瓷材料,硬度大、耐磨损。利用SiO2和C的混合粉末在N2的气氛中加热至1300℃反应制得。请回答下列问题:
(1)已知氮化硅的晶体结构中,原子间都以单键相连,且N原子和N原子,Si原子与Si原子不直接相连,同时每个原子都满足8电子稳定结构,则氮化硅的化学式____,晶体类型是?;
(2)基态Si原子的电子排布式为_________;Si和C相比,电负性较大的是_________,
(3)在SiO2晶体结构中,O-Si-O的键角是_______,Si原子和周围的四个O原子组成的空间构型为?,SiO2中Si的杂化类型_______;
(4)氮化硅抗腐蚀能力强,一般不与其他无机酸反应,但能和氢氟酸反应生成硅酸。试写出该反应的化学方程式?。
(5)晶体硅的晶胞如图所示,则每个晶体硅的晶胞中含有?个硅原子。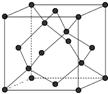
参考答案:(1) Si3N4 (2分)原子晶体(1分) (2) 1s22s22p63s22p2 ?(2分) C (1分)
(3) 109°28′(1分)?正四面体(2分)sp3(2分)?
(4) Si3N4+4HF+9H2O=3H2SiO3↓+4NH4F(2分)? (5)? 8(2分)
本题解析:(1)每个原子都满足8电子稳定结构,所以其化合价分别是+4价和-3价,因此化学式为Si3N4。由于晶体中的微粒是原子,所以形成的晶体是原子晶体。
(2)根据构造原理可知,基态Si原子的电子排布式为 1s22s22p63s22p2 。非金属性越强,电负性越大,所以碳的电负性大于硅的。
(3)由于在SiO2晶体结构中,Si原子和周围的四个O原子相邻,所以构成的应是正四面体,采用的是sp3杂化,O-Si-O的键角是 109°28′。
(4)能和氢氟酸反应生成硅酸,则根据原子守恒可知,另外一种生成物是NH4F,所以方程式为Si3N4+4HF+9H2O=3H2SiO3↓+4NH4F。
(5)根据晶体硅的晶胞结构可知,8个顶点有8个硅原子,6个面心处有6个硅原子,晶胞内部还有4个硅原子,所以共计是8×1/8+6×1/2+4=8个。
本题难度:一般
2、选择题 下列物质的熔点高低顺序,正确的是
A.金刚石>晶体硅>碳化硅
B.K>Na
C.NaF<NaCl<NaBr
D.CI4>CBr4
参考答案:D
本题解析:
A.原子晶体熔点,比较共价键键长,键长越短,键能越大,物质越稳定;键长:C-C<C-Si<Si-Si,熔点:金刚石>碳化硅>晶体硅;
B.金属晶体键能的大小比较看金属原子的半径大小 ,半径越小 键能越大,熔点越高。K<Na
C.离子晶体熔点,比较晶格能,离子半径越小,所带电荷越多,晶格能越大,离子晶体熔点越高;离子半径:F-<Cl-<Br-,熔点:NaF>NaCl>NaBr ;
D.分子晶体熔点,比较分子间作用力,相对分子质量越大,分子间作用力越大,熔点越高。
【考点定位】比较物质的熔点和沸点的高低,通常按下列步骤进行,首先比较物质的晶体类型,然后再根据同类晶体中晶体微粒间作用力大小,比较物质熔点和沸点的高低,具体比较如下:
一、判断所给物质的晶体类型,然后按晶体的熔点和沸点的高低进行比较,一般来说晶体的熔点和沸点的高低是:原子晶体>离子晶体>分子晶体,例如:晶体硅>氯化钠>干冰。但并不是所有这三种晶体的熔点和沸点都符合该规律,例如:氧化镁(离子晶体)>晶体硅(原子晶体)。而金属晶体的熔点和沸点变化太大,例如汞、铷、铯、钾等的熔点和沸点都很低,钨、铼、锇等的熔点和沸点却很高,所以不能和其它晶体进行简单的比较。
本题难度:一般
3、选择题 等电子原理认为:含有相同原子数和相同价电子数(指全部电子总数或价电子总数)的分子或离子,具有相同的结构特征.下面各组微粒中,几何构型不相同的是( )
A.H3O+、NH3
B.NH4+、CH4
C.NH3、BF3
D.CO2、BeCl2
参考答案:C
本题解析:
本题难度:一般
4、选择题 据某科学杂志报道,国外有一研究发现了一种新的球形分子,它的分子式为C60Si60,其分子结构好似中国传统工艺品“镂雕”,经测定其中包含C60,也有Si60的结构。下列叙述正确的是?
A.该物质有很高的熔点、很大的硬度
B.该物质形成的晶体属分子晶体
C.该物质分子中Si60被包裹在C60里面
D.C60易溶于水
参考答案:B
本题解析:该物质的的分子式为C60Si60,这说明该物质形成的晶体类型是分子晶体,A不正确,B正确;碳原子半径小于硅原子半径,所以该物质分子中Si60不可能包裹在C60里面,C不正确。水是极性分子,该物质是非极性分子,难溶于水,D不正确,大啊啊阿香B。
点评:该题是高考中的常见题型和考点,属于中等难度试题的考查,试题综合性强,侧重对学生能力的培养和训练,有利于培养学生的逻辑推理能力、自学能力和知识的迁移能力,提高学生的应试能力和学习效率。
本题难度:简单
5、填空题 铜及其合金是人类最早使用的金属材料。
(1)铜原子的核外电子排布式是____________。
(2)下图是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为____。
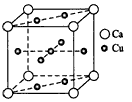
(3)Cu2+能与NH3、H2O、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]2+中存在的化学键类型有____(填序号)。
A.配位键 B.金属键 C.极性共价键 D.非极性共价键 E.离子键
②[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为__________。
③某种含Cu2+的化合物可催化丙烯醇制备丙醛的反应:HOCH2CH=CH2→CH3CH2CHO。在丙烯醇分子中发生某种方式杂化的碳原子数是丙醛分子中发生同样方式杂化的碳原子数的2倍,则这类碳原子的杂化 方式为______________。
参考答案:(1)1s22s22p63s23p63d104s1
(2)1:5
(3)①AC;②平面正方形;③sp2
本题解析:
本题难度:一般