��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ֱ���ŷź�SO2�����������γɽ��꣬Σ�������������Ƽ�ѭ�������ѳ������е�SO2
��1�����Ƽ�ѭ�����У�Na2 SO3��Һ��Ϊ����Һ������NaOH��Һ����SO2�Ƶã�
�÷�Ӧ�����ӷ���ʽ��
��2������Һ����SO2�Ĺ����У�pH��n(SO3²-)��n(HSO3
�ο��𰸣�
���������
�����Ѷȣ�����
2��ѡ���� ���е��뷽��ʽ������ǣ� ? ��
A��H2CO3?2H++CO32-
B��NaHSO4����Һ��=Na++H++SO42-
C��NaHCO3=Na++HCO3-
D��CaCO3=Ca2++CO32-
�ο��𰸣�A
���������
�����Ѷȣ���
3������� ��12�֣�
��1��20��ʱ0.1 mol��L��1NaOH�ֱ�ζ�0.1 mol��L��1HCl��0.1 mol��L��1CH3COOH��pH�仯�������¡�
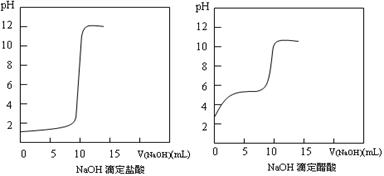
�����������ش��������⣺
�ٲ�ô������pHΪ3����20��ʱ��Ũ�ȴ���ĵ����Ϊ ��
�ڵζ���ʼ��������߱仯��������ԭ���� ��
��2��25 ��ʱ0.1 mol��L-1��H2Rˮ��Һ�У�������������������ҺpH���õ�����H2R��HR����R2������������Һ����c(Na+)=c(R2��)+c(HR��)+c(H2R)ʱ��Һ������Ϊ (�ѧʽ)��
��3����ͼ��ijˮ��Һ��pH��0��14�ķ�Χ��H2CO3��HCO3����CO32�����ֳɷ�ƽ��ʱ����ɷ�����
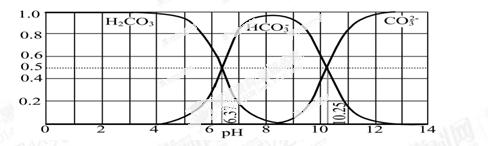
������������ȷ���� ��
A����ͼ��1.0 mol��L��1̼������Һ�ζ�1.0 mol��L��1 HCl��Һ�ĵζ�����
B����pH�ֱ�Ϊ6.37��10.25ʱ����Һ��c(H2CO3)=c(HCO3��)=c(CO32��)
C������ѪҺ��pHԼΪ7.4����CO2��ѪҺ�ж���HCO3����ʽ����
D������CO2��NaOH��Ӧ��ȡNaHCO3���˿�����Һ��pHΪ7��9֮��
��4��������ʩ����������ͨ��ת��Ϊ̼��炙�̼����狀�ű����������ã����ط�����������ڵ���ø�����£�ת��Ϊ̼��李���֪���������ˮ�еĵ���ƽ�ⳣ����25�棩���±���
�������
| H2CO3
| NH3��H2O
|
����ƽ�ⳣ��
| Ka1��4.30��10-7 Ka2��5.61��10-11
| 1.77��10-5
|
���г�����0.1 mol��L-1��(NH4)2CO3��Һ��
������Ϊ����Һ�� �ԣ���ᡱ�����С����������ԭ���� ��
�ھ���Һ������֮�������й�ϵʽ������Ϊ������ȷ���� ��
A��c (NH4+)��c (CO32-)��c (HCO3-)��c (NH3��H2O)
B��c(NH4+)+c(H+)��c(HCO3-)+c(OH-)+c(CO32-)
C��c (CO32-) + c (HCO3-) +c (H2CO3)��0.1 mol��L-1
D��c (NH4+)+ c (NH3��H2O)��2 c (CO32-) + 2c (HCO3-) +2 c (H2CO3)
�ο��𰸣�(1)1% ����������,�к����ɵĴ�������ӶԴ������������� ��2��NaHR ��3��CD ��4��
�� �� ����NH3��H2O�ĵ���ƽ�ⳣ������HCO3-�ĵ���ƽ�ⳣ�������CO32-ˮ��̶ȴ���NH4+ˮ��̶ȣ���Һ��c (OH-) > c(H+)����Һ�ʼ��� �� A��C��D
���������
�����������2���ٸ���ͼ���֪0.1mol?L-1�Ĵ��ᣬ��PHΪ3������c��H+��=10-3mol/L���ʵ����=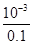 ��100%=1%���ڴ��������ᣬ�������������Ʒ�Ӧ����CH3COO-��ʹ����ƽ������CH3COOH?CH3COO-+H+����H+Ũ�ȱ仯�ȽϿ죬�ʴ�Ϊ�����������ᣬ�кͷ�Ӧ���ɵĴ�������ӶԴ���ĵ���������ƣ���2��25��ʱ0.1mol?L-1��H2Rˮ��Һ�У�������������������ҺpH���õ�����H2R��HR-��R2-����������Һ����Һ�д���c��Na+��=c��R2-��+c��HR-��+c��H2R����˵����ԭ�Ӻ�Rԭ����1��1����������Һ�У�R�γɵ���Ϊ��Ԫ�ᣬ���Ը�����Ϊ��Ԫ�����ʽ�Σ���NaHR���ʴ�Ϊ��NaHR����3����A.1.0mol/L̼������Һ�ζ�1.0mol/LHCl��Һ����̼��Ũ�ȴﵽ����֮ǰ��̼��Ũ��Ӧ����������ʼŨ�Ȳ�����Ϊ1.0mol/L����A����B����ͼ��֪��pHΪ6.37ʱc��H2CO3��=c��HCO3-����pHΪ10.25ʱ��c��HCO3-��=c��CO32-���������ߵ�Ũ�Ȳ���ȣ���B����C����ͼ��֪��pHΪ7.4ʱ��HCO3-�����������ѪҺ��pHԼΪ7.4����CO2��ѪҺ�ж���HCO3-����ʽ���ڣ���C��ȷ��D����Һ��pHΪ7��9֮��ʱ����Һ�е���������Ҫ��HCO3-��ʽ���ڣ�������Һ�е�������ҪΪ̼�����ƣ���D��ȷ����ѡCD����4���ٷ�������ƽ�ⳣ����֪����̶ȣ�NH3?H2O��H2CO3��HCO3-����Ӧ��ˮ��̶�NH4+��HCO3-��CO32-��������0.1mol?L-1�ģ�NH4��2CO3��Һ�ʼ��ԣ�����NH3?H2O�ĵ���ƽ�ⳣ������HCO3-�ĵ���ƽ�ⳣ�������CO32-ˮ��̶ȴ���NH4+ˮ��̶ȣ���Һ��c ��OH-����c��H+������Һ�ʼ��ԣ���A����Һ��笠�����Ũ�ȴ���̼�������Ũ�ȣ�̼�������ˮ��̶ȴ���笠�����ˮ��̶ȣ�������Һ������Ũ�ȴ�СΪ��c��NH4+����c��CO32-����c��HCO3-����c��NH3?H2O������A��ȷ��B����Һ�д��ڵ���غ�Ϊ��c��NH4+��+c��H+��=c��HCO3-��+c��OH-��+2c��CO32-�����ʴ���C��������Һ�������غ�õ���c��CO32-��+c��HCO3-��+c��H2CO3��=0.1mol?L-1 ����C��ȷ��D��������Һ�������غ㣬n��N����n��C��=2��1�������Һ������������غ��ϵ�õ���c��NH4+��+c��NH3?H2O��=2c��CO32-��+2c��HCO3-��+2c��H2CO3������D��ȷ���ʴ�Ϊ��ACD��
��100%=1%���ڴ��������ᣬ�������������Ʒ�Ӧ����CH3COO-��ʹ����ƽ������CH3COOH?CH3COO-+H+����H+Ũ�ȱ仯�ȽϿ죬�ʴ�Ϊ�����������ᣬ�кͷ�Ӧ���ɵĴ�������ӶԴ���ĵ���������ƣ���2��25��ʱ0.1mol?L-1��H2Rˮ��Һ�У�������������������ҺpH���õ�����H2R��HR-��R2-����������Һ����Һ�д���c��Na+��=c��R2-��+c��HR-��+c��H2R����˵����ԭ�Ӻ�Rԭ����1��1����������Һ�У�R�γɵ���Ϊ��Ԫ�ᣬ���Ը�����Ϊ��Ԫ�����ʽ�Σ���NaHR���ʴ�Ϊ��NaHR����3����A.1.0mol/L̼������Һ�ζ�1.0mol/LHCl��Һ����̼��Ũ�ȴﵽ����֮ǰ��̼��Ũ��Ӧ����������ʼŨ�Ȳ�����Ϊ1.0mol/L����A����B����ͼ��֪��pHΪ6.37ʱc��H2CO3��=c��HCO3-����pHΪ10.25ʱ��c��HCO3-��=c��CO32-���������ߵ�Ũ�Ȳ���ȣ���B����C����ͼ��֪��pHΪ7.4ʱ��HCO3-�����������ѪҺ��pHԼΪ7.4����CO2��ѪҺ�ж���HCO3-����ʽ���ڣ���C��ȷ��D����Һ��pHΪ7��9֮��ʱ����Һ�е���������Ҫ��HCO3-��ʽ���ڣ�������Һ�е�������ҪΪ̼�����ƣ���D��ȷ����ѡCD����4���ٷ�������ƽ�ⳣ����֪����̶ȣ�NH3?H2O��H2CO3��HCO3-����Ӧ��ˮ��̶�NH4+��HCO3-��CO32-��������0.1mol?L-1�ģ�NH4��2CO3��Һ�ʼ��ԣ�����NH3?H2O�ĵ���ƽ�ⳣ������HCO3-�ĵ���ƽ�ⳣ�������CO32-ˮ��̶ȴ���NH4+ˮ��̶ȣ���Һ��c ��OH-����c��H+������Һ�ʼ��ԣ���A����Һ��笠�����Ũ�ȴ���̼�������Ũ�ȣ�̼�������ˮ��̶ȴ���笠�����ˮ��̶ȣ�������Һ������Ũ�ȴ�СΪ��c��NH4+����c��CO32-����c��HCO3-����c��NH3?H2O������A��ȷ��B����Һ�д��ڵ���غ�Ϊ��c��NH4+��+c��H+��=c��HCO3-��+c��OH-��+2c��CO32-�����ʴ���C��������Һ�������غ�õ���c��CO32-��+c��HCO3-��+c��H2CO3��=0.1mol?L-1 ����C��ȷ��D��������Һ�������غ㣬n��N����n��C��=2��1�������Һ������������غ��ϵ�õ���c��NH4+��+c��NH3?H2O��=2c��CO32-��+2c��HCO3-��+2c��H2CO3������D��ȷ���ʴ�Ϊ��ACD��
���㣺�к͵ζ��������ˮ��
�����Ѷȣ�����
4������� д������������ˮ��Һ�еĵ��뷽��ʽ��H2SO4______AlCl3______��
�ο��𰸣�������ǿ����ʣ�����������Ӻ���������ӣ���H2SO4�T2H++SO42-���Ȼ�����ǿ����ʣ�����ȫ����������Ӻ������ӣ���AlCl3=Al3++3Cl-��
�ʴ�Ϊ��H2SO4�T2H++SO42-��AlCl3=Al3++3Cl-��
���������
�����Ѷȣ�һ��
5������� д���������ʵĵ��뷽��ʽ��
(1)HCl��___________�� (2)Na2SO4��________��
(3)NH4Cl��__________�� (4)Ca(OH)2��________��
�ο��𰸣�(1)HCl=H++Cl-
(2)Na2SO4=2Na++SO42-
(3)NH4Cl=NH4++Cl-
(4)Ca(OH)2=Ca2++2OH-
���������
�����Ѷȣ�һ��