微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
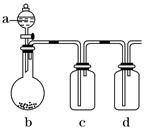
1、填空题 有几个实验小组的同学,利用下图装置进行“一器多用”的实验探究(a中盛放的液体均匀慢速滴下;b中盛放的药品足量;若在c、d中盛装液体,则长导管均浸入液面以下),每组同学设想在a、b、c、d中分别盛放不同物质,来制取某种气体并检验其性质。
请你回答以下各组同学在交流实验设计方案中提出的问题:
Ⅰ.(1)若a:浓盐酸;b:高锰酸钾(其氧化性比二氧化锰强很多);c:红色鲜花瓣。在实验过程中c中的现象_____________________________________________________________。
d装置中盛放药品的作用是______________________________,请写出d中反应的离子方程式: ___________________________________________________________________。
(2)若a:稀盐酸;b:贝壳粉;c:饱和碳酸钠溶液;d:饱和Na2SiO3溶液。在实验过
程中,c中出现的现象是____________________。d中现象是____________,这说明
________________________________________________________________________。
Ⅱ.你认为四组同学在制取气体之前都应进行的操作是________________。你还可以利用此装置的a和b两部分制取的气体有(只写一种)_________________。
2、选择题 实验室中某些气体的制取、收集、尾气处理(或性质实验)装置如图所示,用此装置和下表中提供的物质完成相关实验,合理的选项是

选项
| I中的物质
| II中收集的气体
| III中的物质
|
A
| Cu和浓硝酸
| NO
| NaOH溶液
|
B
| 浓盐酸和MnO2
| Cl2
| NaOH溶液
|
C
| 碳酸钙和盐酸
| CO2
| 澄清石灰水
|
D
| 浓氨水和CaO
| NH3
| 酚酞溶液
|
?
3、实验题 现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。已知实验中可能会发生下列反应:


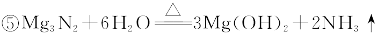
可供选择的装置和药品如下图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。

回答下列问题:
(1)在设计实验方案时,除装置A、E外,还应选择的装置(填字母代号)及其目的分别是________________________________________________________________________________
_______________________________________________________________________________。
(2)连接并检查实验装置的气密性。实验开始时,打开自来水的开关,将空气从5升的储气瓶压入反应装置,则气流流经导管的顺序是(填字母代号)______________________________。
(3)通气后,如果同时点燃A、F装置的酒精灯,对实验结果有何影响? __________,原因是_____________________________________________________________________________。
(4)请设计一个实验,验证产物是氮化镁:________________________________________
_______________________________________________________________________________。
4、填空题 (15分)氯化铁是常见的水处理剂,无水氯化铁的熔点为555K、沸点为588K。工业制备氯化铁的一种工艺如下:
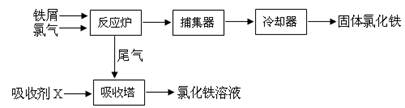
回答下列问题
(1)取0.5mL氯化铁溶液滴入50mL沸水中,再煮沸片刻得红褐色透明液体,该过程可用离子方程式表示为?。
(2)已知FeCl3・6H2O在水中的溶解度如下:
温度/℃
| 0
| 10
| 20
| 30
| 50
| 80
| 100
|
溶解度(g/100gH2O)
| 74.4
| 81.9
| 91.8
| 106.8
| 315.1
| 525.8
| 535.7
|
从FeCl3溶液中获得FeCl3・6H2O的方法是?。
(3)捕集器中温度超过673K,存在相对分子质量为325的物质,该物质的化学式为?。
(4)室温时向FeCl3溶液中滴加NaOH溶液,当溶液中c(Fe3+)≤1.0×10-5 mol・L-1时,视作Fe3+沉淀完全,则Fe3+沉淀完全的pH至少为?(已知Ksp[Fe(OH)3]=1.0×10-38)。
(5)吸收剂X是?,吸收塔中吸收剂X的作用是?。
(6)测定样品中FeCl3的质量分数的方法是:
a.称取mg无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容
b.取出10mL待测溶液于锥形瓶中,加入稍过量的KI溶液充分反应
c.以淀粉作指示剂,用b mol・L-1Na2S2O3溶液滴定(I2+2 Na2S2O3= Na2S4O6+2NaI),共用去VmL。①样品中氯化铁的质量分数为?。
②若用上述办法测定的样品中FeCl3的质量分数偏低(测定过程中产生的误差可忽略),其原因可能是?。
5、填空题 利用图所示装置收集以下6种气体(图中烧瓶的位置不得变化)。 ①H2②Cl2 ③CH4 ④HCl ⑤NH3⑥SO2 若烧瓶是干燥的,则由A口进气,可收集的气体有(写序号); ____? ;