微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关试验操作的叙述正确的是(?)


A.实验室制取少量的乙酸乙酯时,浓硫酸作催化剂和脱水剂
B.将铜丝灼热后伸入到乙醇中,反应后铜丝的质量增重
C.用苯萃取溴水中的溴,分液时有机层从分液漏斗的上口倒出
D.在制取少量的乙酸乙酯时,先在试管中加入浓硫酸,再加入乙醇和乙酸的混合液
参考答案:C
本题解析:略
本题难度:简单
2、实验题 碱式碳酸铜是一种用途广泛的化工原料。工业上可用酸性刻蚀废液(主要含有Cu2+、Fe2+、Fe3+、H +、Cl-)制备,其制备过程如下:

Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
物 质
| Cu(OH)2
| Fe (OH)2
| Fe (OH)3
|
开始沉淀pH
| 4.2
| 5.8
| 1.2
|
完全沉淀pH
| 6.7
| 8.3
| 3.2
|
?
(1)滤渣的主要成分是?(写化学式)。
(2)调节反应A后溶液的pH范围应为?。选择的试剂最合适的是?(填序号)。
a.氨水? b.稀硫酸? c.氢氧化钠? d.碳酸铜
(3)反应B的温度如过高,则所得蓝绿色产品中可能会出现的杂质是?。
(4)将Na2CO3溶液滴入到一定量CuCl2溶液中得到沉淀。用相应的离子方程式表示:
① 沉淀只有CuCO3:?;
② 沉淀只有Cu(OH)2且放出气泡:?。
(5)碱式碳酸铜的组成可表示为:aCuCO3?bCu(OH)2?cH2O。要测定其组成,甲同学设计的实验方案中需要如下五个步骤:①称量样品的质量;②高温分解;③测出CO2的质量;④测出水蒸汽的质量;⑤称量CuO的质量。而乙同学认为除步骤②外,实验只需测定四个量中的三个即可,则合理的组合为?(填序号,写一组即可)。
参考答案:(15分,除注明外每空2分)
(1)Fe(OH)3 ;?(2)3.2~4.2;? d;?(3)CuO(名称亦可);
(4)①Cu2++CO32-=CuCO3↓;②Cu2++CO32-+H2O= Cu(OH)2↓+ CO2↑;
(5)①③④(或①③⑤、①④⑤)(3分)
本题解析:(1)对比原料和目标产物的成分,可以猜测该流程各个步骤的主要目的,反应A是为了氧化亚铁离子,调节pH是为了使铁离子全部变为氢氧化铁沉淀,过滤是为了除去铁元素,因此滤渣的主要成分是Fe(OH)3,反应B是制取碱式碳酸铜,第二次过滤是为了除去可溶性盐;(2)读表中信息,根据流程中原料和目标产物的组成,调节溶液pH时,应使铁离子完全沉淀,而铜离子不能开始沉淀,因此溶液pH应介于3.2~4.2之间;若选择氨水,会引入铵根离子等杂质,故a选项错误;若选择稀硫酸,会引入硫酸根离子等杂质,故b选项错误;若选择氢氧化钠,会引入钠离子等杂质,故c选项错误;若选择碳酸铜,不仅能除去杂质,而且引入的铜离子能增大目标产物的量,故d选项正确;(3)若反应B的温度过高,产生的碱式碳酸铜可能分解生成黑色的氧化铜固体,使制备的目标产物不纯;(4)碳酸根离子与铜离子结合生成碳酸铜沉淀,即Cu2++CO32-=CuCO3↓;铜离子与碳酸根离子发生双水解反应,生成氢氧化铜沉淀和二氧化碳气体,即Cu2++CO32-+H2O= Cu(OH)2↓+ CO2↑;(5)碱式碳酸铜高温分解的原理为:aCuCO3?bCu(OH)2?cH2O  (a+b)CuO+(b+c)H2O↑+aCO2↑,由于各物质的摩尔质量数值上等于式量,n=m/M,该反应中碱式碳酸铜、氧化铜、水蒸气、二氧化碳的系数之比等于物质的量之比,只需要进行①③④(或①③⑤、①④⑤)实验, 就可以计算出碱式碳酸铜的组成中a、b、c的值。
(a+b)CuO+(b+c)H2O↑+aCO2↑,由于各物质的摩尔质量数值上等于式量,n=m/M,该反应中碱式碳酸铜、氧化铜、水蒸气、二氧化碳的系数之比等于物质的量之比,只需要进行①③④(或①③⑤、①④⑤)实验, 就可以计算出碱式碳酸铜的组成中a、b、c的值。
本题难度:一般
3、选择题 除去CO中少量的CO2,选用的试剂和装置均正确的是( )
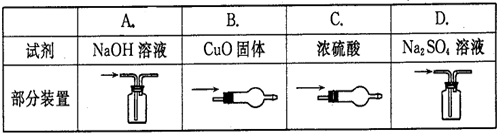
A.A
B.B
C.C
D.D
参考答案:A、二氧化碳是酸性气体,能和碱液反应,一氧化碳和碱不反应,所以可用碱液洗气,故A正确;
B、二氧化碳和氧化铜不反应,所以无法除去二氧化碳,故B错误;
C、干燥管内的干燥剂为粒状固体,浓硫酸是液体,且浓硫酸和二氧化碳不反应,所以无法除去二氧化碳,故C错误;
D、硫酸钠溶液是中性溶液,不含二氧化碳反应,所以无法除去二氧化碳,故D错误;
故选A.
本题解析:
本题难度:简单
4、选择题 下列装置不能达到相应实验目的的是(?)?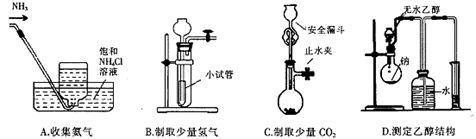
参考答案:A
本题解析:
氨气极易溶于水,不能用排水法收集,氨气密度小于空气,应该用向下排空气法收集氨气,故A答案错误,选A。
本题难度:简单
5、实验题 (16分)下图是某化工厂对海水资源的综合利用的示意图。
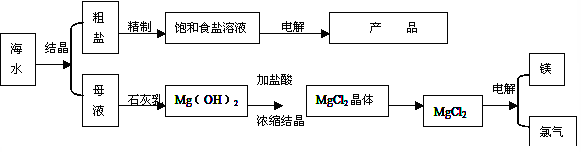
(1)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是:?(填物理变化、化学变化)
(2)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”。电解饱和食盐水的离子方程式为:???。阳极产生气体的如何检验?。利用电解所得气体制36.5%的浓盐酸100t,最少需要消耗食盐:?t。
(3)分离出粗盐的母液中含有Mg2+,从图中可看出对母液进行一系列的加工可制得金属镁。
①在母液中加入石灰乳所起的作用是:?。
②从充分利用当地海洋化学资源,就地取材,经济效益的角度考虑,生产生石灰的原料可是:??。
③电解熔融氯化镁的化学方程式是:?。?
④氮气和氩是两种化学性质相对稳定的气体,都可用做白炽灯的填充气体。但工业上冷却电解无水氯化镁所得的镁蒸气时,却选择稀有气体氩。试用化学反应方程式解释不选用氮气的原因:?。
参考答案:(1)物理变化?(2)2Cl- +2H2O 2OH-+H2 ↑+Cl2 ↑?湿润的淀粉碘化钾试纸? 58.5
2OH-+H2 ↑+Cl2 ↑?湿润的淀粉碘化钾试纸? 58.5
(3)①将镁离子转化为沉淀而分离?②贝壳?③MgCl2 Mg +Cl2 ↑
Mg +Cl2 ↑
④3Mg +N2 Mg3N2
Mg3N2
本题解析:(1)蒸馏法是利用物质的沸点不同进行分离两种互溶的液体的方法,所以蒸馏法是物理变化。
(2)电解饱和食盐水的离子方程式:2Cl- +2H2O 2OH-+H2 ↑+Cl2 ↑。阳极产生的是Cl2,检验Cl2的方法是用湿润的淀粉碘化钾试纸,当试纸变蓝说明有Cl2生成。利用电解所得气体制的36.5%的浓盐酸100t,则需要HCl 36.5t,因此需要NaCl 58.5t。
2OH-+H2 ↑+Cl2 ↑。阳极产生的是Cl2,检验Cl2的方法是用湿润的淀粉碘化钾试纸,当试纸变蓝说明有Cl2生成。利用电解所得气体制的36.5%的浓盐酸100t,则需要HCl 36.5t,因此需要NaCl 58.5t。
(3)①Mg2+可以和OH-反应生成Mg(OH)2,所以在母液中加入石灰乳是将镁离子转化为沉淀而分离。②海边的贝壳主要是CaCO3,CaCO3受热分解得到CaO。③电解熔融氯化镁的化学方程式是:MgCl2 Mg +Cl2 ↑。④氮气可以和镁反应:3Mg +N2
Mg +Cl2 ↑。④氮气可以和镁反应:3Mg +N2 Mg3N2。
Mg3N2。
点评:本题综合性较强,考查的知识点比较基础简单。
本题难度:一般