微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 相同质量的下列材料制成相同长度的绳子,能吊起的物质重量最大的是?
[? ]
A.涤纶绳
B.锦纶绳
C.金属钛绳
D.碳钢绳
参考答案:B
本题解析:
本题难度:简单
2、填空题 电镀污泥中含有Cr(OH)3、Al2O3、ZnO、CuO、NiO等物质,工业上通过“中温焙烧―钠氧化法”回收Na2Cr2O7等物质。
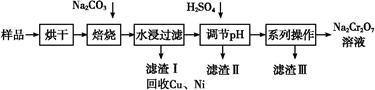
已知:在Na2CrO4溶液中含有少量NaAlO2、Na2ZnO2等物质
(1)水浸后的溶液呈 性(填“酸”、“碱”或“中”)。?
(2)完成氧化焙烧过程中生成Na2CrO4的化学方程式。
Cr(OH)3+ Na2CO3+ 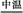 Na2CrO4+ CO2+ ?
Na2CrO4+ CO2+ ?
(3)滤渣Ⅱ的主要成分有Zn(OH)2、 。?
(4)“系列操作”中为:继续加入H2SO4, ,冷却结晶,过滤。继续加入H2SO4目的是 ?。?
已知:①除去滤渣II后,溶液中存在如下反应:
2CrO42―+2H+ Cr2O72―+H2O
Cr2O72―+H2O
②Na2Cr2O7、Na2CrO4在不同温度下的溶解度如下表
?温度
溶解度
化学式
| 20 ℃
| 60 ℃
| 100 ℃
|
Na2SO4
| 19.5
| 45.3
| 42.5
|
Na2Cr2O7
| 183
| 269
| 415
|
Na2CrO4
| 84
| 115
| 126
|
(5)工业上还可以在水浸过滤后的溶液(Na2CrO4)加入适量H2SO4,用石墨作电极电解生产金属铬,写出生成铬的电极反应方程式 ?。?
参考答案:(1)碱
(2)4Cr(OH)3+4Na2CO3+3O2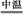 4Na2CrO4+4CO2+6H2O
4Na2CrO4+4CO2+6H2O
(3)Al(OH)3
(4)蒸发浓缩 促进平衡2CrO42―+2H+ Cr2O72―+H2O向正反应方向移动,尽可能生成更多溶解度更大的Na2Cr2O7
Cr2O72―+H2O向正反应方向移动,尽可能生成更多溶解度更大的Na2Cr2O7
(5)CrO42―+8H++6e- Cr+4H2O
Cr+4H2O
本题解析:(1)水浸后溶液中含碳酸钠,碳酸根水解显碱性;
(2)空气中的氧气氧化Cr(OH)3且和Na2CO3反应生成Na2CrO4,根据H元素守恒Cr(OH)3中的H会生成H2O,然后根据化合价升降总数相等配平化学方程式。
(3)根据水浸后溶液中存在Al、Zn元素,加入硫酸调节pH会生成Zn(OH)2、Al(OH)3沉淀。
(4)根据表格中数据知Na2CrO4比Na2Cr2O7溶解度小,故应加入硫酸使Na2CrO4转化成Na2Cr2O7,Na2SO4在温度较低时溶解度小更容易结晶析出,故采用蒸发浓缩、冷却结晶、过滤分离Na2SO4。
(5)CrO42―得电子生成Cr,O2-结合H+生成H2O。
本题难度:困难
3、选择题 下列有关一些物质的用途说法不正确的是
[? ]
A.钛合金广泛用于航天工业
B.光导纤维的主要成分是二氧化硅
C.医院用于造影的“钡餐”主要成分是BaCO3
D.硅胶可以作为实验室某些药品的干燥剂
参考答案:C
本题解析:
本题难度:简单
4、填空题 技术的发展与创新永无止境,我国化工专家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下图:
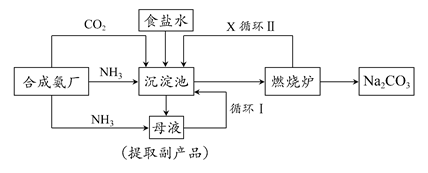
(1)向沉淀池中要通入CO2和氨气,应先通入________(填化学式),原因是________________。
(2)沉淀池中发生的化学反应方程式是________________。
(3)母液中的溶质主要是________。向母液中通氨气后再加入细小食盐颗粒,冷却析出副产品,通入氨气的作用是________________。
(4)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了________(填上述流程中的编号)的循环,物质X是________,从沉淀池中提取沉淀的操作是________________。
(5)写出煅烧炉中发生反应的化学方程式____________________________。
(6)这样制得的产品碳酸钠中可能含有的杂质是________(填化学式),为检验该杂质的存在,具体操作是__________________________________。
参考答案:(1)NH3 因为CO2溶解度较小,而NH3易溶于水,先通NH3有利于CO2吸收
(2)NH3+CO2+NaCl+H2O=NaHCO3↓+NH4Cl
(3)NH4Cl 增大NH4+浓度,使NH4Cl更多析出
(4)循环Ⅰ CO2 过滤
(5)2NaHCO3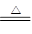 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
(6)NaCl 取少量试样溶解,加用HNO3酸化的AgNO3溶液,若有白色沉淀,说明含有NaCl杂质
本题解析:向沉淀池中通入氨气,使溶液显碱性,有利于CO2吸收;母液中的溶质主要是副产品NH4Cl,通氨气及加入细小食盐颗粒都可使NH4Cl的溶解平衡向结晶方向移动;采取循环操作可提高原料的利用率;由于用了饱和食盐水使析出的碳酸氢钠含氯化钠,则纯碱中含氯化钠。
本题难度:一般
5、选择题 钛和钛合金是21世纪的重要金属材料。它们具有优良的性能,如熔点高、密度小、可塑性好、机械性能好、抗腐蚀能力强,钛合金与人体有很好的“相容性”。根据它们的主要性能,不合实际的用途是
A.用于核潜艇设备的制造
B.用于制造航天设备
C.用来作保险丝
D.可用来制造人造骨
参考答案:C
本题解析:因钛的熔点高,故不适合作保险丝。
本题难度:简单