��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���з�Ӧ�����ӷ���ʽ��ȷ���ǣ���?��
A��̼��Ƹ����ᷴӦ�� CO32-+2H+==CO2��+H2O
B����ˮ�����ᷴӦ�� OH- + H+ ="=" H2O
C������������ϡ���ᷴӦ�� Ba2+ + OH- + H+ + SO42- ="=" BaSO4��+ H2O
D�������Ȼ�����Һ��Ӧ: Fe + Fe3+ ==3Fe2+
2��ѡ���� ������Ba2++SO42-�TBaSO4����ʾ�ķ�Ӧ�ǣ�������
A���������Һ������������Һ��Ӧ
B��������Һ������������Һ��Ӧ
C��������Һ�����ᱵ��Һ��Ӧ
D���Ȼ�����Һ���������Һ��Ӧ
3������� ��������Ԫ��A��B��C��D��E��Ϊ���ڱ���ǰ18��Ԫ�أ���ԭ����������������֪A��B���γɻ�����������������Ԫ�أ�BԪ�غ�CԪ��ͨ���γɵ�����Ϊ14��22�Ļ����DԪ�ص�ԭ�Ӱ뾶�Ƕ���������Ԫ�������ģ�EԪ���ǵؿ��к�����ߵĽ�������ش��������⣺
��1���뻭��D�����ӽṹʾ��ͼ______����C��A����Ԫ���γɵ�18���ӻ�����ĵ���ʽΪ______��
��2��E�������������D������������ˮ���ﷴӦ�����ӷ���ʽ��______��
��3������������Ԫ������������γɵĻ������У��Ⱥ������Ӽ��ֺ��зǼ��Թ��ۼ��ij�����������______���ѧʽ����������Ҫ��;��______������ˮ��Ӧ�����ӷ���ʽ______��
4������� ��ˮ����þ��MgSO4?7H2O����ӡȾ����ֽ��ҽҩ�ȹ�ҵ�϶��й㷺��Ӧ�ã����û�����������ɰ�ķ���-��þ�����ȡ��ˮ����þ����þ�����Ҫ�ɷ���MgCO3���������������ʣ�MgO��SiO2��Fe2O3��FeO��CaO��Al2O3��MnO�ȣ���
��1?����������������������ʽ��ȫ����ʱ��Һ��pH
| ������ | Al��OH��3 | Fe��OH��3 | Fe��OH��2 | Mn��OH��2 | Mg��OH��2
pHֵ
5.2
3.2
9.7
10.4
11.2
|
��2?�����ε��ܽ�ȣ���λΪg/100gˮ��
| �¶�/�� | 10 | 30 | 40 | 50 | 60
CaSO4
0.19
0.21
0.21
0.20
0.19
MgSO4?7H2O
30.9
35.5
40.8
45.6
/
|
��þ����ȡ��ˮ����þ�Ĺ����������£�
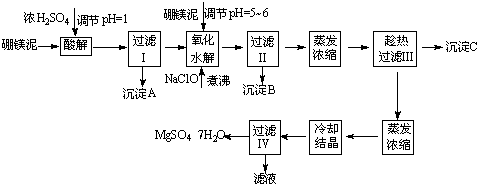
������������ͼ���ο�����pH���ݺ��ܽ�����ݣ��Իش��������⣺
��1������I����Һ�м�����þ�࣬������Һ��pH=5��6���ټ���NaClO��Һ������У�����Һ�е�Mn2+������MnO2����Ӧ�����ӷ�Ӧ����ʽΪ______��������е���ҪĿ����______��
��2������B�г�MnO2��SiO2�����______���ѧʽ�������ʣ�
��3��������ˢ�����Һ���Ƿ���Fe3+��ʵ�鷽����______��
��4������C�Ļ�ѧʽ��______�����ˢ�����ȹ��˵�������______��
5��ѡ���� ���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ���ǣ�?��
A�����Ȼ�����Һ��ʴͭ�壺Cu��Fe3+��Cu2+��Fe2+
B��Fe3O4������ϡHNO3��Ӧ��3Fe3O4��28H+��NO3-��9Fe3+��NO����14H2O
C����С�մ�����θ����ࣺNaHCO3��H+��Na+��CO2����H2O
D����KAl(SO4)2��Һ�е���Ba(OH)2��Һ�����������ʵ������