微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某校化学课外活动小组利用下面所提供的仪器装置和药品制取NaHCO3溶液,设计如下实验。实验室提供的药品、仪器装置如下:
药品:①2%NaOH溶液 ②稀HCl ③稀H2SO4 ④饱和KHCO3溶液 ⑤浓H2SO4 ⑥CaCO3固体 ⑦K2CO3粉末
仪器装置(如图所示):
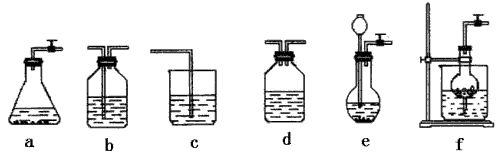
请根据题目要求回答下列问题:
(1)请按下表要求、填写选择的装置和药品。
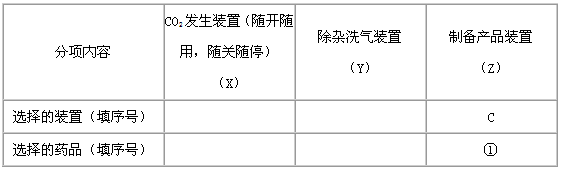
(2)如何检验所选择的CO2发生装置(X)的气密性,请写出主要操作过程:___________________ (3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为_______________,Y装置中除去的杂质为________________
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其原因是___________________;通入过量CO2后,Z装置内的溶液中离子浓度大小顺序为___________________;若要保证乙装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过_________%(质量分数)。
附:有关物质在常温(20℃)时的溶解度
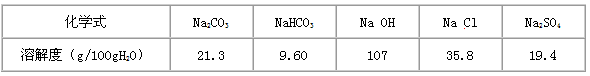
参考答案:
(1)
(2)方案1:塞紧单孔塞,关闭开关,将烧杯中加入一定量水使干燥管下端管口浸没在水中,如果干燥管内外液面有一定高度差,说明装置的气密性良好。
方案2:塞紧单孔塞,关闭开关,将烧杯中加入一定量水使干燥管下端管口浸没在水中,如果用手捂住干燥管,管口处出现少量气泡,松手后,干燥管下端管口处出现一段水柱,说明装置的气密性良好
(3)CaCO3+2H+==Ca2++CO2↑+H2O;HCl(或氯化氢)
(4)使溶液中的NaOH完全转化为NaHCO3? ;c(Na+)>c(HCO3-)>c(OH-)>c(H+)]
([或c(Na+)>c(HCO3-)>c(OH-)>c(CO32-)>c(H+)]?; 4.40%(4.39%或4.41%)
本题解析:
本题难度:一般
2、实验题 纳米材料二氧化钛(TiO2)可做优良的催化剂。
(1)工业上二氧化钛的制备方法是
Ⅰ.将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应,制得混有SiCl4杂质的TiCl4。
Ⅱ.将SiCl4分离,得到纯净的TiCl4。
Ⅲ.在TiCl4中加水、加热,水解得到沉淀TiO2・xH2O。
Ⅳ.T 91Exam.orgiO2・xH2O高温分解得到TiO2。
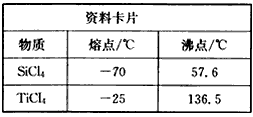
①根据资料卡片中信息判断,TiCl4与SiCl4在常温下的状态是_________,分离二者所采取的操作名称是
__________。
②Ⅲ中反应的化学方程式是___________________。
③如Ⅳ在实验室完成,应将TiO2・xH2O放在______(填仪器编号)中加热。

(2)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2,其过程大致如下:
a.O2→2O b.O+H2O→2OH c.OH+OH→H2O2
①b中破坏的是____(填“极性共价键”或“非极性共价键”)。
②H2O2能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的____ (填“氧化性”或“还原性”)。
(3)某研究小组用下列装置模拟“生态马路”清除CO的原理。(夹持装置已略去)
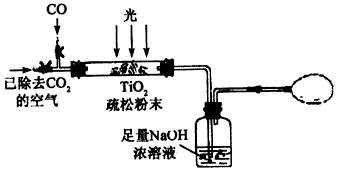
①如缓慢通入22.4 L(已折算成标准状况)CO气体,结果NaOH溶液增重11 g, 则CO的转化率为____。
②当CO气体全部通入后,还要通一会儿空气,其目的是___________。
参考答案:(1)①液态;蒸馏;②TiCl4+(x+2)H2O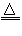 TiO2・xH2O↓+4HCl;③b
TiO2・xH2O↓+4HCl;③b
(2)①极性共价键;②氧化性
(3)①25%;②将残留在装置中的CO2气体排出,被NaOH溶液吸收,减小误差
本题解析:
本题难度:困难
3、选择题 对下列实验过程的评价,正确的是(?)
A.某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐
B.某溶液中滴加BaCl2溶液,生成不溶于稀HNO3的白色沉淀,证明一定含有SO42-
C.某无色溶液滴入酚酞试液显红色,该溶液一定是含有大量的H+
D.验证某不纯的烧碱溶液中是否含Cl-,先加过量的稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明含Cl-
参考答案:D
本题解析:略
本题难度:简单
4、实验题 为了探究铜与浓硫酸的反应,某研究性学习小组做了如下实验
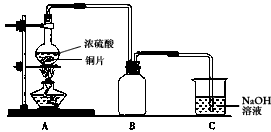
①在放有铜片的圆底烧瓶中加入10mL浓硫酸,加热煮沸10min(如图所示)后,所得固体分离除去未反应的铜片,再经水洗仍有大量黑色不溶物。
②取少量不溶物,向其中加入几滴浓硝酸,产生大量红棕色气体。
③取少量不溶物,向其中加5mL酒精,充分振荡后,静置、过滤,把滤液移入盛有水的小试管中,振荡,出现浑浊。
④取少量不溶物,向其中加入3mL氨水,振荡,溶液呈无色,在空气中静置,溶液变为深蓝色。
⑤取少量不溶物,向其中加入浓盐酸并加热,沉淀几乎全部溶解。为了解释上述现象,学习小组通过查阅资料了解到。
a.铜与浓硫酸反应的不溶性副产物可能有:CuS、Cu2S、Cu2O、S等物质;
b.CuS和Cu2S都能溶于热的浓盐酸;
c.Cu2O能溶于氨水生成无色的[Cu(NH3)2]+,[Cu(NH3)2]+在氨水中被空气中的氧气氧化成深蓝色的
[Cu(NH3)4]2+。
回答下列问题:
(1)实验结束后,装置C中的溶液中可能含有的溶质有__________________。
(2)第②步操作要注意的问题是_________________________;对比①②两步操作中的现象,你能得到的结论是_________________________。
(3)第③步操作中出现的沉淀是__________________,请解释出现这一现象的原因_______________。
(4)写出④步涉及的离子方程式______________________________。
(5)综合分析铜与浓硫酸的反应,生成的不溶物是___________________________。
(6)某工厂拟用废铜屑制备硫酸铜,请你分析利用上述实验原理是否可行。若可行,请说明理由____________________________________。若不可行,请设计更合理的实验方案(用化学反应方程式表示)
______________________________。
参考答案:(1)Na2SO3、NaOH、Na2SO4
(2)必须在密闭系统中(或在通风厨中)进行,防止污染空气(或防止中毒);黑色沉淀中有还原性物质,浓硝酸的氧化性强于浓硫酸。
(3)硫(或S);硫微溶于酒精但不溶于水,将硫的酒精溶液倒入水中,即可析出固体硫
(4)Cu2O+4NH3・H2O=2[Cu(NH3)2]++2OH-+3H2O,4[Cu(NH3)2]++8NH3・H2O+O2=4[Cu(NH3)4]2++4OH-+
6H2O
(5)Cu2O、S以及CuS和Cu2S中的一种或两种
(6)“略”
本题解析:
本题难度:困难
5、实验题 (10分)某化学学习小组在实验室里利用下图装置测定中和反应中的热效应。实验时将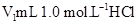 溶液和
溶液和 未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,所得实验结果如右下图所示(实验中始终保持
未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,所得实验结果如右下图所示(实验中始终保持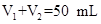 )。
)。
据此请回答下列问题:
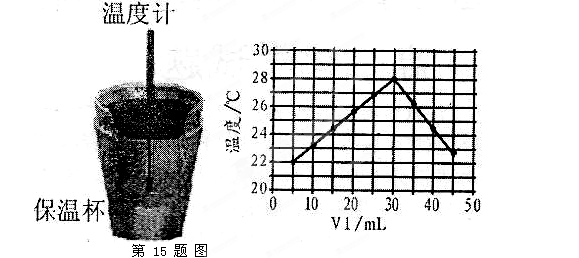 (1)从实验装置上看,左图中尚缺少的一种玻璃用品是________________________。
(1)从实验装置上看,左图中尚缺少的一种玻璃用品是________________________。
(2)保温杯的作用是_______________________________________________________。
(3)某同学根据所得数据,提出了以下观点,其中正确的是______________________。
A.做该实验时环境温度为22℃
B.该实验表明化学能可以转化为热能
C.该实验表明有水生成的反应都是放热反应
(4)利用图中所给数据,可测得NaOH溶液的浓度约为______________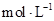
(5)除了使用保温杯外,为了保证实验成功,还要注意哪些问题(说出1点即
可) ____________________________
参考答案:(1)环形玻璃搅拌器(2)防止热量散失(3)B (4)1.5 (5)使用的盐酸和氢氧化钠溶液的浓度要小不要大;温度计的水银球部分要完全浸在溶液中(合理给分)。
本题解析:(1)反应时需要搅拌,所以还缺少环形环形搅拌棒。
(2)在实验中,应该尽可能减少热量的损失,所以保温杯的作用是减少热量的损失。
(3)根据图像可知,当V1=0时,溶液的温度不是22℃,A不正确。随着反应的进行,溶液的温度升高,所以反应放热,B正确。选项C和实验无关系,不正确,答案选B。
(4)当酸碱恰好反应时,放出的热量最多,所以根据图像可判断,氢氧化钠的浓度是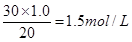 。
。
(5)在实验中,应该尽可能减少热量的损失,所以使用的盐酸和氢氧化钠溶液的浓度要小不要大;温度计的水银球部分要完全浸在溶液中
本题难度:一般