微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 在密闭容器中将NO2加热到某温度时,进行如下的反应:2NO2 2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。
2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。
试求:
(1)NO2的转化率为?
(2)反应前后的压强比为多少?
(3)用O2来表示的反应速率是多少mol・L-1・min-1
参考答案:(1)80%
(2)P前/P后= 5/7
(3)0.024 mol・L-1・min-1
本题解析:
本题难度:一般
2、填空题 (15分)已知化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。请回答下列问题:
(1)可逆反应FeO(s)+CO(g) Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
?
①写出该反应平衡常数的表达式__________。
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,若升高温度,混合气体的平均相对分子质量_____;充入氦气,混合气体的密度____(选填“增大”、“减小”、“不变”)。
(2)常温下,浓度均为0.1 mol・L-1的下列六种溶液的pH如下表:
溶质
| CH3COONa
| NaHCO3
| Na2CO3
| NaClO
| NaCN
| C6H5ONa
|
pH
| 8.8
| 9.7
| 11.6
| 10.3
| 11.1
| 11.3
|
①上述盐溶液中的阴离子,结合质子能力最强的是?
②根据表中数据判断,浓度均为0.01 mol・L-1的下列五种物质的溶液中,酸性最强的是?;
将各溶液分别稀释100倍,pH变化最小的是?(填编号)。
A.HCN?B.HClO?C.C6H5OH?D.CH3COOH ?E.H2CO3
③据上表数据,请你判断下列反应不能成立的是?(填编号)。
A.CH3COOH+ Na2CO3=NaHCO3+CH3COONa? B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO?D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为?
(3)已知常温下Cu(OH)2的Ksp=2×10-20。又知常温下某CuSO4溶液里c(Cu2+)=0.02 mol・L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于?;要使0.2 mol・L-1的CuSO4溶液中Cu2+沉淀较为完全 ( 使Cu2+浓度降至原的千分之一)则应向溶液里加NaOH溶液,使溶液pH为?。
参考答案:⑴? ①k=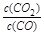 ?;②减小;增大
?;②减小;增大
⑵? ①CO32-;②D;C;③? C D;④2Cl2+CO32-+H2O=CO2↑+2Cl-+2HClO。⑶ 5; 6。
本题解析:(1)①该反应平衡常数的表达式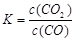 ;②由于温度升高,化学平衡常数减小。说明升高温度,平衡逆向移动,逆反应方向是吸热反应,所以该反应的正反应是放热反应。若升高温度,平衡逆向移动,气体的质量减小,而气体的物质的量不变,所以混合气体的平均相对分子质量减小;充入氦气,化学平衡不发生移动,但在整个容器内气体的质量增大,所以混合气体的密度增大;(2)①同种浓度的离子结合质子能力越强,则盐水解程度就越大,盐溶液的碱性就越强,即pH越大。由于Na2CO3溶液的pH最大,说明CO32-与H+结合力最强。因此上述盐溶液中的阴离子,结合质子能力最强的是CO32-。③发生反应时应该是强酸制取弱酸。A.酸性CH3COOH> H2CO3,正确。B.酸性CH3COOH> HCN.正确。C. H2CO3>HClO。正确。D.由于酸性:H2CO3>C6H5OH> HCO3-,所以会发生反应CO2+H2O+C6H5ONa=NaHCO3+C6H5OH。错误。④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为:2Cl2+CO32-+H2O=CO2↑+2Cl-+2HClO。(3)c (Cu2+)・c2(OH-)≥Ksp=2×10-20; c2(OH-)≥2×10-20÷0.02=1×10-18; c(OH-)≥1×10-9;所以pH=5; c(Cu2+)= 0.2 mol/L÷1000=2×10-4mol/L,则c2(OH-)≥2×10-20÷2×10-4mol/L=1×10-16,所以c(OH-)≥1×10-8;pH=6.
;②由于温度升高,化学平衡常数减小。说明升高温度,平衡逆向移动,逆反应方向是吸热反应,所以该反应的正反应是放热反应。若升高温度,平衡逆向移动,气体的质量减小,而气体的物质的量不变,所以混合气体的平均相对分子质量减小;充入氦气,化学平衡不发生移动,但在整个容器内气体的质量增大,所以混合气体的密度增大;(2)①同种浓度的离子结合质子能力越强,则盐水解程度就越大,盐溶液的碱性就越强,即pH越大。由于Na2CO3溶液的pH最大,说明CO32-与H+结合力最强。因此上述盐溶液中的阴离子,结合质子能力最强的是CO32-。③发生反应时应该是强酸制取弱酸。A.酸性CH3COOH> H2CO3,正确。B.酸性CH3COOH> HCN.正确。C. H2CO3>HClO。正确。D.由于酸性:H2CO3>C6H5OH> HCO3-,所以会发生反应CO2+H2O+C6H5ONa=NaHCO3+C6H5OH。错误。④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为:2Cl2+CO32-+H2O=CO2↑+2Cl-+2HClO。(3)c (Cu2+)・c2(OH-)≥Ksp=2×10-20; c2(OH-)≥2×10-20÷0.02=1×10-18; c(OH-)≥1×10-9;所以pH=5; c(Cu2+)= 0.2 mol/L÷1000=2×10-4mol/L,则c2(OH-)≥2×10-20÷2×10-4mol/L=1×10-16,所以c(OH-)≥1×10-8;pH=6.
本题难度:一般
3、选择题 在密闭容器中充入4mol SO2和 O2,在一定条件下建立平衡:2SO2(g) + O2(g) ? ?2SO3(g) △H,若SO2的转化率为90%,则在此条件下,反应放出的热量为(?)
A.3.6△H
B.1.8△H
C.2△H
D.0.9△H
参考答案:B
本题解析:由反应2SO2(g) + O2(g) ? ?2SO3(g) △H
起始物质的量? 4mol? 3mol? 0
变化物质的量? 3.6 mol? 1.8 mol? 3.6 mol
平衡物质的量? 0.43.6 mol? 1.2 mol? 3.6 mol
可逆反应方程式中的反应热为反应物完全转化为生成物时的反应热,在该反应中,每消耗2mol SO2放出的热量为△H,则反应3.6 mol SO2放出的热量为1.8△H;
本题难度:一般
4、选择题 下列事实,不能用勒夏特列原理解释的是
A.硫酸工业中,增大O2的浓度有利于提高SO2的转化率
B.对2HI H2+I2平衡体系增加压强使颜色变深
H2+I2平衡体系增加压强使颜色变深
C.开启啤酒瓶后,瓶中立刻泛起大量泡沫
D.滴有酚酞的氨水溶液,适当加热溶液(氨气不挥发)后颜色变深
参考答案:B
本题解析:如果改变影响平衡的1个条件,平衡就向能够减弱这种改变的方向进行,中这就是勒夏特列原理,该原理适用于所有的平衡体系。A、硫酸工业中,增大O2的浓度平衡向生成三氧化硫的反应进行,因此有利于提高SO2的转化率,适用于勒夏特列原理;B、对2HI H2+I2平衡体系增加压强,反应速率加快,但反应前后体积不变,因此平衡不移动。由于单质碘的浓度增大,从而使颜色变深,不能适用于勒夏特列原理,B正确;C、气体的溶解度随压强的增大而降低,因此开启啤酒瓶后,压强降低瓶中立刻泛起大量泡沫,适用于勒夏特列原理;D、一水合氨是弱电解质,存在电离平衡。电离是吸热的,因此滴有酚酞的氨水溶液,适当加热溶液(氨气不挥发)后促进一水合氨的电离,溶液的碱性增强,所以颜色变深,适用于勒夏特列原理,答案选B。
H2+I2平衡体系增加压强,反应速率加快,但反应前后体积不变,因此平衡不移动。由于单质碘的浓度增大,从而使颜色变深,不能适用于勒夏特列原理,B正确;C、气体的溶解度随压强的增大而降低,因此开启啤酒瓶后,压强降低瓶中立刻泛起大量泡沫,适用于勒夏特列原理;D、一水合氨是弱电解质,存在电离平衡。电离是吸热的,因此滴有酚酞的氨水溶液,适当加热溶液(氨气不挥发)后促进一水合氨的电离,溶液的碱性增强,所以颜色变深,适用于勒夏特列原理,答案选B。
本题难度:一般
5、简答题 t℃时,将3molA和1molB气体通入容积为2L的密闭容器中(容积不变),发生如下反应:3A(g)+B(g)
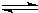
xc(g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol?L-1.请计算:
(1)从反应开始到平衡状态,生成C的平均反应速率;
(2)x的值.
参考答案:(1)2min时反应达到平衡状态,容器C的浓度为0.4mol?L-1,
所以C的平均反应速率v(C)=△c△t=0.4mol/L2min=0.2mol/(L?min),
答:C的平均反应速率为0.2mol/(L?min);
(2)参加反应的B的物质的量为1mol-0.8mol=0.2mol,
生成的C的物质的量为0.4mol?L-1×2L=0.8mol,
所以0.2mol:0.8mol=1:x,
解得x=4,
答:x的值为4.
本题解析:
本题难度:一般