微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 在一固定容积的密闭容器中,保持一定条件下进行以下反应:X(气)+2Y(气)?3Z(气).加入1mol X和3mol Y.达到平衡后,生成a?mol?Z.
(1)达到平衡时,Z在反应混合气体中的体积分数是______.
(2)在相同实验条件下,若在同一容器中改为加入2mol?X和6mol?Y,达到平衡后,Z的物质的量为______mol.
(3)在相同实验条件下,若在同一容器中改为加入2mol?X和7mol?Y,达到平衡后若要求在反应混合气体中Z的体积分数不变,还需加入Z______mol.
2、填空题 反应aA(g)+bB(g) cC(g)+dD(g)在容积不变的密闭容器中达到平衡,且起始时A与B的物质的量之比为
cC(g)+dD(g)在容积不变的密闭容器中达到平衡,且起始时A与B的物质的量之比为
a:b,则:
(1)平衡时A、B的转化率之比是_________________。
(2)若同等倍数地增大A、B的物质的量浓度,且要使A与B的转化率同时增大,(a+b)与(c+d)所满足的关系是a+b_______c+d。填(>、<、=或没关系)
(3)若设定a=2,b=1,c=3,d=2,在甲、乙、丙、丁4个相同恒容容器中A的物质的量依次是2mol、
1mol、2mol、1mol,B的物质的量依次是1mol、1mol、2mol、2mol,C和D的物质的量均为0。则等温条件下达到平衡时,A的转化率最大的容器是______________,B转化率由大到小的顺序是_______________(填容器序号) 。
3、填空题 (8分)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
T/℃
| 700
| 800
| 830
| 1 000
| 1 200
|
K
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
|
回答下列问题:
(1)该反应为________反应(填“吸热”“放热”).
(2)能判断该反应是否已达化学平衡状态的依据是________.
a.容器中压强不变? b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O)d.c(CO2)=c(CO)
(3)某温度下,在2 L的密闭容器中,加入1 mol CO2和1 mol H2充分反应达平衡时,CO平衡浓度为0.25 mol/L,试判断此时的温度为________℃.
(4)若在(3)所处的温度下,在1 L的密闭容器中,加入2 mol CO2和3 mol H2充分反应达平衡时,H2的物质的量为________.
a.等于1.0 mol b.大于1.0 mol
c.大于0.5 mol?d.无法确定
4、计算题 已知850℃时,CO(g)+H2O(g) CO2(g)+H2(g)的K=1。850℃时,若在容积为2L的密闭容器中同时充入1.0mol CO,3.0mol H2O,1.0mol CO2和xmol H2。
CO2(g)+H2(g)的K=1。850℃时,若在容积为2L的密闭容器中同时充入1.0mol CO,3.0mol H2O,1.0mol CO2和xmol H2。
(1)当x=5.0时,判断化学反应进行的方向。
(2)若要使上述反应开始时向正反应方向进行,则x应满足的条件是什么?
(3)若x=5.0,当上述反应达到平衡后,计算H2的体积分数。
5、填空题 (12分).随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
(1)目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作冷剂已成为一种趋势,这一做法对环境的积极意义在于?。
(2)将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
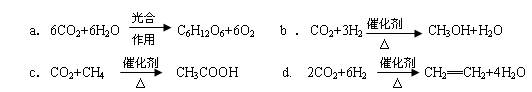
以上反应中,最节能的是?,原子利用率最高的是?。
(3)为探究用CO2来生产燃料甲醇的反应原理,现进行如下实验:
在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:
 ? CO2(g)+3H2(g)? CH3OH(g)+H2O(g)△H=-49.0kJ/mol
? CO2(g)+3H2(g)? CH3OH(g)+H2O(g)△H=-49.0kJ/mol
测得CO2和CH3OH(g)的浓度随时间变化如图所示。
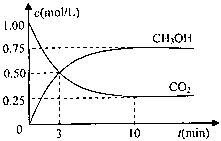
①从反应开始到平衡,氢气的平均反应速率v(H2)=?mol/(L・min)
②该反应的平衡常数表达式为?,升高温度,平衡常数的数值将
?(填“增大”、“减小”或“不变”)。
③下列措施中能使n(C H3OH)/n(CO2)增大的是?.
A.升高温度
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离
D.再充入1molCO2和3molH2

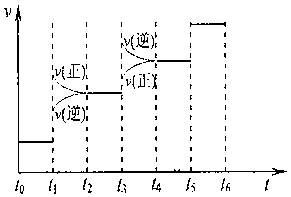 ?
?