微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,有下列四种溶液:
①
| ②
| ③
| ④
|
0.1mol/L
NaOH溶液
| pH=11
NaOH溶液
| 0.1mol/L
CH3COOH溶液
| pH=3
CH3COOH溶液
|
下列说法正确的是
A.由水电离出的c(H+):③<①
B.③稀释到原来的100倍后,pH与④相同
C.①与③混合,若溶液pH=7,则V(NaOH)>V(CH3COOH)
D.②与④混合,若溶液显酸性,则所得溶液中离子浓度可能为:c(CH3COOˉ)> c(H+) > c(Na+)>c(OHˉ)
参考答案:D
本题解析:A项,NaOH完全电离,CH3COOH部分电离,前者对水的电离抑制程度大,故由水电离出的c(H++):①<③;B项,0.1mol・L-1CH3COOH溶液,稀释100倍,无法计算其pH值,错误;C项,①③若等体积混合,溶液呈碱性,若呈中性,则碱不足,即V(NaOH)<V(CH3COOH);D项c(CH3COOˉ)>c(H+)>c(Na+)>c(OHˉ)是CH3COOH过量很多的情况,正确。
考点:酸碱对水的电离平衡的影响,酸碱的混合时的pH计算,盐的水解,溶液中离子浓度的比较。
本题难度:一般
2、填空题 已知H2A是一种无机二元酸,请回答以下问题:
(1) 若H2A为二元弱酸,在水溶液中的电离方程式为 ;
(2) 若NaHA溶液显碱性,则H2A是 (填“强酸”、“弱酸”或“无法确定”),原因是 。
(3) 若溶液显酸性,在25℃下,若向0.1 mol・L-1的NaHA溶液中逐滴滴加0.1 mol・L-1 KOH溶液至溶液呈中性。此时该混合溶液中下列关系中,一定正确的是 ;
a.c(H+)・c(OH-)=1×10-14 b.c(Na+)+c(K+)=0.1 mol・L-1
c.c(Na+)>c(K+) d.c(Na+)=c(HA-)+c(A2-)
参考答案:
(1)H2A H++HA-,HA-
H++HA-,HA- H++A2-(2分)
H++A2-(2分)
(2)弱酸(1分)HA-水解生成H2A和OH-使溶液显碱性,故H2A必为弱酸;(2分)
(3)a(2分) ;
本题解析:(1)多元弱酸部分电离,分步书写。(2)若NaHA溶液显碱性, 说明HA-水解生成H2A和OH-使溶液显碱性,故H2A必为弱酸;(3)在25℃下,任何溶液一定存在c(H+)・c(OH-)=1×10-14,故a正确;滴加到溶液刚好反应时,生成Na2A和K2A,溶液呈碱性,要成中性必须NaHA过量,故b错、C错;根据物料守恒:c(Na+)=c(HA-)+c(A2-)+ c(H2A),故d错。
考点:考查弱电解质的电离、盐类水解、水溶液中的离子平衡等相关知识。
本题难度:一般
3、填空题 (10分)(1)现有NH4Cl和NH3・H2O组成的混合溶液,若其pH=7,则该溶液中c(NH4+)___c(Cl-);若pH>7,则该溶液中c(NH4+)______c(Cl-)。(填“>”、“<”、“=”).
(2)0.1mol/L的NaHCO3溶液中,按物质的量浓度由大到小顺序排列该溶液中各种微粒(水分子除外) ,c(Na+)+c(H+)=_______________ ,c(Na+)=____________
参考答案:(1)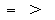 (2)c(Na+)> c(HCO3-)> c(OH-)> c(H2CO3)> c(H+)> c(CO32-)。c(Na+)+ c(H+)= c(HCO3-)+ c(OH-)+2 c(CO32-), c(Na+)= c(HCO3-)+c(H2CO3)+ c(CO32-)。
(2)c(Na+)> c(HCO3-)> c(OH-)> c(H2CO3)> c(H+)> c(CO32-)。c(Na+)+ c(H+)= c(HCO3-)+ c(OH-)+2 c(CO32-), c(Na+)= c(HCO3-)+c(H2CO3)+ c(CO32-)。
本题解析:(1)氯化铵和氨水的混合溶液,若pH=7,说明溶液为中性,即氢离子浓度=氢氧根离子浓度,根据电荷守恒,则铵根离子浓度=氯离子浓度。若pH>7,溶液为碱性,即氢离子浓度<氢氧根离子浓度,根据电荷守恒知铵根离子浓度大于氯离子浓度。(2)碳酸氢钠溶液中存在碳酸氢根电离和水解,水解大于电离,所以离子浓度大小顺序为: c(Na+)> c(HCO3-)> c(OH-)> c(H2CO3)> c(H+)> c(CO32-)。根据电荷守恒知道:c(Na+)+ c(H+)= c(HCO3-)+ c(OH-)+2 c(CO32-),根据物料守恒,即c(Na+)= c(HCO3-)+c(H2CO3)+ c(CO32-)。
考点:溶液中的离子浓度关系。
本题难度:一般
4、选择题 下列有关物质浓度关系的描述中,正确的是
A.25℃时,NaB溶液的pH=9,则c(Na+)-c(B-)=9.9×10-7mol・L-1
B.0.1mol・L-1的NaHCO3溶液中:c(OH-)+2c(CO32-)=c(H+)+c(H2CO3)
C.25℃时,向0.1mol・L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
D.25℃时,将pH均为3的醋酸溶液和盐酸分别加水稀释到pH均为5,则由水电离出的H+的浓度均减小为原来的100倍