|
|
|
高考化学知识点归纳《盐类水解的原理》试题强化练习(2017年最新版)(七)
2017-09-24 00:28:42
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
A.明矾水解形成的Al(0H)3胶体能杀菌消毒,可用于水的净化
B.镀锡的铁制品比镀锌的铁制品耐用
C.乙醇和乙酸都能溶于水,都是电解质
D.分别与等物质的量的HC1和CH3COOH恰好中和时,消耗NaOH的物质的量相同
|
2、选择题 下列说法正确的是

A.①表示化学反应2NO2(g) + O3(g)  N2O5(g) + O2(g)△H> 0 N2O5(g) + O2(g)△H> 0
B.②表示25℃时,用0.1 mol/LCH3COOH溶液滴定20 mL 0.1 mol/LNaOH溶液,溶液的pH随加入酸体积的变化
C.③表示10 mL 0.01 mol/L KMnO4酸性溶液与过量的0.1 mol/LH2C2O4溶液混合时,n (Mn2+)随时间的变化
D.④表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液
|
3、填空题 利用硫酸渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:
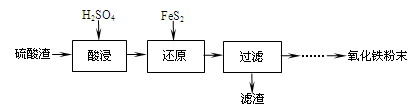
(1)“酸浸”中硫酸要适当过量,目的是:①提高铁的浸出率,② 。
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO42-,该反应的离子方程式为
。
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量。实验步骤为:
准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定,有关反应方程式如下:
2Fe3++Sn2++6Cl-=2Fe2++SnCl62-,
Sn2++4Cl-+2HgCl2=SnCl62-+Hg2Cl2↓,
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O。
①若SnCl2不足量,则测定的Fe3+量 (填“偏高”、“偏低”、“不变”,下同)。
②若不加HgCl2,则测定的Fe3+量 。
(4)①可选用 (填试剂)检验滤液中含有Fe3+。产生Fe3+的原因是
(用离子反应方程式表示)。
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物
| Fe(OH)3
| Al(OH)3
| Fe(OH)2
| Mg(OH)2
| Mn(OH)2
|
开始沉淀
| 2.7
| 3.8
| 7.5
| 9.4
| 8.3
|
完全沉淀
| 3.2
| 5.2
| 9.7
| 12.4
| 9.8
|
实验可选用的试剂有:稀HNO3、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体。请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
a. 氧化:
;
b. 沉淀:
;
c. 分离,洗涤; d. 烘干,研磨。
4、选择题 25℃时,0.1mol/L下列溶液的pH如下表,有关比较错误的是
序 号
| ①
| ②
| ③
| ④
|
溶液
| NaCl
| CH3COONH4
| NaF
| NaHCO3
|
pH
| 7.0
| 7.0
| 8.1
| 8.4
|
A.酸的强度:HF>H2CO3
B.由水电离产生的c(H+):①=②
C.溶液中离子的总浓度:①>③
D.④溶液中:c(HCO3-)+c(CO32-)+c(H2CO3)
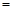
0.1 mol/L
5、选择题 将0.4 mol/L的CH3COOK与0.2 mol/L的HCl等体积混合后,溶液中下列微粒的物质的量浓度关系正确的是
A.c(CH3COO-)=c(Cl-)>c(H+)>c(OH-)
B.c(CH3COO-)=c(Cl-)>c(H+)>c(CH3COOH)
C.c(K+)+c(H+)=c(CH3COO-)+c(Cl-)
D.c(K+)>c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)

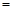 0.1 mol/L
0.1 mol/L