��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ�������������������ʡ�ȡ��������Ʒ�ֱ�Ͷ��������ϡ�����������ϡ����������Һ�У��ų�������H2����ô���������Ĺ�ϵ��ȷ����
A�����ʵ���֮��Ϊ1:1
B�����ʵ���֮��Ϊ2:1
C������֮��Ϊ1:1
D������֮��Ϊ2:1
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
2��ѡ���� �����й�����˵����ȷ����
A�������������������������Һ�ֱ�Ӧ������0.2 mol����ʱ��ʧȥ�ĵ�������ͬ
B�������������ᷴӦ(����AlCl3)��������NaOH��Һ��Ӧ(����NaAlO2)�����Խ�������������
C�����������ڿ������γ�һ�����ܵ�����Ĥ�������һ�ֱȽϻ��õĽ��������Խ�������Ͷ�뵽������FeCl3��Һ�У������û���������
D����Ԫ���������ھۼ����࣬�Խ������������龡���������Ʋ;ߡ�����ʳƷ��װ��������������
�ο��𰸣�D
���������A���������ʧ���Ӹ�H�����ɵ�H2����ͬ��ʧ��������ͬ��B���������̸���ԣ�����˵���ǽ������Ѵ��в��ַǽ����ԣ�C��������γ����ܵ�����Ĥ���Ƿ��ǻ��ý�����ֱ�ӹ�ϵ��������Ͷ��FeCl3��Һ���ȷ�����Ӧ��Al��3Fe3��===3Fe2����Al3����Fe3����Ӧ��ȫ���ټ�������������Ӧ��3Fe2����2Al===3Fe��2Al3����
�����Ѷȣ���
3��ѡ���� ʵ��Al3����3 ��6H2O��4Al(OH)3������ȷ��������
��6H2O��4Al(OH)3������ȷ��������
A����������Һ�в��ϼ��봿����Һ
B����������Һ�в��ϼ���С�մ���Һ
C�����ռ���Һ�в��ϵ���������Һ
D����������Һ�в��ϵ����ռ���Һ
�ο��𰸣�C
���������A��B�ж���ˮ����ٽ���������������������CO2��D�������������������������������ƹ���ʱ�����ܽ�����ƫ�����ƣ�������ȷ�Ĵ�ѡC��
�����Ѷȣ�һ��
4��ѡ���� ��MgSO4��Al2(SO4)3�Ļ����Һ��, ��μ���NaOH��Һ������ͼ����, ����ȷ��ʾ������Ӧ����(�������ʾ����NaOH��Һ�����, �������ʾ��Ӧ���ɳ���������)
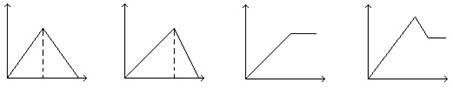
A?B?C?D
�ο��𰸣�D
�����������������ʾ����NaOH��Һ��������������ʾ��Ӧ���ɳ���������������MgSO4��Al2��SO4��3�Ļ����Һ�У���μ���NaOH��Һ������Mg2++2OH-�TMg(OH)2����Al3++3OH-�TAl(OH)3���������������һֱ������ֱ�����Ȼ����Al(OH)3+OH-�TAlO2-+2H2O���������������٣���������þ����Ӧ����������������Ϊһ��ֵ����D��ȷ��
�����Ѷȣ�һ��
5������� ������ijЩ������������ɵĻ�����ڻ�ѧ�ϳ�Ϊ���ȼ����û�����ڸ����������ܷ����û���Ӧ��Ϊȷ��ij���ȼ���Ʒ������������������ɣ��ֱ��������ʵ�飺
��1����ȡ10.7 g����Ʒ�������м���������NaOH��Һ��������ɵ�����(��״������ͬ)���Ϊa L����Ӧ�Ļ�ѧ����ʽ��?����Ʒ����������������?���ú�a�ı���ʽ��ʾ����
��2����ȡͬ��������Ʒ���ڸ�����ʹ��ǡ�÷�Ӧ����a =?L���÷�Ӧ�Ļ�ѧ����ʽ��?��
��3������2���з�Ӧ������ȴ�����������ᣬ������ɵ��������Ϊb L���������루1������������������a��b =_______��
�ο��𰸣��� 2Al + 2NaOH + 2H2O �� 2NaAlO2 + 3H2��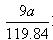 ��0.075a
��0.075a
�� 3.36? 2 Al+ Fe2O3 2Fe + Al2O3
2Fe + Al2O3
�� 3��2
�����������
�����Ѷȣ���